Clear Sky Science · fr
Détection ultrasensible de biomarqueurs de la maladie d’Alzheimer avec des biocapteurs photoniques à nanopiliers
Pourquoi un simple test sanguin pour la perte de mémoire importe
À mesure que de nouveaux médicaments capables de ralentir la maladie d’Alzheimer apparaissent, les médecins ont un besoin urgent de tests simples qui identifient les personnes à risque bien avant l’apparition des symptômes. Aujourd’hui, confirmer un diagnostic d’Alzheimer signifie généralement recourir à des examens cérébraux coûteux ou à des ponctions lombaires que peu de patients reçoivent en soin courant. Cette étude décrit un minuscule capteur optique capable de repérer des molécules clés liées à l’Alzheimer dans une goutte de sang à des niveaux cliniquement significatifs, ouvrant potentiellement la voie à des tests rapides et peu coûteux utilisables en cabinet ou même au chevet du patient.
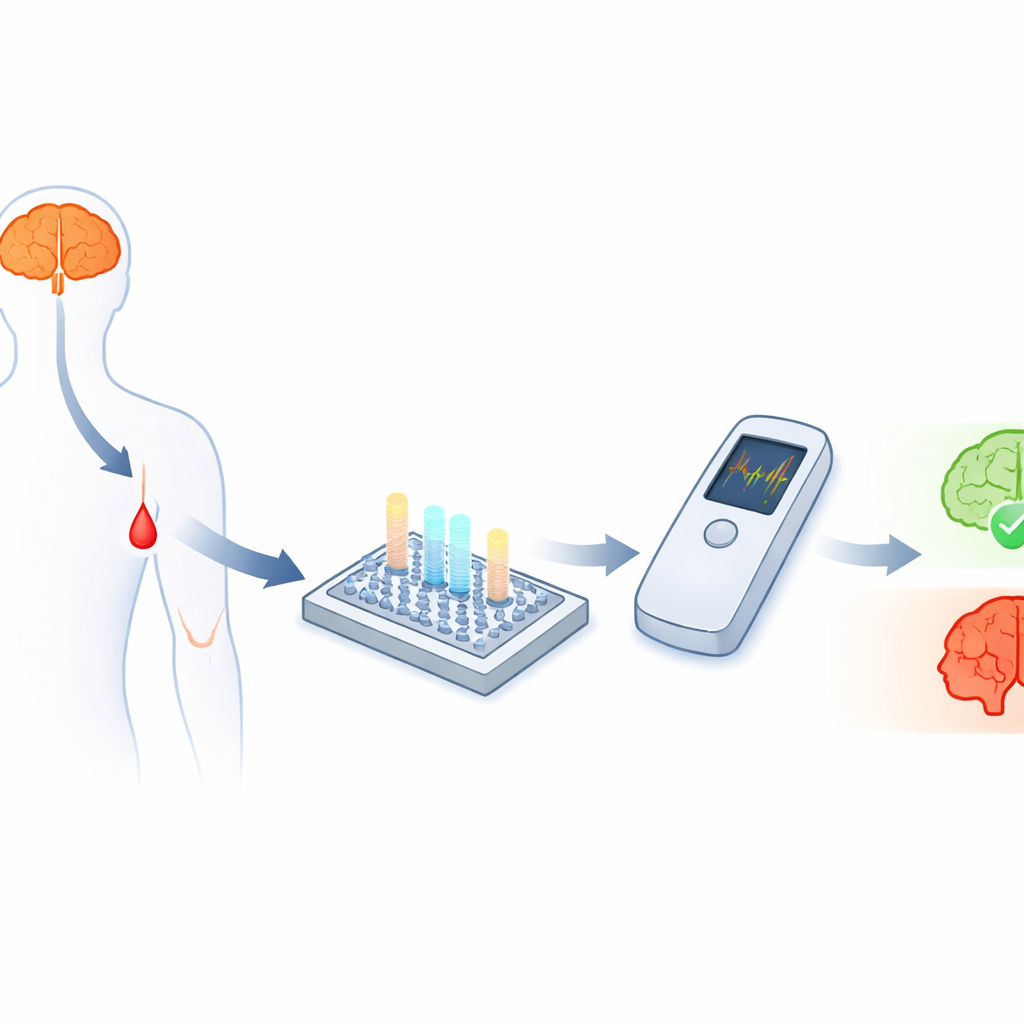
Chercher des indices dans le sang
La maladie d’Alzheimer est étroitement liée à de petits fragments protéiques appelés amyloïde‑bêta, en particulier deux formes connues sous les noms Aβ40 et Aβ42. Leurs quantités, et en particulier leur rapport, fournissent des informations importantes sur la présence et l’évolution de la maladie. Le défi réside dans le fait que ces fragments sont minuscules et circulent dans le sang à des niveaux extrêmement faibles—des billionièmes de gramme par millilitre—ce qui rend leur mesure précise difficile en dehors de laboratoires spécialisés. Bien que des capteurs électrochimiques puissent en principe détecter de telles concentrations, les transformer en tests robustes et abordables utilisables au point de soin et capables de suivre plusieurs biomarqueurs simultanément s’est révélé difficile.
Guider la lumière à travers de minuscules piliers
L’équipe a relevé ce défi en recourant à la nanophotonique—des structures qui contrôlent la lumière à une échelle inférieure à la longueur d’onde. Ils ont construit une puce recouverte d’une grille régulière de paires de piliers en silicium aussi fins que des cheveux, déposés sur du verre. Quand la lumière éclaire cette surface structurée, elle se retrouve piégée dans un mode résonant particulier très sensible aux changements près des sommets des piliers, un peu comme le timbre d’un diapason qui se décale si l’on ajoute de la matière. En ajustant précisément la distance entre les piliers de chaque paire, les chercheurs ont équilibré simultanément trois propriétés cruciales : la netteté de la résonance optique, la sensibilité aux variations de l’environnement et l’amplitude du signal. Cette conception « point idéal » rend la puce particulièrement adaptée à la détection de très petites quantités de matière.
Rendre visibles des molécules invisibles
Même avec ce dispositif optimisé, les marqueurs de l’Alzheimer seuls modifieraient à peine la lumière. Pour amplifier l’effet, les chercheurs ont utilisé une stratégie en sandwich avec des nanoparticules d’or. Tout d’abord, ils ont recouvert la surface du capteur de couches de chimie adhésive qui orientent correctement des anticorps spécialisés afin que leurs sites de liaison soient tournés vers le liquide. Ces anticorps captent soit Aβ40 soit Aβ42 dans l’échantillon. Ensuite, des nanoparticules d’or, chacune décorée d’un second anticorps reconnaissant une autre extrémité du même fragment amyloïde, sont mises en flux sur la puce. Lorsqu’un fragment amyloïde est présent, il fait le pont entre la surface et une particule d’or, « signalant » ainsi sa présence. Parce que l’or perturbe fortement l’environnement optique local, chaque fragment capturé provoque un décalage beaucoup plus important de la résonance du capteur que le peptide seul, augmentant la sensibilité d’environ un à deux ordres de grandeur tout en conservant un signal optique propre.
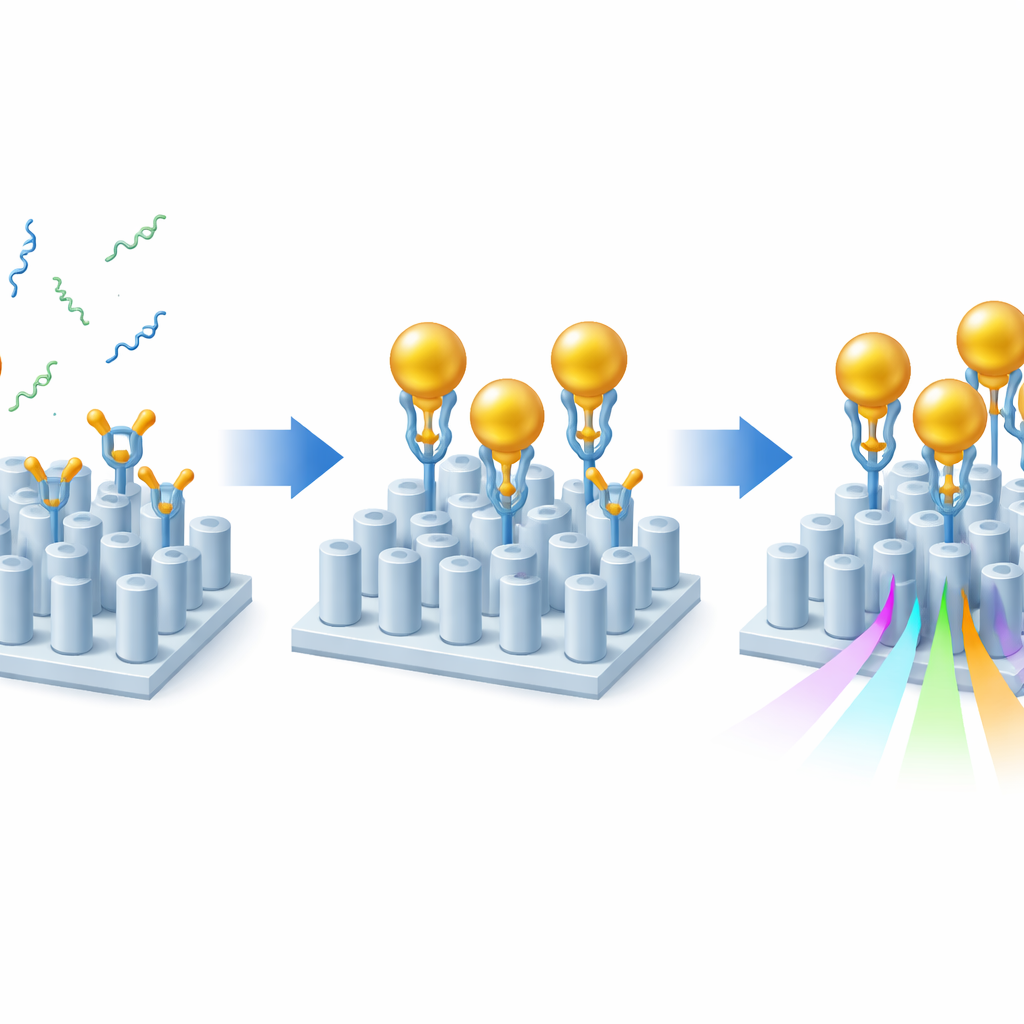
Tester des échantillons réalistes
Pour montrer que l’approche fonctionne au‑delà des tampons de laboratoire, l’équipe a testé son capteur avec du sérum sanguin humain. Ils ont dilué le sérum pour le rendre compatible avec la manipulation microfluidique tout en maintenant des niveaux d’amyloïde représentatifs de ceux observés chez les patients. Fait important, ils ont pu détecter à la fois Aβ40 et Aβ42 à 0,2 picogramme par millilitre dans ce sérum dilué—équivalant au niveau cliniquement pertinent de 20 picogrammes par millilitre dans le sang total. En déposant différents anticorps de capture dans des zones distinctes sur la même puce, ils ont mesuré simultanément les deux formes d’amyloïde au sein d’un unique minuscule canal, une étape clé pour évaluer leur rapport à partir d’un seul petit échantillon. Les signaux distinguaient clairement les échantillons enrichis en amyloïde de ceux ne contenant que les niveaux de fond naturellement présents, y compris chez les personnes en bonne santé.
Ce que cela pourrait signifier pour les soins futurs
Ensemble, ces avancées montrent qu’un capteur compact optique, renforcé par des nanoparticules d’or, peut atteindre les sensibilités requises pour des tests sanguins pertinents pour l’Alzheimer tout en prenant en charge plusieurs biomarqueurs simultanément. Bien que des travaux supplémentaires soient nécessaires pour transformer cela en un dispositif commercial robuste et pour ajouter d’autres marqueurs tels que différentes formes de la protéine tau, la technologie sous‑jacente est fabriquée à partir de matériaux évolutifs et peut être associée à une optique simple et portable. Si elle est pleinement développée, elle pourrait permettre aux cliniciens de surveiller la santé cérébrale à partir d’un petit échantillon sanguin, facilitant grandement la détection précoce de l’Alzheimer et le suivi de l’efficacité des traitements au fil du temps.
Citation: Guilherme S. Arruda, Katie Morris, Augusto Martins, Yue Wang, Sian Sloan-Dennison, Duncan Graham, Steven D. Quinn, Emiliano R. Martins, and Thomas F. Krauss, "Ultrasensitive Alzheimer’s disease biomarker detection with nanopillar photonic crystal biosensors," Optica 12, 1587-1596 (2025). https://doi.org/10.1364/OPTICA.566672
Mots-clés: test sanguin pour la maladie d’Alzheimer, biocapteur nanophotonique, amyloïde bêta, nanoparticules d’or, diagnostic précoce