Clear Sky Science · fr
L’origine de la structure quaternaire de la fibrillation de l’hémoglobine falciforme : une étude en dynamique moléculaire
Pourquoi cette histoire de sang est importante
La drépanocytose naît d’un tout petit changement dans une protéine sanguine, et pourtant ce changement peut remodeler les globules rouges, obstruer les vaisseaux et provoquer des douleurs chroniques. Cette étude examine de près, sur la base de la physique, comment cette substitution unique pousse l’hémoglobine à s’empiler en fibres rigides à l’intérieur de la cellule. En utilisant des simulations informatiques avancées, les auteurs relient des détails atomiques à des problèmes à l’échelle cellulaire, offrant de nouvelles pistes sur la manière dont des futurs médicaments pourraient empêcher l’hémoglobine de bloquer notre circulation.
Un petit échange aux grandes conséquences
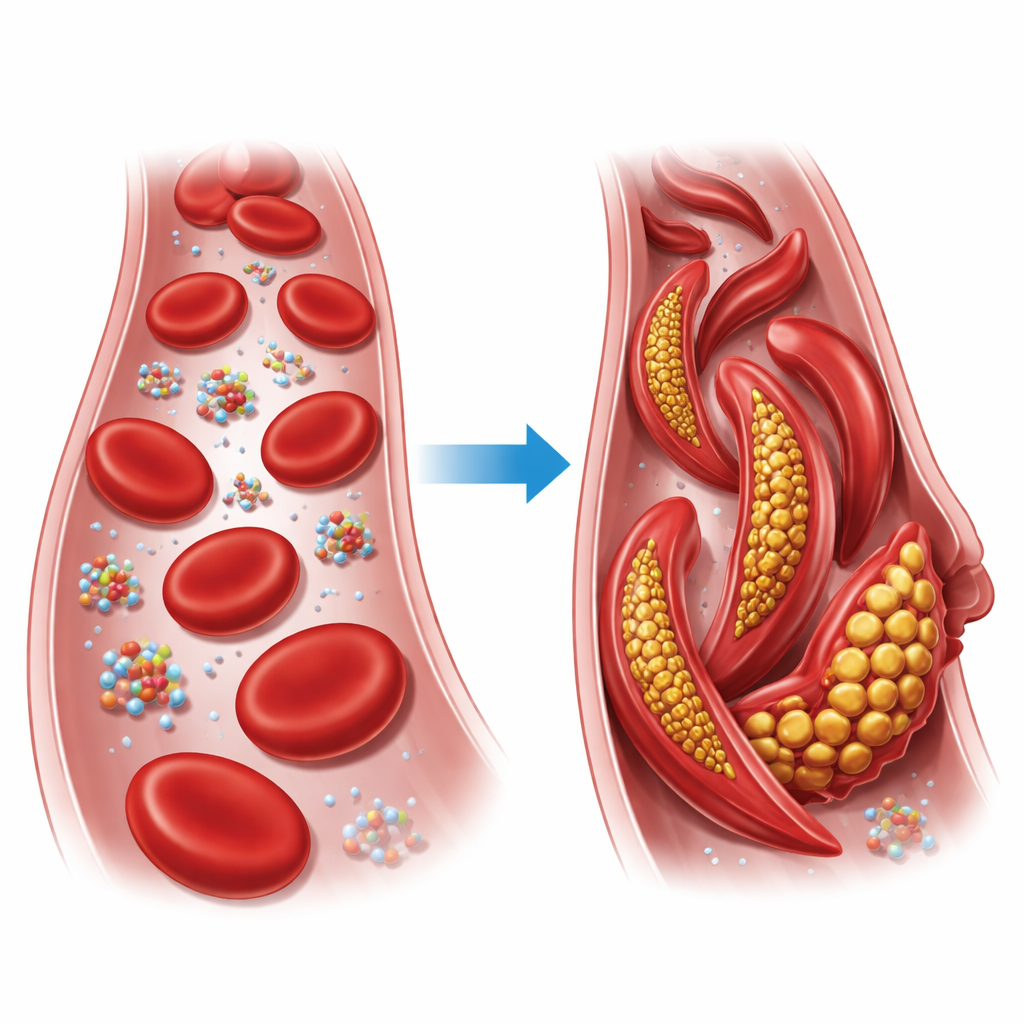
L’hémoglobine est la protéine qui transporte l’oxygène au sein de nos globules rouges. Chaque unité d’hémoglobine est constituée de quatre chaînes qui peuvent s’organiser selon deux conformations principales, connues sous les états relâché (R) et tendu (T). Dans la drépanocytose, un seul acide aminé d’une de ces chaînes est remplacé : un glutamate chargé est substitué par une valine hydrophobe en position six de la chaîne bêta. En conditions de faible oxygénation, cette version altérée, appelée hémoglobine falciforme, s’assemble en longues fibres qui déforment les globules rouges normalement ronds en formes rigides en faucille, capables d’obstruer les petits vaisseaux et de priver les tissus d’oxygène.
Suivre la variation de conformation de l’hémoglobine
Les auteurs se concentrent sur la façon dont des unités complètes d’hémoglobine tournent et se compactent dans une fibre. Ils suivent ce changement de grande échelle à l’aide d’un angle unique qui mesure comment les deux moitiés de la protéine se tordent l’une par rapport à l’autre. En recourant à des simulations de dynamique moléculaire — des expériences virtuelles qui calculent le mouvement des atomes dans le temps en présence d’eau et de sel — ils poussent progressivement cet angle sur une large plage et calculent l’énergie associée à chaque conformation. Ils montrent que l’hémoglobine normale comme la falciforme peuvent explorer de nombreuses conformations à la température corporelle. L’hémoglobine falciforme présente un angle légèrement favorisé, mais ces préférences de conformation seules ne suffisent pas à expliquer pourquoi seule la forme falciforme forme des fibres stables.
Pourquoi les fibres falciformes adhèrent et pourquoi les fibres normales se désagrègent
Pour atteindre le cœur de la formation des fibres, l’étude mesure la force d’attraction entre unités d’hémoglobine voisines le long et à travers la fibre. L’équipe calcule l’énergie cohésive — la force nette qui maintient les unités ensemble — pour de nombreuses conformations globales. Pour l’hémoglobine falciforme, cette énergie cohésive demeure négative (c’est-à-dire attractive) sur toute la plage de conformations testées, de sorte que les fibres restent stables et ne se désorganisent pas facilement. Pour l’hémoglobine normale, en revanche, certaines conformations présentent une énergie cohésive positive, rendant les fibres à ces angles instables et sujettes à une rupture spontanée. Une différence clé réside dans la façon dont les chaînes latérales de valine mutée s’insèrent dans les protéines voisines : dans l’hémoglobine falciforme, ces régions hydrophobes forment des contacts robustes à la fois latéralement et le long de l’axe de la fibre, favorisant directement la croissance des fibres.
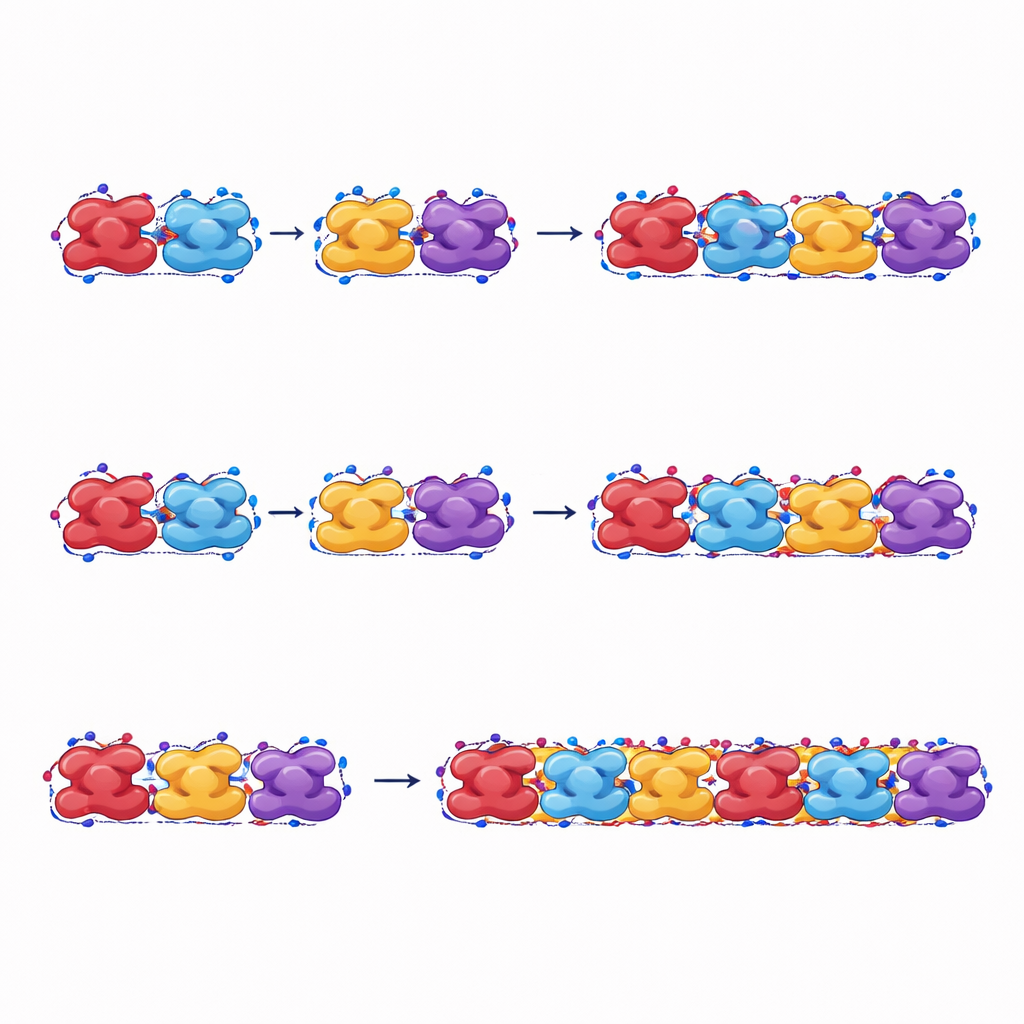
Comment ces fibres supportent des charges et se rompent
Les auteurs étirent aussi leurs fibres simulées pour imiter le stress mécanique. Lorsqu’elles sont tirées le long de leur longueur, les fibres constituées d’hémoglobine falciforme résistent à des forces et des déformations plus élevées et dissipent plus d’énergie avant la rupture que celles faites d’hémoglobine normale. Même la forme relâchée des fibres falciformes, qui n’est pas celle où les fibres apparaissent initialement, peut néanmoins maintenir la chaîne par des changements plastiques de conformation, contribuant à la stabilité de la fibre une fois formée. Les fibres d’hémoglobine normale, en revanche, se séparent plus facilement entre unités voisines et absorbent moins d’énergie avant la défaillance, ce qui confirme qu’elles sont moins stables sous contrainte.
Indications pour de futurs traitements et de nouveaux matériaux
Pris ensemble, les simulations montrent qu’un seul changement d’acide aminé modifie la façon dont les unités d’hémoglobine s’agencent, faisant basculer l’assemblage global vers des angles qui favorisent une attraction forte, en particulier dans l’état tendu. Cette combinaison de géométrie et d’adhérence permet à l’hémoglobine falciforme de former de longues fibres rigides qui résistent aussi bien aux mouvements thermiques qu’aux contraintes mécaniques, déformant en fin de compte les globules rouges et obstruant le flux sanguin. En mettant en évidence des caractéristiques précises de l’arrangement global de la protéine qui contrôlent la stabilité des fibres, ce travail suggère que des médicaments antisickling efficaces pourraient agir en poussant l’hémoglobine vers des conformations où les fibres deviennent énergétiquement défavorables et mécaniquement fragiles — transformant ainsi un embouteillage moléculaire mortel en une circulation sanguine libre à nouveau.
Citation: Jiang, M., Qin, Z. The quaternary structure origin of the fibrillation of sickle hemoglobin: a molecular dynamics study. npj Soft Matter 2, 7 (2026). https://doi.org/10.1038/s44431-026-00019-8
Mots-clés: drépanocytose, fibres d’hémoglobine, agrégation protéique, dynamique moléculaire, troubles sanguins