Clear Sky Science · fr
Combler le fossé calculatoire‑expérimental : exploiter un grand modèle de langage pour prioriser les thérapeutiques de la maladie d’Alzheimer en comparant des modèles d’apprentissage
Pourquoi cela compte pour les familles et les patients
La maladie d’Alzheimer prive les personnes de leur mémoire, de leur autonomie et de leur qualité de vie, et pourtant les traitements véritablement efficaces restent rares. Cette étude explore une manière plus rapide de trouver de nouveaux traitements en réutilisant des médicaments existants, en combinant des modèles informatiques puissants avec un grand modèle de langage — le même type d’IA utilisé aujourd’hui dans les chatbots — pour analyser d’énormes volumes de données médicales et d’articles scientifiques. L’objectif est de réduire une longue liste de médicaments possibles à un petit ensemble réaliste que les chercheurs et les cliniciens peuvent réellement tester chez les patients.
Réutiliser d’anciens médicaments à de nouveaux usages
Développer un médicament entièrement nouveau peut prendre plus d’une décennie et coûter des milliards de dollars, sans garantie de succès. Une alternative est le « repositionnement de médicaments », qui recherche de nouveaux usages pour des médicaments déjà approuvés pour d’autres pathologies, comme la maladie de Parkinson ou la dépression. Parce que ces médicaments ont des profils de sécurité connus, ils peuvent souvent passer plus rapidement aux essais cliniques pour l’Alzheimer. Mais les méthodes informatiques modernes qui explorent les bases de données biologiques et la littérature médicale génèrent aujourd’hui d’immenses listes de candidats — bien plus que ce que les chercheurs peuvent raisonnablement évaluer manuellement — créant ainsi un nouvel goulot d’étranglement dans le processus.
Conjuguer plusieurs modèles intelligents
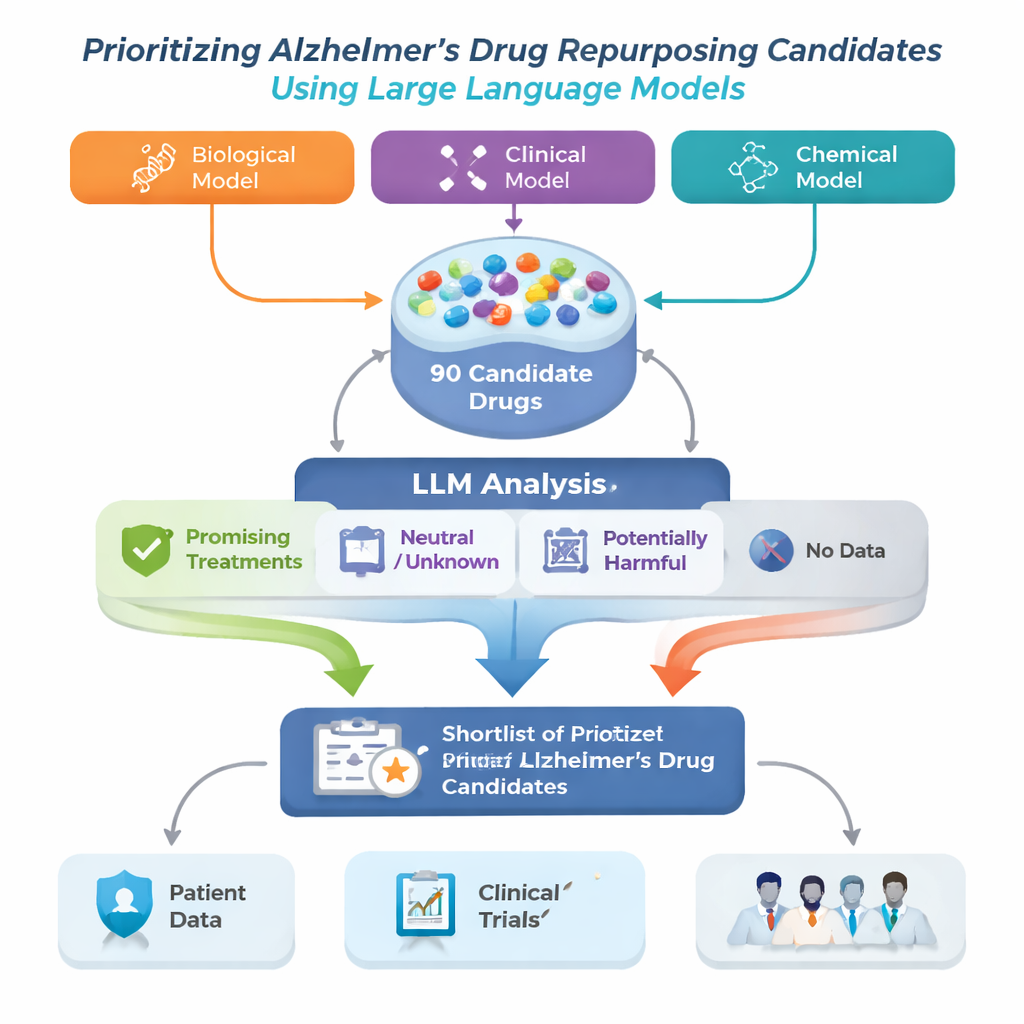
L’équipe de recherche a abordé ce problème en construisant un cadre de repositionnement de médicaments pour l’Alzheimer qui démarre avec trois modèles informatiques avancés différents. Chaque modèle examine une grande « carte » biomédicale appelée graphe de connaissances, qui relie maladies, médicaments, gènes et autres concepts médicaux, et suggère des médicaments susceptibles d’aider contre l’Alzheimer. Parce que chaque modèle perçoit les motifs différemment, leurs listes ne se recoupent pas entièrement. Les auteurs ont combiné les 30 meilleures suggestions de chaque modèle en un seul pool de 90 médicaments candidats, puis ont utilisé un grand modèle de langage (LLM) pour jouer le rôle d’un relecteur automatisé mais prudent, lisant les études publiées pour chaque médicament et jugeant si les preuves semblaient utiles, neutres ou nuisibles pour l’Alzheimer.
Comment l’IA lit la littérature médicale
Pour chaque médicament candidat, le système a extrait jusqu’à 200 résumés scientifiques depuis PubMed, ainsi que des descriptions détaillées des médicaments issues d’une base de données pharmaceutique. Le LLM a reçu pour consigne de fonder son jugement uniquement sur le texte qui lui était présenté, et d’étiqueter chaque résumé comme positif, neutre ou négatif pour le traitement de l’Alzheimer. Ces étiquettes ont ensuite été transformées en scores simples : la part des résumés classés positifs, neutres ou négatifs. En appliquant deux jeux de règles — l’un plus strict exigeant une preuve positive claire, l’autre plus indulgent signalant toute indication d’un bénéfice — le cadre a trié les médicaments en quatre groupes : traitements prometteurs, potentiellement nocifs, indéterminés ou neutres, et médicaments sans aucun article lié à l’Alzheimer. Ce dernier groupe, bien que peu étudié, peut receler des opportunités particulièrement novatrices.
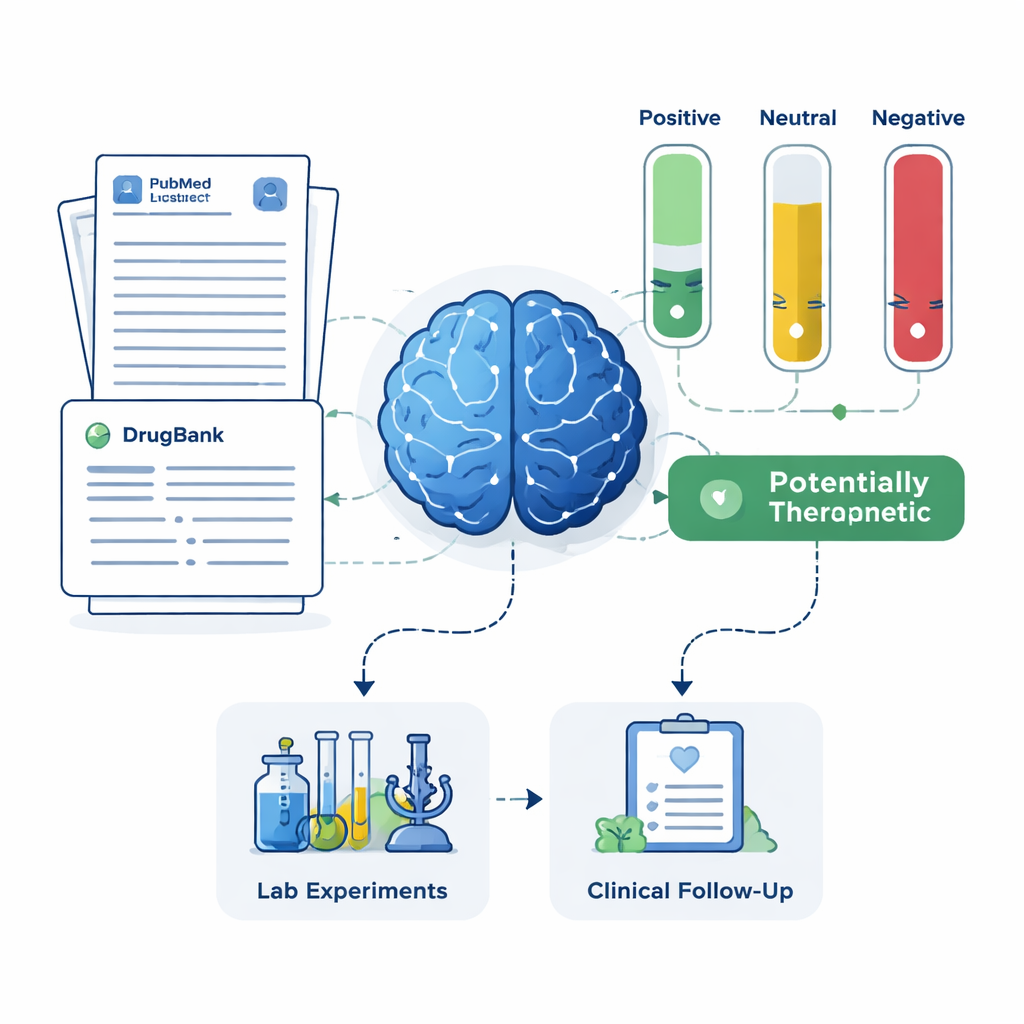
Vérification auprès de patients réels et d’essais cliniques
Pour savoir si la courte liste générée par l’IA avait du sens dans le monde réel, l’équipe a comparé ses résultats avec deux sources indépendantes : un grand registre de patients atteints d’Alzheimer et les dossiers d’essais cliniques enregistrés. Le cadre a retrouvé avec succès la mémantine, un médicament existant contre l’Alzheimer présentant des signaux protecteurs forts dans les données patient et une ample histoire d’essais, comme un candidat à haute priorité. Il a également mis en évidence des médicaments tels que le magnésium, la minocycline, la pimavanserine, la testostérone et la doxycycline, qui disposent de niveaux variables de preuves mais avaient été jugés prometteurs par des cliniciens experts. En parallèle, le système a identifié des médicaments dont la littérature suggérait un possible effet nocif ou un manque d’efficacité, recommandant de les déprioriser ou d’examiner leurs effets secondaires plutôt que de les considérer comme traitements.
Des prédictions informatiques aux étapes pratiques suivantes
Concrètement, ce cadre agit comme un assistant de recherche ultra‑rapide et minutieux qui lit des milliers d’articles, recoupe les motifs dans de larges bases de données médicales et remet aux experts humains une liste beaucoup plus courte et mieux organisée de candidats-médicaments pour l’Alzheimer sur lesquels se concentrer. L’étude montre qu’en combinant différents types d’IA — des modèles basés sur des graphes pour générer des idées et un modèle de langage pour juger les preuves — les chercheurs peuvent plus rapidement identifier à la fois des médicaments bien étayés et des options nouvelles et intrigantes à tester. Si cette approche ne guérit pas l’Alzheimer à elle seule, elle offre une nouvelle voie puissante pour relier les idées générées par ordinateur au travail concret des expériences en laboratoire et des essais cliniques, accélérant potentiellement le chemin vers des traitements plus efficaces.
Citation: Li, M., Niu, S., Xu, Y. et al. Bridging the computational-experimental gap: leveraging large language model to prioritize Alzheimer’s therapeutics based on comparison of learning models. npj Health Syst. 3, 20 (2026). https://doi.org/10.1038/s44401-026-00074-3
Mots-clés: maladie d’Alzheimer, repositionnement de médicaments, intelligence artificielle, grands modèles de langage, graphes de connaissances