Clear Sky Science · fr
La mutation APP E590D augmente la production de peptides Aβ et Aη et aggrave la tauopathie
Pourquoi cette mutation rare compte
La maladie d’Alzheimer est généralement vue comme l’accumulation lente de deux protéines nuisibles, l’amyloïde et la tau, dans le cerveau. La plupart des personnes développent la maladie sans cause unique claire, mais quelques familles portent des variants génétiques rares qui peuvent faire pencher la balance de façon spectaculaire. Cet article examine l’un de ces changements peu fréquents dans le gène de la protéine précurseur amyloïde (APP) et montre comment il peut suractiver la production de fragments protéiques toxiques et aggraver le processus d’entrelacement connu sous le nom de tauopathie. Comprendre ce cas rare fournit des indices qui peuvent s’appliquer beaucoup plus largement à la façon dont la maladie d’Alzheimer débute puis s’accélère.
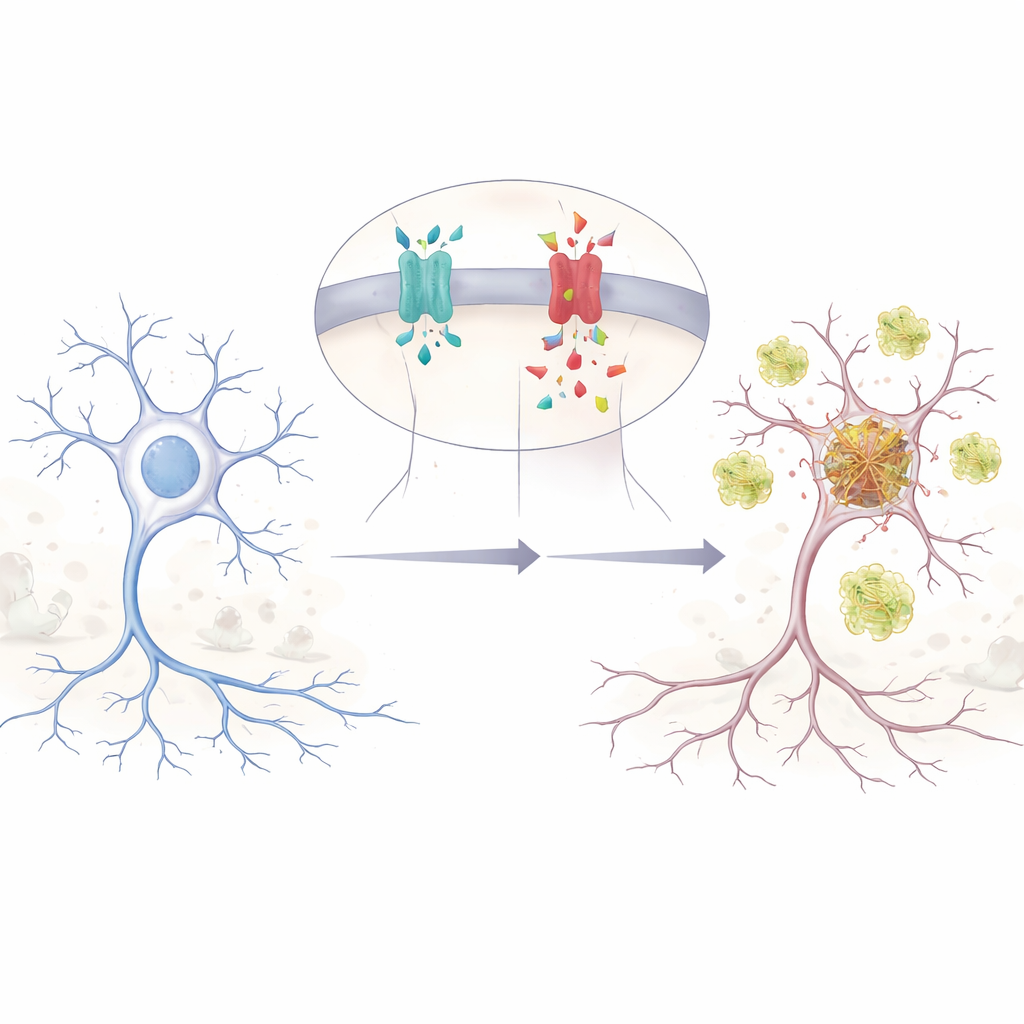
Un petit changement génétique aux grands effets
Les auteurs se concentrent sur un changement d’une seule lettre dans le gène APP, appelé E590D dans la forme principale d’APP présente dans le cerveau. Cette mutation n’a été signalée que chez deux personnes, toutes deux atteintes de la maladie d’Alzheimer à un âge relativement jeune et présentant des troubles mnésiques et comportementaux très précoces et inhabituels. Parce qu’elle est si rare, les chercheurs ne savaient pas si elle était véritablement causale ou simplement un témoin innocent. Pour en avoir le cœur net, l’équipe a recréé la mutation dans des cellules humaines et dans des neurones de souris, puis a suivi la façon dont APP était découpée en ses nombreux fragments. Ils ont découvert que l’APP mutante produit beaucoup plus de bêta-amyloïde (Aβ), le peptide adhésif longtemps associé à Alzheimer, que l’APP normale lorsque les niveaux sont comparés équitablement.
Deux peptides toxiques au lieu d’un
APP peut être clivée de plusieurs façons, comme une bûche qu’on tranche à différents endroits. La voie classique de l’Alzheimer génère Aβ, mais une autre coupure produit un fragment moins connu appelé Aη. Des travaux antérieurs ont montré que Aη peut endommager les connexions entre les cellules nerveuses et affaiblir la capacité du cerveau à renforcer les souvenirs. Dans leurs expériences, les chercheurs ont constaté que la mutation E590D n’augmente pas seulement Aβ ; elle accroît également fortement Aη et un fragment en amont qui alimente les deux voies. Cela signifie que la mutation oriente le traitement d’APP vers un double effet de peptides nocifs, perturbant potentiellement les circuits cérébraux avant même que de véritables plaques amyloïdes classiques ne soient attendues.
Comment la mutation accélère le trafic cellulaire
Pour comprendre pourquoi davantage de fragments toxiques sont produits, l’équipe a étudié où APP se situe et se déplace à la surface cellulaire. De nombreuses coupures qui créent Aβ n’ont lieu qu’après qu’APP a été internalisée par la cellule via un processus appelé endocytose. À l’aide d’imagerie et d’astuces biochimiques qui marquent les protéines à la surface puis suivent leur internalisation, les scientifiques ont montré que l’APP mutante est moins abondante à l’extérieur des cellules et est internalisée plus rapidement dans des compartiments internes que l’APP normale. Une fois à l’intérieur de ces endosomes précoces, APP rencontre les enzymes qui génèrent Aβ, et le trafic altéré semble donner à ces enzymes davantage d’occasions d’agir. Parallèlement, la coupure au site η à la surface est également augmentée, ce qui explique la hausse d’Aη.
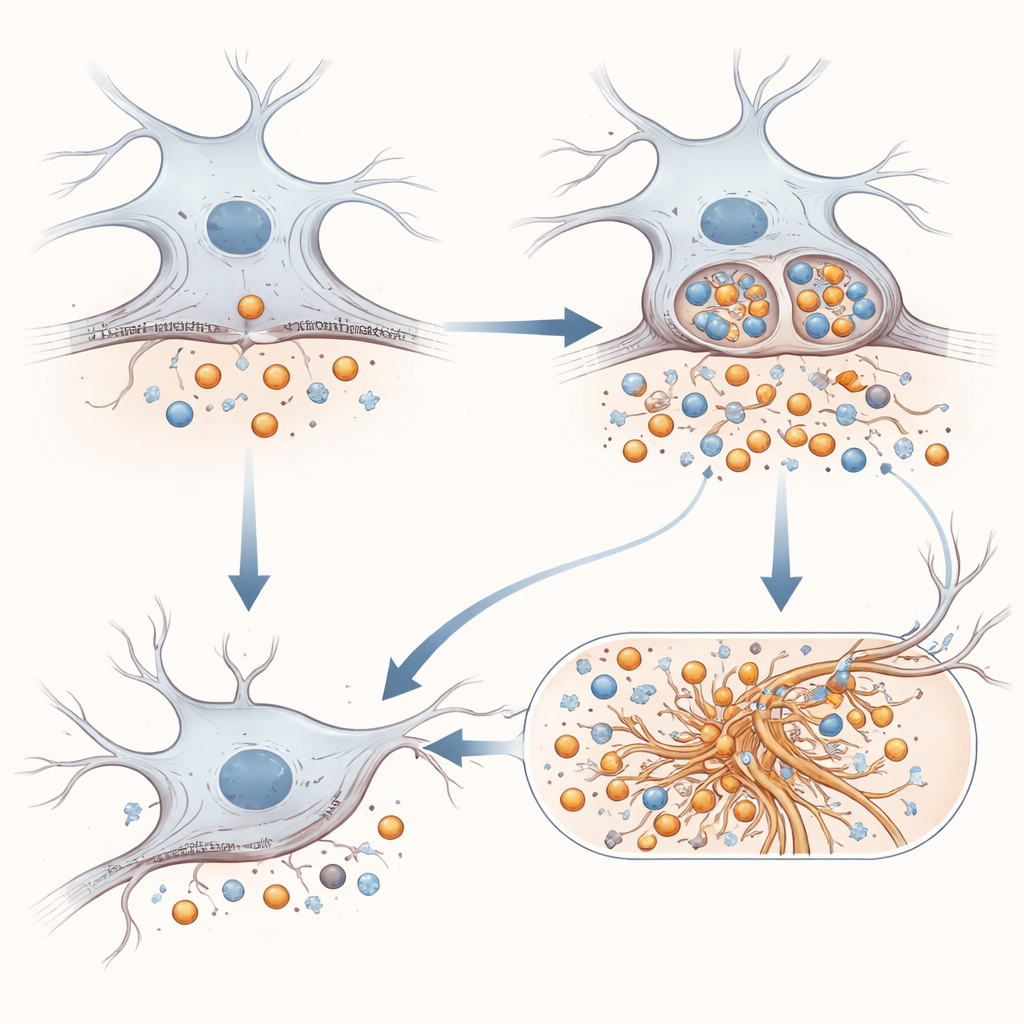
Des fragments protéiques aux enchevêtrements de tau et à l’inflammation cérébrale
L’histoire ne s’arrête pas aux fragments liés à l’amyloïde. Les chercheurs ont testé si l’APP mutante influencerait la tau, la protéine structurelle qui forme des fibres torsadées dans de nombreuses démences. Dans des modèles cellulaires qui s’allument lorsque des graines de tau provoquent la formation de nouvelles agglomérations de tau, la présence d’APP E590D a conduit à une agrégation plus marquée que l’APP normale ou l’absence d’APP. Dans un modèle murin déjà prédisposé aux problèmes de tau, l’injection d’un virus produisant l’APP mutante dans l’hippocampe a aggravé les enchevêtrements de tau et déclenché une activation plus forte des astrocytes et des microglies, les cellules de soutien et immunitaires du cerveau. Fait intéressant, les fragments amyloïdes solubles standard étaient difficiles à détecter dans ces cerveaux de souris, mais un fragment distinct dérivé d’APP est apparu uniquement en présence de la mutation, suggérant un traitement altéré dans le tissu vivant.
Ce que cela signifie pour la compréhension d’Alzheimer
En synthèse, les résultats montrent que cette mutation rare d’APP n’est pas bénigne. Elle pousse APP à générer plus d’un peptide toxique, accélère les étapes d’internalisation qui favorisent les coupures dommageables et amplifie l’entrelacement de la tau ainsi que l’inflammation cérébrale. Pour les non-spécialistes, le message clé est que la biologie d’Alzheimer n’est pas portée par un seul coupable mais par un réseau de fragments protéiques et de réponses cellulaires interconnectés. L’étude de tels variants génétiques puissants mais inhabituels offre une vue amplifiée de ce réseau. Dans ce cas, cela suggère que les thérapies pourraient devoir prendre en compte à la fois l’amyloïde et d’autres peptides dérivés d’APP comme Aη, ainsi que leur impact combiné sur la tau, plutôt que de cibler une voie isolée.
Citation: Liu, T., Wetzel, L., Roy, D. et al. APP E590D mutation increases generation of Aβ and Aη peptides and exacerbates tauopathy. npj Dement. 2, 21 (2026). https://doi.org/10.1038/s44400-026-00069-9
Mots-clés: Maladie d’Alzheimer, protéine précurseur amyloïde, enchevêtrements de tau, neuroinflammation, mutation génétique