Clear Sky Science · fr
Une plateforme quantitative à haut débit utilisant des organoïdes cérébraux humains dissociés en 2D pour modéliser la neuroinflammation dans la maladie d’Alzheimer
Pourquoi les infections pourraient avoir un rôle dans la perte de mémoire
La maladie d’Alzheimer est généralement décrite comme une accumulation lente de protéines collantes dans le cerveau, mais des preuves croissantes suggèrent que des infections pourraient contribuer à déclencher ce processus. Cette étude explore cette hypothèse en utilisant de minuscules modèles cérébraux cultivés en laboratoire pour poser une question simple : un virus courant responsable des boutons de fièvre peut-il provoquer des changements de type Alzheimer dans des cellules cérébrales humaines, et un médicament antiviral peut-il atténuer ces changements ?
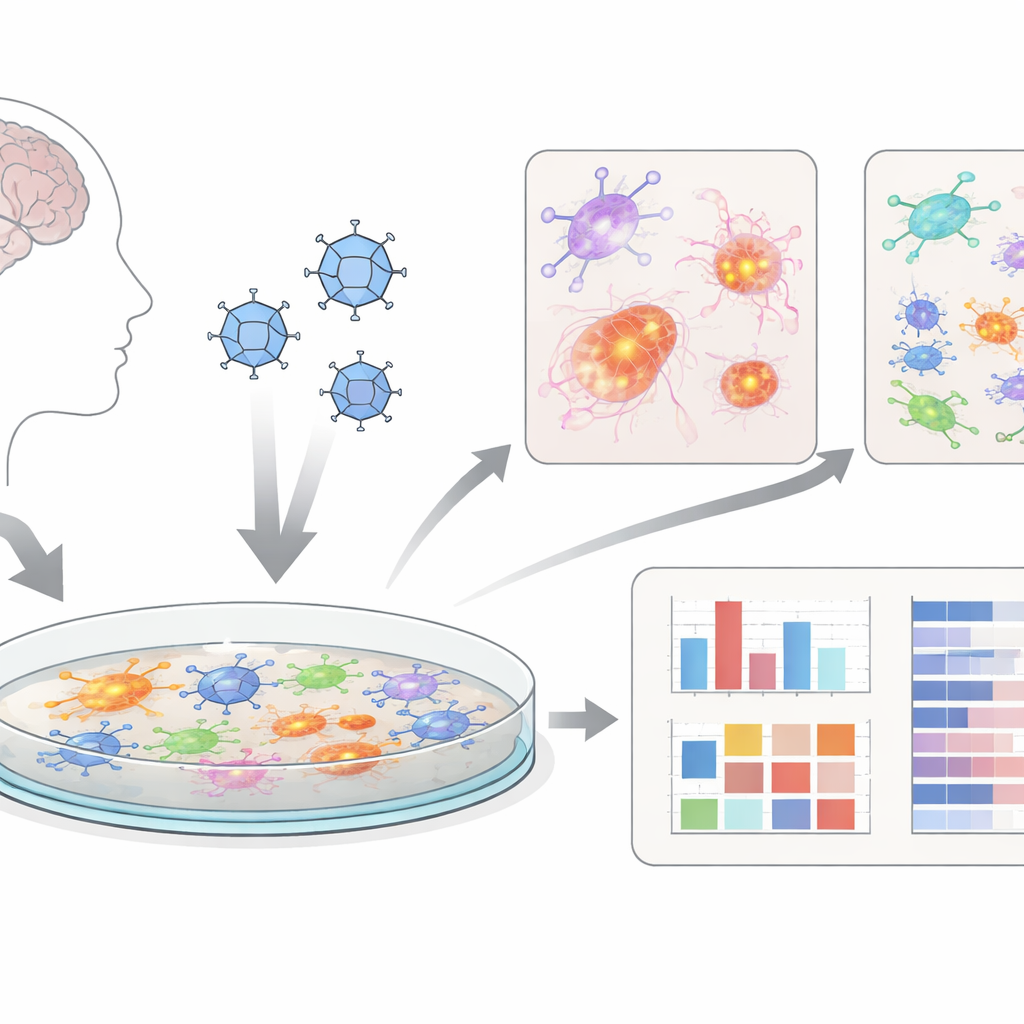
Des mini-cerveaux en culture
Plutôt que de travailler uniquement avec des animaux, les chercheurs ont utilisé des « organoïdes cérébraux » – des amas de cellules proches du cerveau cultivés à partir de cellules souches humaines. Ils ont ensuite dissocié délicatement ces organoïdes 3D en couches plates de cellules cérébrales mélangées, incluant des neurones, des cellules de soutien appelées astrocytes et des microglies de type immunitaire. Ces cultures bidimensionnelles, qu’ils appellent dcOrgs, sont plus faciles à infecter de manière homogène et à tester en haute fréquence, ce qui signifie que de nombreuses plaques et conditions médicamenteuses peuvent être examinées en parallèle. Cela rend le système attrayant comme outil de criblage pour de nouveaux traitements.
Un virus des boutons de fièvre comme étincelle
L’équipe a infecté des dcOrgs avec le virus de l’herpès simplex 1 (HSV-1), le virus responsable de la plupart des boutons de fièvre et depuis longtemps suspecté de contribuer à la démence chez certaines personnes. Ils ont comparé les cultures infectées à des contrôles simulés, à des cultures traitées par un antiviral (acyclovir), à des cultures exposées à un autre virus (influenza A) et à du virus inactivé par rayons ultraviolets. À l’aide d’analyses cellulaires automatisées et de séquençage unicellulaire, ils ont confirmé que le HSV-1 infectait fortement de nombreux types cellulaires dans la plaque, tandis que le virus inactivé et la grippe produisaient des schémas de changements très différents et plus légers.
Des changements de type Alzheimer à l’intérieur et entre les cellules
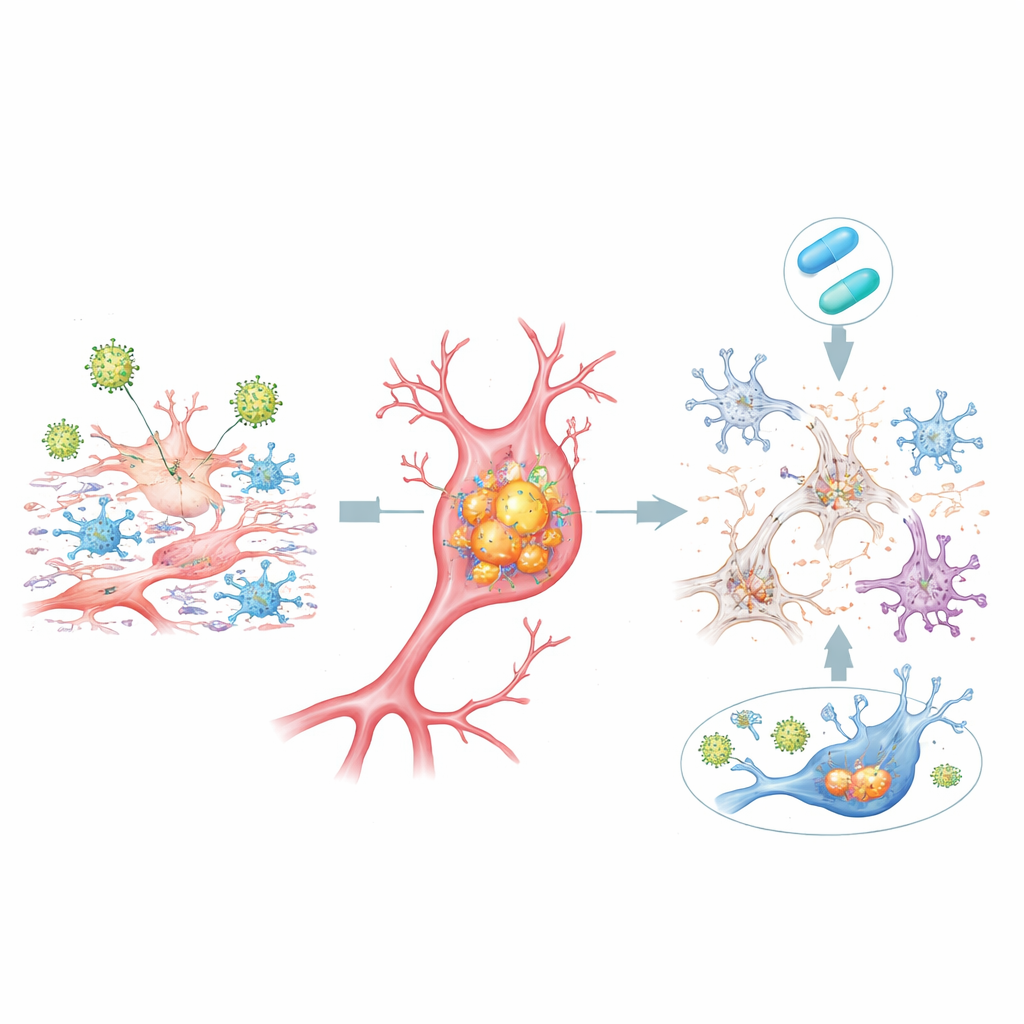
Dans les dcOrgs infectés par le HSV-1, de nombreuses cellules ont accumulé des niveaux élevés des mêmes formes protéiques observées dans les cerveaux d’Alzheimer : des amas de bêta‑amyloïde à l’intérieur des cellules et plusieurs formes « phosphorylées » de la protéine tau, autre composant clé de la maladie. Ces accumulations étaient étroitement liées aux cellules contenant des protéines virales et particulièrement prononcées dans les cellules en train de mourir. Parallèlement, moins du fragment bêta‑amyloïde plus long (Aβ42) était libéré dans le fluide environnant par rapport aux formes plus courtes, un déplacement qui reflète les profils mesurés dans le liquide céphalorachidien des patients atteints d’Alzheimer. Les populations cellulaires ont aussi changé : le nombre de neurones a diminué, tandis que les astrocytes et les microglies se sont multipliés, faisant écho à la perte neuronale et à l’inflammation réactive observées dans les tissus cérébraux des patients.
L’activité génique relie le modèle à l’Alzheimer humain
Lorsque les chercheurs ont examiné l’activité génique à l’échelle du génome, ils ont constaté que l’infection par le HSV-1 dans les dcOrgs activait et réprimait de nombreux gènes déjà liés au risque d’Alzheimer dans de grandes études génétiques humaines. Ces changements n’ont pas été observés dans des cultures plus simples de cellules souches ni dans des dcOrgs infectés par la grippe, ce qui suggère une interaction spécifique entre le HSV-1 et l’environnement cérébral mixte. Le séquençage unicellulaire a révélé que certaines des modifications des gènes associés à l’Alzheimer provenaient de cellules exposées au virus mais contenant peu ou pas de matériel génétique viral elles-mêmes, laissant entendre que des signaux émis par des voisins infectés peuvent propager des programmes inflammatoires nocifs.
Ce que le traitement antiviral peut et ne peut pas réparer
L’ajout de l’antiviral acyclovir peu après l’exposition au HSV-1 a réduit l’expression des gènes viraux, atténué de nombreuses réponses inflammatoires, diminué l’accumulation de bêta‑amyloïde et de tau toxiques à l’intérieur des cellules, et restauré partiellement l’équilibre entre les différents types cellulaires. Pour une fraction substantielle des gènes associés à l’Alzheimer, leurs niveaux d’activité sont revenus vers la normale. Cependant, tous les changements n’étaient pas réversibles : un groupe important de gènes humains est resté inchangé ou même davantage perturbé par le traitement, surtout lorsque le médicament était moins efficace pour bloquer l’expression des gènes viraux tardifs. Cela souligne que, bien qu’arrêter la réplication virale puisse aider, cela peut ne pas suffire à annuler complètement la cascade biologique une fois qu’elle est engagée.
Ce que cela signifie pour la compréhension de l’Alzheimer
Pour un non-spécialiste, la conclusion est qu’un virus humain responsable des boutons de fièvre, agissant au sein d’un mélange réaliste de cellules cérébrales humaines, peut rapidement produire de nombreux marqueurs de la maladie d’Alzheimer – des amas protéiques et des neurones mourants aux profils génétiques déjà observés chez les patients. Le système à base d’organoïdes aplatis développé ici est rapide, quantitatif et évolutif, ce qui en fait un terrain d’essai puissant pour les antiviraux et d’autres thérapies visant à calmer l’inflammation cérébrale. Bien que cela ne prouve pas que les infections à l’herpès causent l’Alzheimer chez tous les patients, cela renforce l’hypothèse que, pour une sous‑population de personnes, des infections virales chroniques ou réactivées peuvent constituer un élément important du puzzle — et une cible potentielle de prévention.
Citation: Olson, M.N., Barton, N.J., Feng, L. et al. A high-throughput, quantitative platform using 2D dissociated human cerebral organoids to model neuroinflammation in Alzheimer’s disease. npj Dement. 2, 20 (2026). https://doi.org/10.1038/s44400-026-00066-y
Mots-clés: maladie d’Alzheimer, virus de l’herpès simplex, organoïdes cérébraux, neuroinflammation, thérapie antivirale