Clear Sky Science · fr
Vieillissement de la substance blanche tout au long de la vie dans la trisomie 21 : origines développementales, progression de la maladie d’Alzheimer et implications thérapeutiques
Pourquoi cela compte pour les familles et les aidants
Les personnes atteintes de trisomie 21 vivent aujourd’hui plus longtemps que jamais, mais ce progrès bienvenue s’accompagne d’une forte augmentation des cas de maladie d’Alzheimer à des âges relativement jeunes. Cette revue explique comment le « câblage » du cerveau — appelé substance blanche — évolue depuis la période prénatale jusqu’à l’âge adulte avancé chez les personnes porteuses de trisomie 21, et comment ces modifications favorisent la perte de mémoire et les troubles cognitifs. Comprendre cette histoire du câblage ouvre de nouvelles voies pour un diagnostic plus précoce et des traitements plus ciblés.
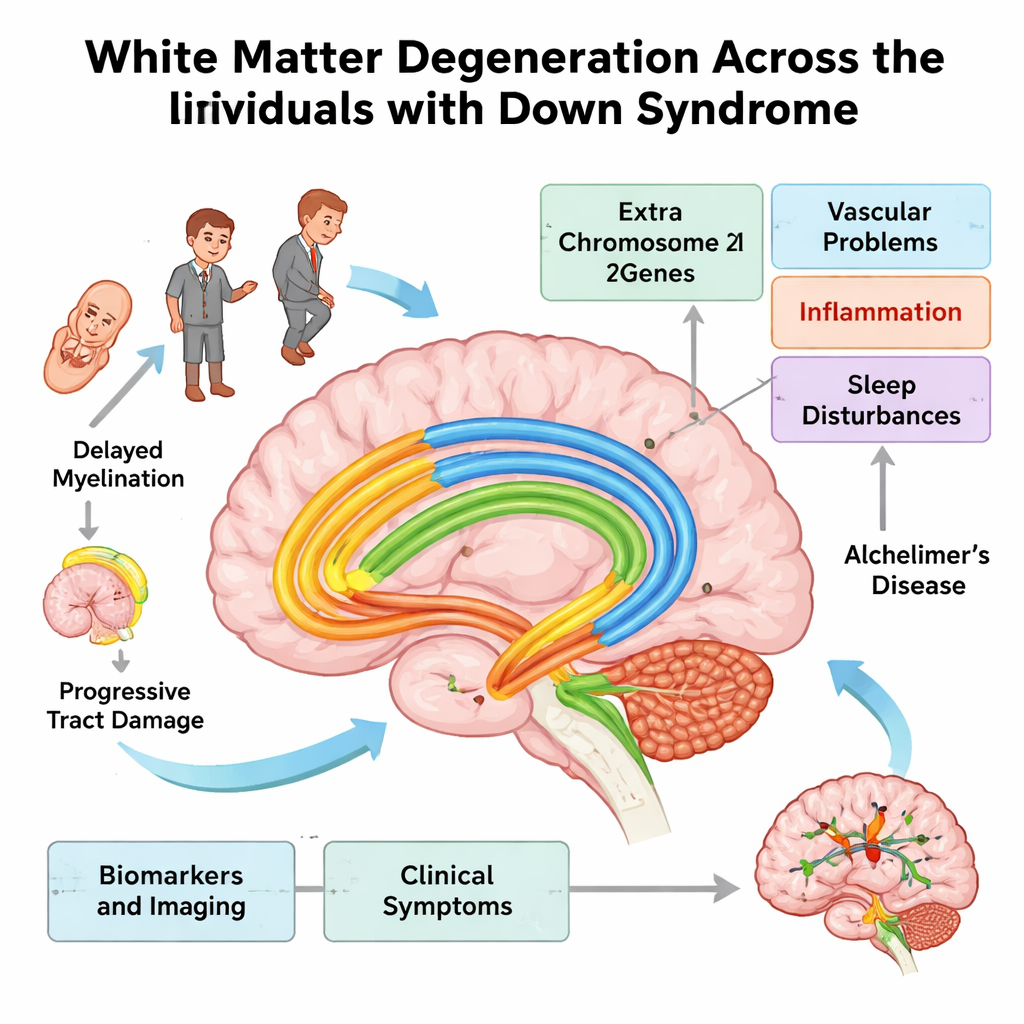
Le câblage cérébral et son influence sur la pensée
La substance blanche représente près de la moitié du cerveau humain : ce sont des fibres nerveuses groupées et isolées qui relient des régions éloignées — un peu comme des câbles Internet à haute vitesse. Ces fibres sont entourées d’une gaine lipidique appelée myéline, produite par des cellules de soutien nommées oligodendrocytes, qui permet aux signaux de circuler rapidement et efficacement. Lorsque la myéline ou les fibres sous-jacentes sont endommagées, les signaux ralentissent, les réseaux se désynchronisent et le cerveau doit fournir plus d’efforts. Les auteurs soutiennent que, dans la trisomie 21, ce câblage est vulnérable tout au long de la vie, contribuant à un traitement plus lent de l’information, à des difficultés d’apprentissage et, plus tard, à la démence.
Différences de câblage précoces qui ne se rattrapent jamais complètement
Les analyses de tissus cérébraux et les IRM pédiatriques montrent que la substance blanche se développe différemment dès le tout début chez les personnes avec trisomie 21. Les études portant sur des fœtus, des nourrissons et des enfants révèlent une myélinisation retardée et réduite, notamment dans les zones liées à la mémoire comme l’hippocampe et dans les connexions longue distance entre l’avant, les côtés et l’arrière du cerveau. Des techniques avancées d’IRM confirment que les enfants d’âge scolaire atteints de trisomie 21 présentent déjà des signes d’un câblage affaibli dans ces longues voies d’association, alors que certaines voies de passage entre les deux hémisphères paraissent étonnamment compactes et immatures. Ces différences précoces de câblage ne traduisent pas simplement des lésions tardives ; elles constituent une vulnérabilité développementale intrinsèque que le cerveau conserve à l’âge adulte.
Usure accélérée avec le vieillissement et la maladie d’Alzheimer
Avec l’âge, presque tous les adultes atteints de trisomie 21 développent des modifications cérébrales caractéristiques de la maladie d’Alzheimer — plaques amyloïdes et enchevêtrements de protéine tau — dès la cinquantaine. La revue montre que la dégénérescence de la substance blanche n’est pas uniforme ; certaines voies sont particulièrement touchées, surtout celles qui mûrissent tardivement. Il s’agit notamment des longues fibres d’association qui soutiennent la mémoire et le langage, du corps calleux qui relie les deux hémisphères, ainsi que des voies de projection et cérébelleuses qui coordonnent le mouvement. Les mesures IRM révèlent une organisation des fibres qui décline et une augmentation de la teneur en eau dans ces voies, tandis que des zones brillantes sur les scans, appelées hyperintensités de la substance blanche, souvent liées à des maladies des petits vaisseaux et à une faible perfusion, s’étendent rapidement à partir du milieu de la trentaine. Ces changements à l’imagerie suivent de près l’accumulation d’amyloïde, les marqueurs sanguins de lésion neuronale et d’inflammation, et une détérioration par paliers allant d’une cognition normale à un déclin léger puis à la démence.
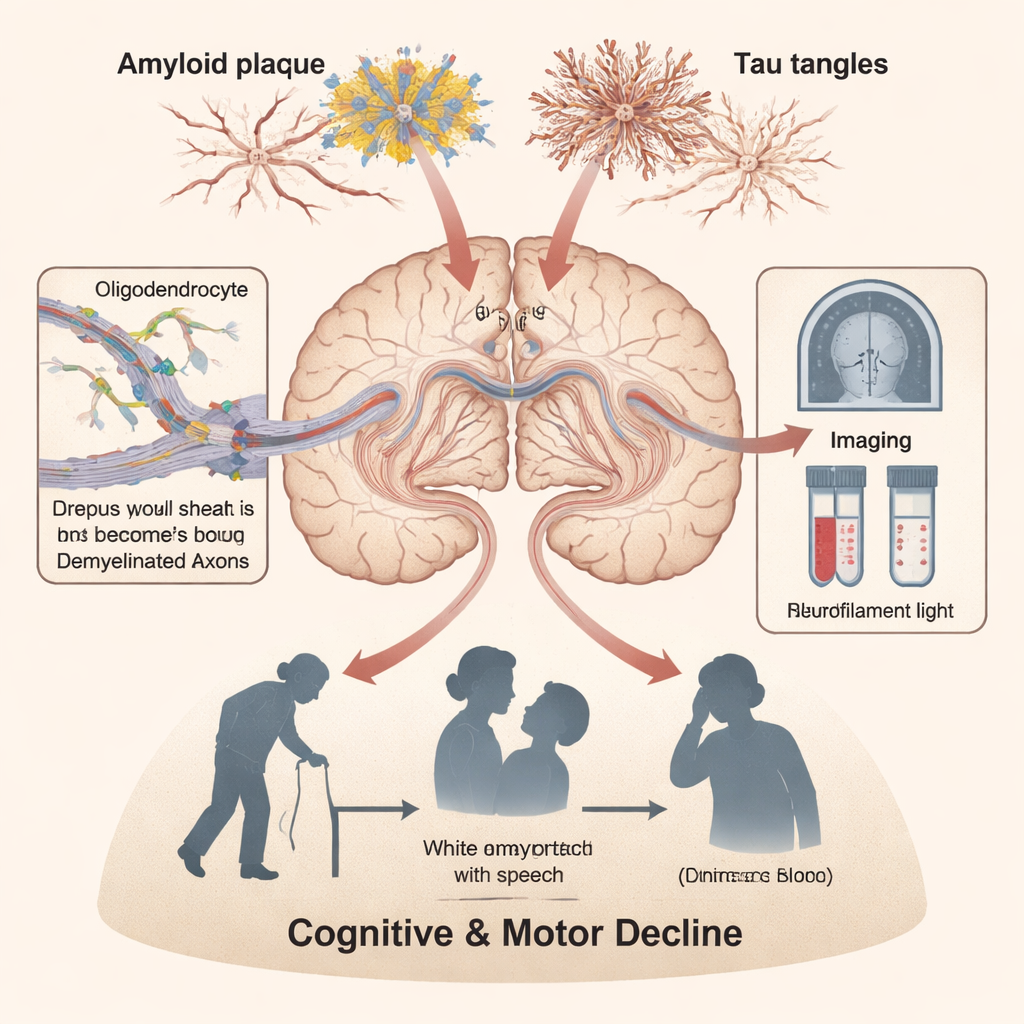
Indices cellulaires, sanguins et liés au mode de vie de l’atteinte de la substance blanche
Au niveau cellulaire, les auteurs décrivent comment la copie supplémentaire du chromosome 21 modifie des gènes clés qui régulent le développement des oligodendrocytes et la formation de la myéline. Dans les tissus cérébraux et les modèles murins, les gaines de myéline sont plus fines, moins d’axones sont correctement entourés, et les cellules progénitrices chargées de renouveler le système myélinique montrent des signes de vieillissement prématuré et de stress inflammatoire. Les analyses du sang et du liquide céphalorachidien mettent en évidence que des taux plus élevés de neurofilament léger, une protéine libérée lorsque de longues fibres nerveuses sont lésées, reflètent fortement les lésions de la substance blanche visibles en IRM. D’autres marqueurs d’amyloïde, de tau et d’activation gliale augmentent également à mesure que les hyperintensités de la substance blanche s’étendent. Des problèmes courants comme l’apnée du sommeil semblent aggraver ces dommages au câblage, en particulier dans les mêmes longues voies qui soutiennent la cognition et l’attention.
Ce que cela signifie pour le traitement et la détection précoce
Les auteurs concluent que la dégénérescence de la substance blanche est à la fois un signal d’alerte sensible et une cible thérapeutique prometteuse dans la maladie d’Alzheimer associée à la trisomie 21. Parce que les modifications du câblage apparaissent avant la perte de mémoire évidente, combiner l’imagerie cérébrale et des tests sanguins tels que le neurofilament léger peut aider à identifier les personnes à plus haut risque et à surveiller la rapidité de la progression de la maladie. Parallèlement, la biologie des oligodendrocytes, de l’inflammation, de la santé vasculaire et du sommeil offre de multiples leviers d’intervention — des médicaments favorisant la réparation de la myéline ou l’élimination des cellules sénescentes au traitement agressif des troubles respiratoires du sommeil. En protégeant le câblage du cerveau, il pourrait être possible de retarder ou d’atténuer la démence chez les personnes avec trisomie 21 et d’en tirer des enseignements plus larges applicables à la maladie d’Alzheimer dans la population générale.
Citation: Silva, J.A., Liou, JJ., Parikh, S. et al. White matter aging across the lifespan in Down syndrome: developmental origins, Alzheimer's disease progression, and therapeutic implications. npj Dement. 2, 16 (2026). https://doi.org/10.1038/s44400-026-00062-2
Mots-clés: trisomie 21, substance blanche, maladie d’Alzheimer, myéline, vieillissement cérébral