Clear Sky Science · fr
15 ans de mesures génétiques, cliniques, cognitives, d’imagerie et biochimiques longitudinales dans DIAN
Pourquoi cela compte pour les familles et l’avenir du traitement de la maladie d’Alzheimer
La plupart des gens associent la maladie d’Alzheimer à une apparition tardive dans la vie, souvent sans signes avant‑coureurs. Mais dans un petit nombre de familles, des variations génétiques héritées spécifiques rendent presque inévitable le développement précoce de la maladie. L’étude observationnelle du Dominantly Inherited Alzheimer Network (DIAN) a passé 15 ans à suivre de près ces familles à travers le monde. En observant comment la maladie se développe bien avant l’apparition des problèmes de mémoire, DIAN dévoile une chronologie détaillée des changements cérébraux qui pourrait aider les médecins à détecter, prévenir ou retarder la maladie chez beaucoup plus de personnes.
Un effort mondial suivant des familles à haut risque
DIAN suit des adultes issus de familles porteuses de mutations rares dans trois gènes liés à une forme héréditaire de la maladie d’Alzheimer. Certains participants portent la mutation, d’autres non, mais aucun n’est informé de son statut par l’étude, sauf s’il choisit un dépistage clinique séparé. Le projet a démarré en 2008 avec 10 sites dans trois pays et s’est étendu à 23 sites opérationnels dans 11 pays, travaillant en sept langues. Plus de 660 personnes se sont inscrites, et plus de 300 participent encore activement. Lors des visites régulières, les volontaires subissent des examens médicaux et cognitifs, des scanners cérébraux, des analyses de liquide céphalo‑rachidien et de sang, et, pour ceux qui y consentent, un don du cerveau après décès. Les proches non‑porteurs servent de groupe témoin exceptionnellement bien apparié, aidant les chercheurs à dissocier le vieillissement normal des changements liés à la maladie.
Voir la maladie des décennies avant les symptômes
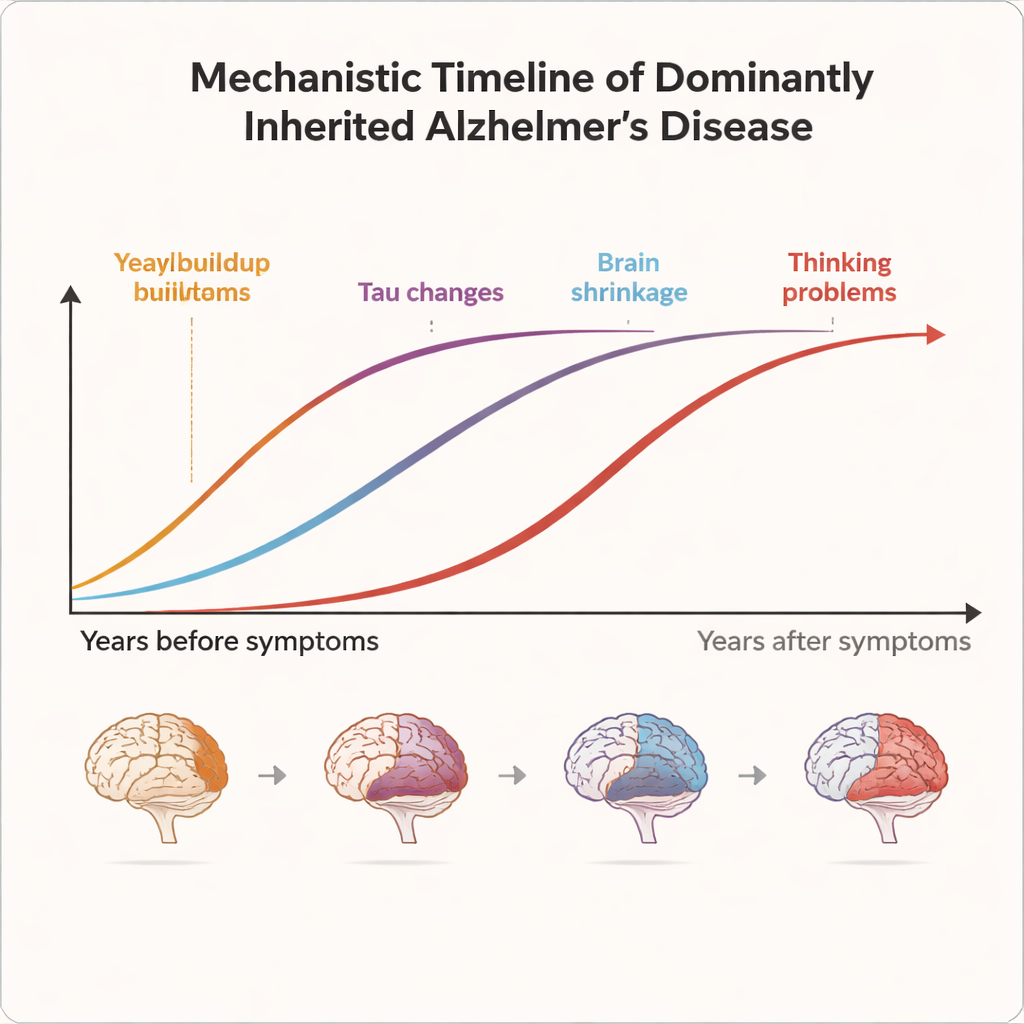
Comme l’âge d’apparition des symptômes est assez prévisible au sein de chaque famille, les chercheurs peuvent estimer combien d’années séparent chaque porteur de son onset probable. Cela leur permet d’aligner les personnes le long d’une « horloge de la maladie », depuis plus de 20 ans avant le début des troubles jusqu’à de nombreuses années après. Les résultats de DIAN montrent que la maladie d’Alzheimer n’est pas un événement soudain mais un long processus. Des agrégats protéiques collants appelés plaques amyloïdes commencent à s’accumuler dans le cerveau 15 à 20 ans avant les symptômes, visibles sur des PET scans spécialisés et corrélés à la baisse d’une forme d’amyloïde dans le liquide céphalo‑rachidien. Environ 10 à 15 ans avant l’onset attendu, d’autres signes apparaissent : des protéines tau anormales augmentent dans le liquide céphalo‑rachidien, le métabolisme cérébral ralentit et un amincissement subtil du cortex apparaît sur les IRM. Ce n’est que plusieurs années plus tard que des changements dans les fonctions cognitives et la vie quotidienne deviennent détectables par des tests cognitifs détaillés.
Une bibliothèque vivante de mesures et d’échantillons
Pour transformer ces observations en science utile à grande échelle, DIAN a constitué l’une des collections les plus riches au monde de données et de tissus liés à la maladie d’Alzheimer. Huit unités spécialisées gèrent les informations cliniques, les tests cognitifs, l’imagerie cérébrale, les biomarqueurs de fluides, la génétique, la pathologie cérébrale, la statistique et l’administration générale. Les échantillons de sang et de liquide céphalo‑rachidien sont traités dans une biobanque centrale, où des outils avancés mesurent des dizaines de protéines liées à l’amyloïde, au tau, à l’inflammation et aux lésions neuronales. Des analyses génétiques et « multi‑omiques » examinent l’ADN, l’ARN, les protéines, les lipides et d’autres molécules dans le sang, le tissu cérébral et des modèles cellulaires dérivés des participants. Un programme de neuropathologie en expansion examine soigneusement les cerveaux donnés pour confirmer les diagnostics et stadifier la maladie. Toutes ces informations sont nettoyées, contrôlées pour la qualité et consolidées en jeux de données annuels que des chercheurs extérieurs peuvent demander sous strictes garanties de confidentialité.
Alimenter les essais et les outils de nouvelle génération
DIAN n’est pas seulement une étude de l’évolution naturelle ; elle constitue aussi l’ossature d’un programme d’essais cliniques compagnon qui teste des médicaments visant à ralentir ou prévenir la maladie d’Alzheimer héréditaire. Parce que les études observationnelles et les essais thérapeutiques utilisent des procédures harmonisées, leurs résultats peuvent être combinés et comparés. La chronologie détaillée des changements cérébraux établie par DIAN a déjà contribué à façonner des critères internationaux définissant biologiquement la maladie d’Alzheimer, sur la base de marqueurs d’amyloïde, de tau et de neurodégénérescence plutôt que des seuls symptômes. Pour l’avenir, le réseau s’étend aux évaluations à distance via des applications pour smartphone, des visites de santé à domicile et des dispositifs portables pour détecter très tôt les changements cognitifs et suivre le fonctionnement quotidien. Il investit également massivement dans des tests sanguins et un profilage moléculaire approfondi pour identifier de nouvelles cibles thérapeutiques et comprendre pourquoi la progression de la maladie varie d’un individu ou d’une population à l’autre.
Ce que cela signifie pour les personnes préoccupées par la maladie d’Alzheimer
L’étude DIAN démontre que, dans la maladie d’Alzheimer héréditaire, le cerveau commence à changer de nombreuses années avant la défaillance de la mémoire — et que ces modifications invisibles peuvent être mesurées dans le sang, le liquide céphalo‑rachidien et les examens d’imagerie. Bien que les mutations étudiées soient rares, le processus sous‑jacent semble très proche de celui de la forme beaucoup plus courante d’apparition tardive. Cela fait de DIAN un modèle puissant pour l’ensemble du domaine. En cartographiant étape par étape le passage d’un cerveau sain à la démence, et en partageant ses ressources soigneusement collectées dans le monde entier, DIAN aide les scientifiques à concevoir des interventions plus précoces et plus précises. Pour les familles confrontées à un risque hérité, et pour les millions de personnes touchées par la maladie d’Alzheimer au sens large, ces connaissances offrent une voie plus claire vers une détection plus précoce, un meilleur suivi et, en fin de compte, une prévention et des traitements plus efficaces.
Citation: Daniels, A.J., McDade, E., Llibre-Guerra, J.J. et al. 15 years of longitudinal genetic, clinical, cognitive, imaging, and biochemical measures in DIAN. npj Dement. 2, 13 (2026). https://doi.org/10.1038/s44400-025-00047-7
Mots-clés: maladie d’Alzheimer, démence génétique, biomarqueurs cérébraux, étude longitudinale, détection précoce