Clear Sky Science · fr
Encodage des arêtes fonctionnelles dans les graphes pour modéliser les relations spatiales variables dans le microenvironnement tumoral
Pourquoi il est important de cartographier le voisinage du cancer
Le cancer ne se développe pas en isolation. Les cellules tumorales vivent dans un voisinage animé d��cellules immunitaires, de cellules de soutien, de vaisseaux sanguins et de signaux chimiques, tous étroitement imbriqu�s dans l�espace. La façon dont ces voisins sont dispos�s et l�intensit� de leurs influences mutuelles peuvent d�terminer si une tumeur se propage, r�pond au traitement ou reste contenue. Cet article pr�sente SPIFEE, un nouveau cadre d�intelligence artificielle qui transforme des images microscopiques et des cartes mol�culaires de tumeurs en r�seaux, aidant les chercheurs �identifier quelles interactions entre cellules et voies sont le plus li�es au type de maladie et au pronostic des patients.
Transformer les tissus en carte r�seau
Les �tudes modernes sur le cancer peuvent mesurer bien plus que l�apparence d�une tumeur au microscope. Certaines m�thodes mettent en �vidence des dizaines de prot�ines sur des cellules individuelles, d�autres fournissent des lames color�es détaill�es de la structure tissulaire, et des outils plus r�cents enregistrent quelles g�nes sont actives � des milliers d�emplacements d�une coupe tumorale. SPIFEE traite toutes ces sources comme des vues diff�rentes d�un m�eme voisinage. Il repr�sente chaque �chantillon sous la forme d�un graphe : les n�uds d�efinissent des entit�s clefs du microenvironnement tumoral — tels que des types cellulaires, des motifs visuels tissulaires ou des voies mol�culaires — tandis que les ar�tes capturent comment ces entit�s interagissent dans l�espace. Crucialement, SPIFEE ne r�duit pas une interaction � un simple nombre comme la « distance ». Chaque ar�te stocke au contraire une petite courbe d�e9crivant � quelle intensit� deux entit�s se m�elent ou se repoussent sur une gamme de distances, pr�servant ainsi des d�etails spatiaux beaucoup plus riches.
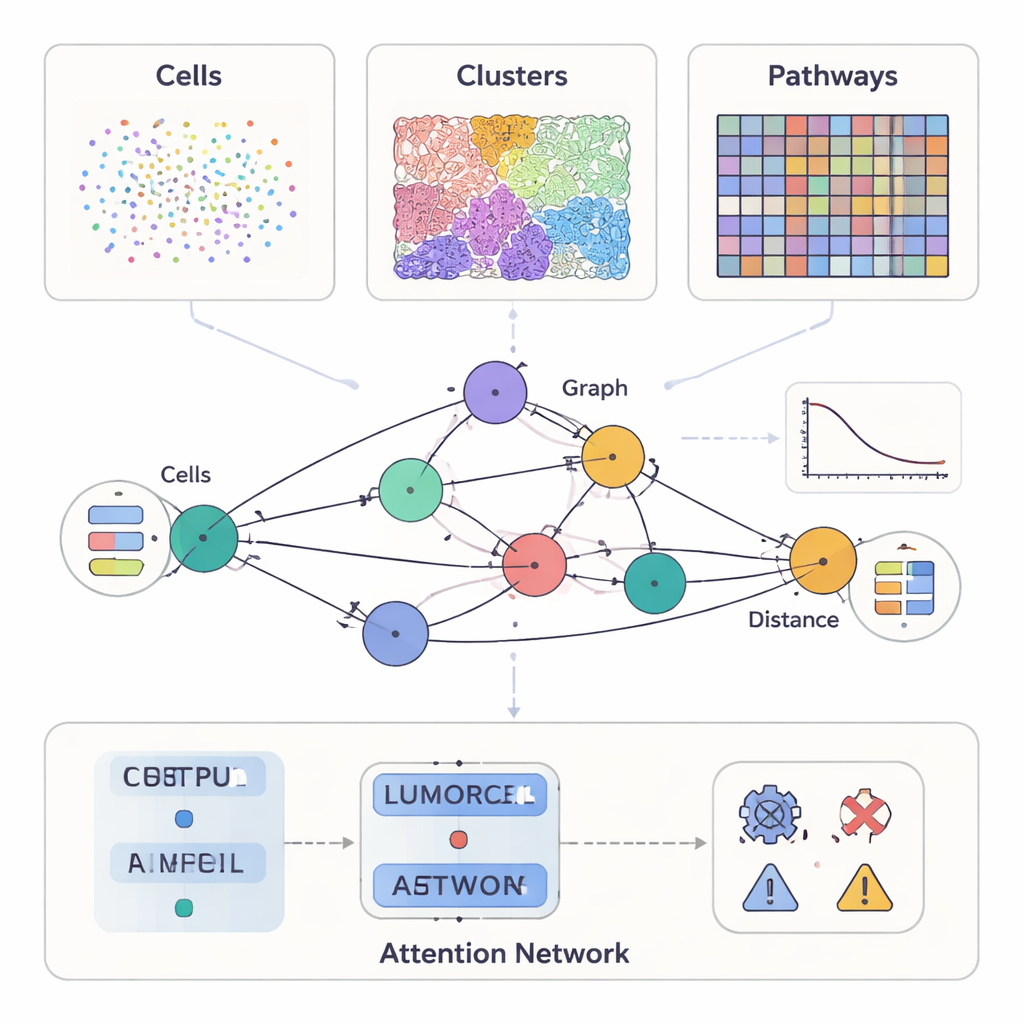
Un prisme adaptable � de nombreux types de donn�ees canc�er
Les auteurs ont test� SPIFEE sur plusieurs grandes bases de donn�ees ind�ependantes couvrant diff�rentes technologies et �chelles. Dans des �chantillons pancr�atiques marqu�s par immunofluorescence multiplex�e9e, chaque n�ud du graphe repr�sentait un type cellulaire, et les attributs des n�uds provenaient du transcriptome cellulaire unique (single-cell RNA sequencing) qui r�sumait la mani�re dont ces cellules communiquent en g�n�ral. Sur des lames de cancer du poumon color�es avec la m�thode routini�re h�matoxyline et �osin, les n�uds repr�sentaient des motifs visuels r�currents du tissu, d�couverts automatiquement par un syst�eme d�apprentissage auto-supervis�. Dans un troisi�me contexte, des lames standard de cancer du poumon ont �t� converties par un outil d�apprentissage profond en transcriptomique spatiale virtuelle, et les n�uds SPIFEE repr�sentaient des voies mol�culaires telles que l�hypoxie, l�estrog�ne ou la signalisation JAK�STAT, avec des attributs d�eriv�s de l�activit� g�n�ique. Dans tous ces contextes, le m�eme cadre pouvait ing�rer diff�rents types de n�uds tout en construisant des graphes spatiaux comparables.
Identifier les interactions qui distinguent les issues de sant�
Une fois que SPIFEE construit un graphe, il le transmet � un r�seau d�attention pour graphes, un type de r�seau neuronal qui apprend non seulement � pr�dire un r�sultat — tel que le sous-type de cancer, le risque de survie, ou la diff�renciation entre maladie et inflammation non canc�reuse — mais aussi � mettre en �vidence quelles ar�tes ont le plus compt� pour cette pr�diction. Dans le tissu pancr�atique, SPIFEE a distingu� la pancr�atite chronique de l�ad�ad�un ad�nocarcinome canalaire pancr�atique avec une pr�cision sup�rieure � des m�ethodes ant�rieures bas�es sur des graphes. Le mod�le s�est r�guli�rement focalis� sur des interactions impliquant les cellules �pith�liales (tumorales), les cellules T r�gulatrices, les cellules pr�sentatrices d�antig�ne et les cellules T auxiliaires, indiquant un voisinage immunosuppresseur plus prononc� dans le cancer que dans l�inflamation. Sur des lames d�ad�nocarcinome pulmonaire, SPIFEE a identifi� des motifs stroma-tumeur particuliers dont les interactions corr�laient avec une meilleure ou pire survie, sugg�rant que les « zones frontali�res » entre tumeur et tissu de soutien contiennent des indices pronostiques importants que les analyses standard peuvent manquer.
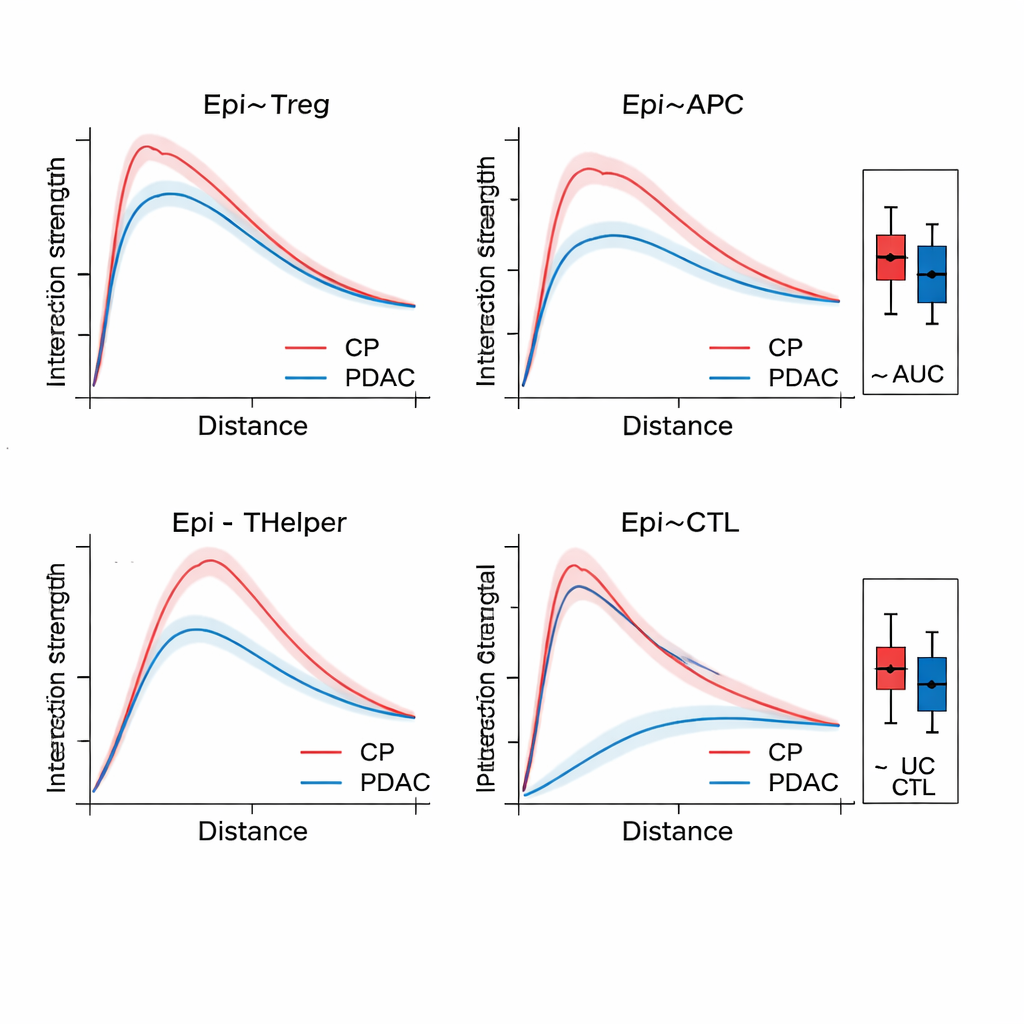
Lire les échanges mol�culaires depuis des lames routini�res
Peut-�tre de fa�on la plus frappante, SPIFEE a pu inf�rer des interactions de voies significatives � partir d�images pathologiques ordinaires une fois celles-ci traduites en cartes pr�dites d�activit� g�n�ique. En traitant les voies comme des n�uds et leur co-occurrence spatiale comme des ar�tes fonctionnelles, la m�thode a mis en avant des paires comme l�hypoxie avec EGFR ou JAK�STAT avec PI3K — des combinaisons d�j� connues pour favoriser l�esquive immunitaire et la r�sistance aux m�edicaments dans le cancer du poumon. Elle a �galement mis en �vidence des voies li�ees � l�estrog�ne dans l�ad�nocarcinome pulmonaire et certaines voies immunitaires et de stress dans les tumeurs squameuses, des constatations coh�rentes avec des sch�mas observ�s en s�equencage ARN en vrac et dans un jeu de donn�ees ind�ependant de transcriptomique spatiale r�elle. Cela sugg�re que, m�eme lorsque les mesures mol�culaires sont approxim�es, les patrons spatiaux pr�sents sur des lames routini�res portent encore des signaux exploitables sur la mani�re dont les voies cl�s interagissent dans les tumeurs vivantes.
Ce que cela signifie pour la prise en charge future du cancer
Pour un non-sp�cialiste, le message principal est que SPIFEE offre une nouvelle mani�re de lire la « vie sociale » des cellules canc�ereuses directement � partir d�images et de cartes mol�culaires. En encodant comment les relations varient avec la distance au lieu de les aplatir en scores uniques, et en utilisant des r�seaux neuronaux � base d�attention pour classer quelles interactions importent le plus, le cadre peut d�couvrir des combinaisons de cellules, de motifs tissulaires et de voies qui distinguent les types de cancer et pr�disent la survie. Bien que ces r�sultats n�ecessitent encore une validation biologique et clinique, des approches comme SPIFEE pointent vers un avenir o� routine les �chantillons tumoraux pourraient fournir non seulement des instantan�s statiques, mais des cartes dynamiques des points chauds d�interaction qui aident � guider le diagnostic, la stratification du risque et, � terme, les choix de th�rapies personnalis�es.
Citation: Tsang, A.P., Krishnan, S.N., Kulkarni, R. et al. Encoding functional edges in graphs to model spatially varying relationships in the tumor microenvironment. npj Artif. Intell. 2, 27 (2026). https://doi.org/10.1038/s44387-026-00075-5
Mots-clés: microenvironnement tumoral, transcriptomique spatiale, réseaux de neurones graphiques, pathologie du cancer, interactions cellule-cellule