Clear Sky Science · fr
Un réseau de neurones informé par le métabolisme identifie des voies influençant la puissance et la toxicité des combinaisons antimicrobiennes
Pourquoi cela compte pour la santé quotidienne
Alors que de plus en plus d’infections ne répondent plus à nos antibiotiques de référence, les médecins recourent de plus en plus à des associations de médicaments. Mais mélanger des médicaments peut être une arme à double tranchant : la bonne combinaison peut éradiquer des bactéries tenaces, tandis qu’un mauvais mélange peut endommager des organes comme les reins et le foie. Cette étude présente une approche informatique nouvelle, baptisée CALMA, conçue pour aider scientifiques et cliniciens à identifier des combinaisons à la fois efficaces contre les microbes et moins nocives pour les patients.
Combattre les microbes sans tâtonnements
Traditionnellement, découvrir de bonnes combinaisons d’antibiotiques impliquait de tester un très grand nombre de paires ou de trios de médicaments en laboratoire et chez les patients. Le nombre de mélanges possibles augmente de façon explosive à chaque médicament ajouté, ce qui rend les tests expérimentaux complets irréalistes. De plus, la plupart des outils existants se concentrent uniquement sur la puissance d’élimination des bactéries, en ignorant les dommages potentiels aux tissus humains. Les auteurs soutiennent que pour concevoir de meilleurs traitements, il faut considérer les deux aspects : l’efficacité contre les agents pathogènes et la sécurité pour les personnes.
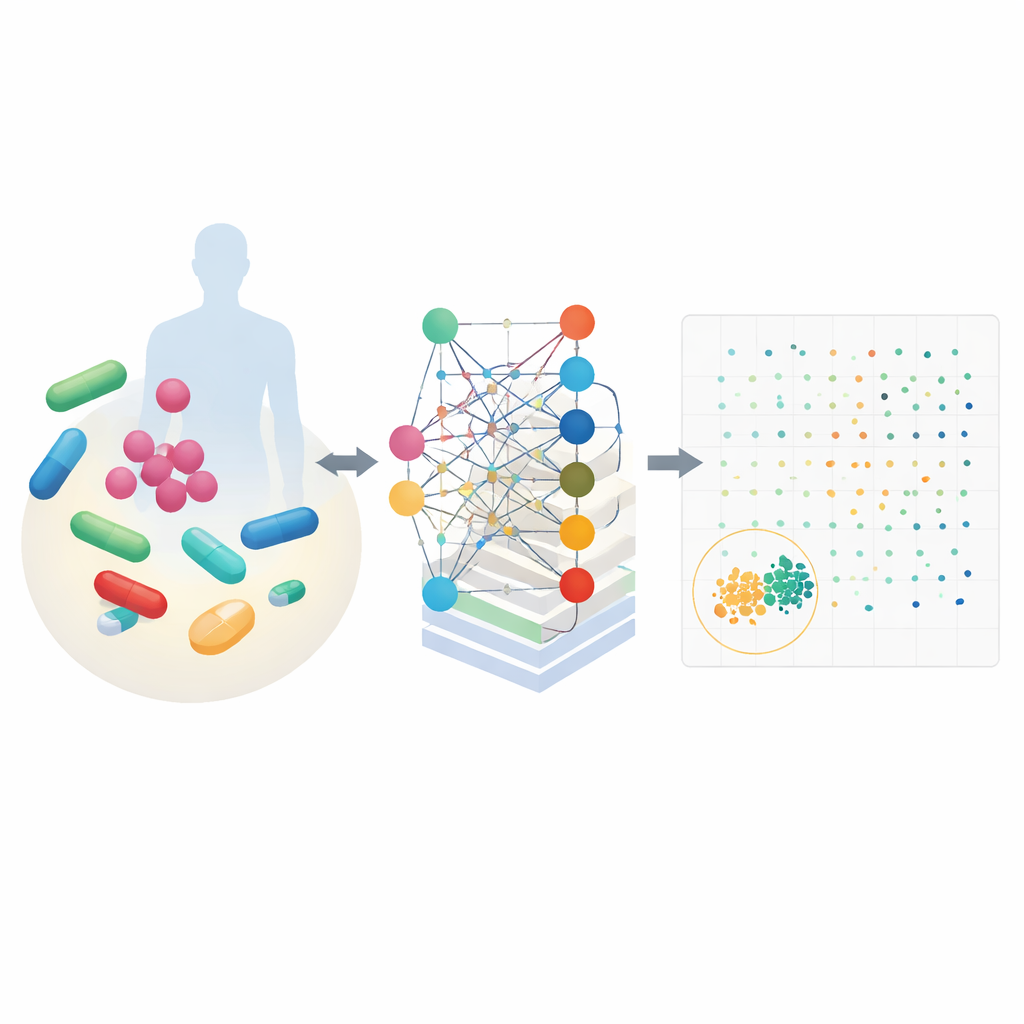
Un modèle intelligent qui comprend la chimie cellulaire
CALMA combine deux idées puissantes. D’abord, il utilise des cartes détaillées du métabolisme cellulaire qui décrivent comment les organismes transforment les nutriments en énergie et en éléments de construction. Ces cartes, établies pour des bactéries comme Escherichia coli et l’agent de la tuberculose, simulent comment des milliers de réactions chimiques évoluent en présence d’un médicament. Ensuite, CALMA alimente ces simulations dans un réseau de neurones artificiels dont la structure reflète les voies métaboliques. En regroupant l’information selon des itinéraires biologiques connus — tels que la production d’énergie ou le recyclage des nucléotides — le modèle apprend des motifs reliant des voies spécifiques soit à une mise à mort efficace des bactéries, soit à des effets secondaires nocifs pour les cellules humaines.
Cartographier le paysage des mélanges médicamenteux
En utilisant des données d’expériences antérieures et de larges bases de données de sécurité, les chercheurs ont entraîné CALMA à attribuer à chaque combinaison médicamenteuse deux scores : l’un pour son intensité d’action contre les bactéries et l’autre pour sa probabilité de toxicité chez l’humain. Tracer ces scores crée un paysage où les meilleurs candidats se situent en bas à gauche — puissants contre les microbes et doux pour les cellules humaines. Lorsqu’ils ont appliqué CALMA à 35 médicaments cliniquement pertinents, l’outil a réduit près de 600 paires possibles à un petit ensemble d’options prometteuses, réduisant l’espace de recherche expérimental d’environ 97 %. Parmi les suggestions de tête figuraient des combinaisons impliquant des antibiotiques courants tels que l’azithromycine, la vancomycine, l’isoniazide et le triméthoprime.
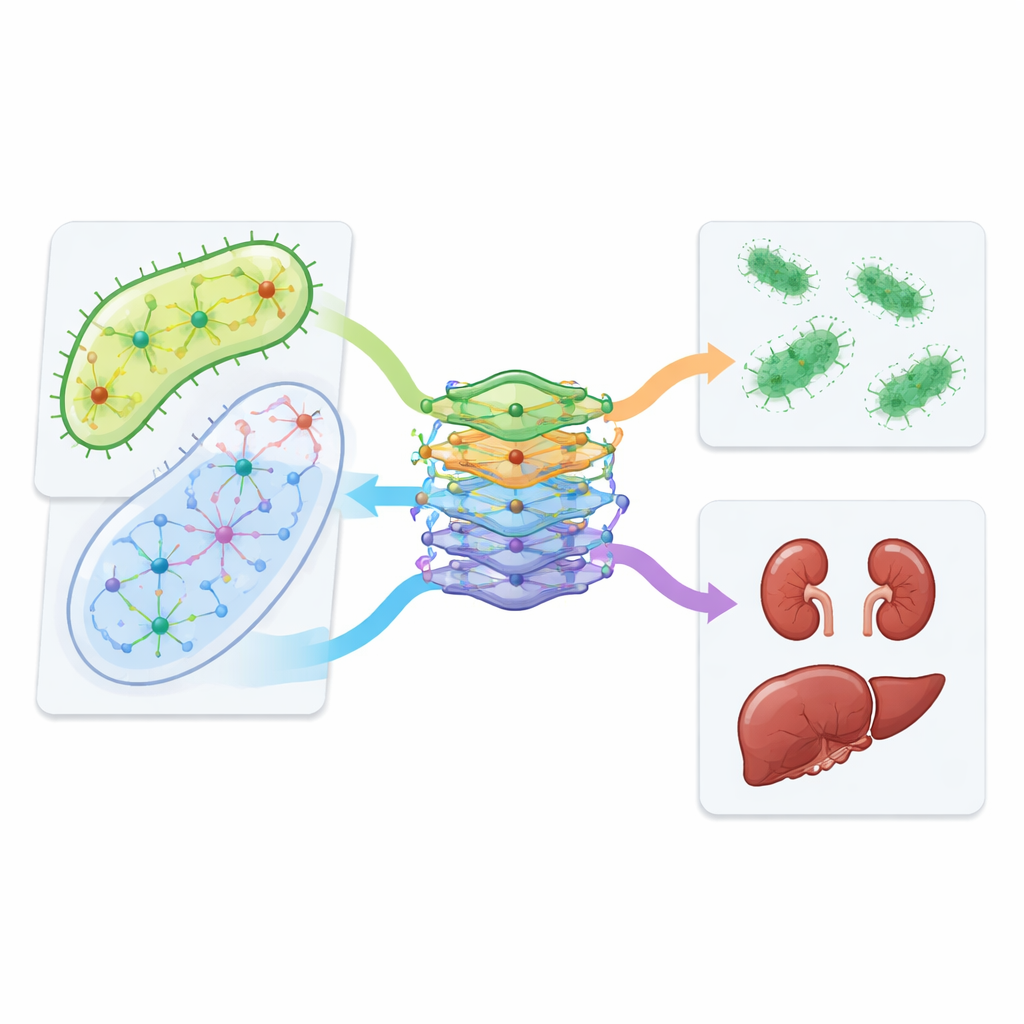
Des prédictions informatiques aux tests en laboratoire et aux patients réels
L’équipe est passée au-delà des simulations pour tester plusieurs combinaisons prédites sur des lignées cellulaires rénales et hépatiques. Ils ont constaté que certaines paires, dont azithromycine avec vancomycine et isoniazide avec triméthoprime, étaient moins toxiques pour les cellules humaines que les médicaments pris isolément, tout en conservant une activité contre E. coli. La conception de CALMA a également permis aux chercheurs d’explorer quelles voies métaboliques sous-tendent la toxicité. Une voie impliquée dans le recyclage des éléments constitutifs de l’ADN, connue sous le nom de sauvetage des nucléotides, est apparue comme un acteur clé : la modifier en expériences cellulaires changeait la nocivité de certaines combinaisons. Enfin, les auteurs ont examiné les dossiers de santé de centaines de milliers de patients et ont observé que les personnes recevant de l’azithromycine associée à la vancomycine présentaient moins de problèmes rénaux documentés que des patients comparables traités par vancomycine seule, faisant écho aux résultats en laboratoire.
Ce que cela signifie pour les traitements futurs
Pour un non-spécialiste, CALMA peut être considéré comme un filtre intelligent qui comprend suffisamment la biologie pour suggérer quelles combinaisons médicamenteuses méritent d’être testées en priorité. Plutôt que de mélanger des antibiotiques au hasard en espérant le meilleur, les chercheurs peuvent se concentrer sur des combinaisons que les modèles prédisent capables d’atteindre les points faibles bactériens tout en épargnant des voies humaines vulnérables. Bien que la méthode dépende des données disponibles et ne soit pas parfaite, elle offre une voie plus rationnelle pour concevoir des thérapies combinées. Avec le temps, des outils comme CALMA pourraient aider les médecins à traiter les infections résistantes de façon plus sûre, réduire les tâtonnements dans le développement des médicaments et même être adaptés à d’autres maladies où les associations de traitements et les effets secondaires sont des enjeux majeurs.
Citation: Arora, H.S., Lev, K., Robida, A. et al. A Metabolism-Informed Neural Network Identifies Pathways Influencing the Potency and Toxicity of Antimicrobial Combinations. npj Drug Discov. 3, 11 (2026). https://doi.org/10.1038/s44386-026-00042-9
Mots-clés: combinaisons d'antibiotiques, toxicité des médicaments, réseaux de neurones artificiels, métabolisme, résistance aux antimicrobiens