Clear Sky Science · fr
La stimulation préférentielle de HER4 préserve l’amélioration de la fonction myocardique induite par la néureguline
Un nouvel espoir pour les cœurs défaillants
L’insuffisance cardiaque touche des millions de personnes dans le monde et s’aggrave souvent malgré les meilleurs traitements actuels. Cette étude explore un nouveau type de médicament biologique, appelé JK07, conçu pour aider le cœur à se réparer tout en évitant une inquiétude majeure : l’activation accidentelle de cancers latents. En modulant un signal naturel de réparation cardiaque et en l’éloignant des voies liées au cancer, les chercheurs cherchent à délivrer le bénéfice sans le risque.
Comment fonctionne le signal réparateur du cœur
Le travail se concentre sur la néureguline‑1 (NRG‑1), une protéine produite par notre organisme qui aide les cellules du muscle cardiaque à croître, survivre et récupérer après une lésion. La NRG‑1 transmet ses instructions via des points d’ancrage cellulaires appelés HER3 et HER4. Lorsque la NRG‑1 se fixe à ces récepteurs, ils s’associent avec un partenaire nommé HER2 et déclenchent des signaux intracellulaires de survie et de réparation. Des études antérieures chez l’animal et l’humain utilisant de la NRG‑1 recombinante ont montré des améliorations significatives de la force de contraction cardiaque, mais elles ont aussi entraîné des effets indésirables comme des troubles digestifs et des atteintes hépatiques. Plus préoccupant encore, on sait que HER3 stimule la croissance de nombreux cancers, ce qui laisse craindre qu’un traitement prolongé par NRG‑1 puisse réveiller des tumeurs silencieuses.
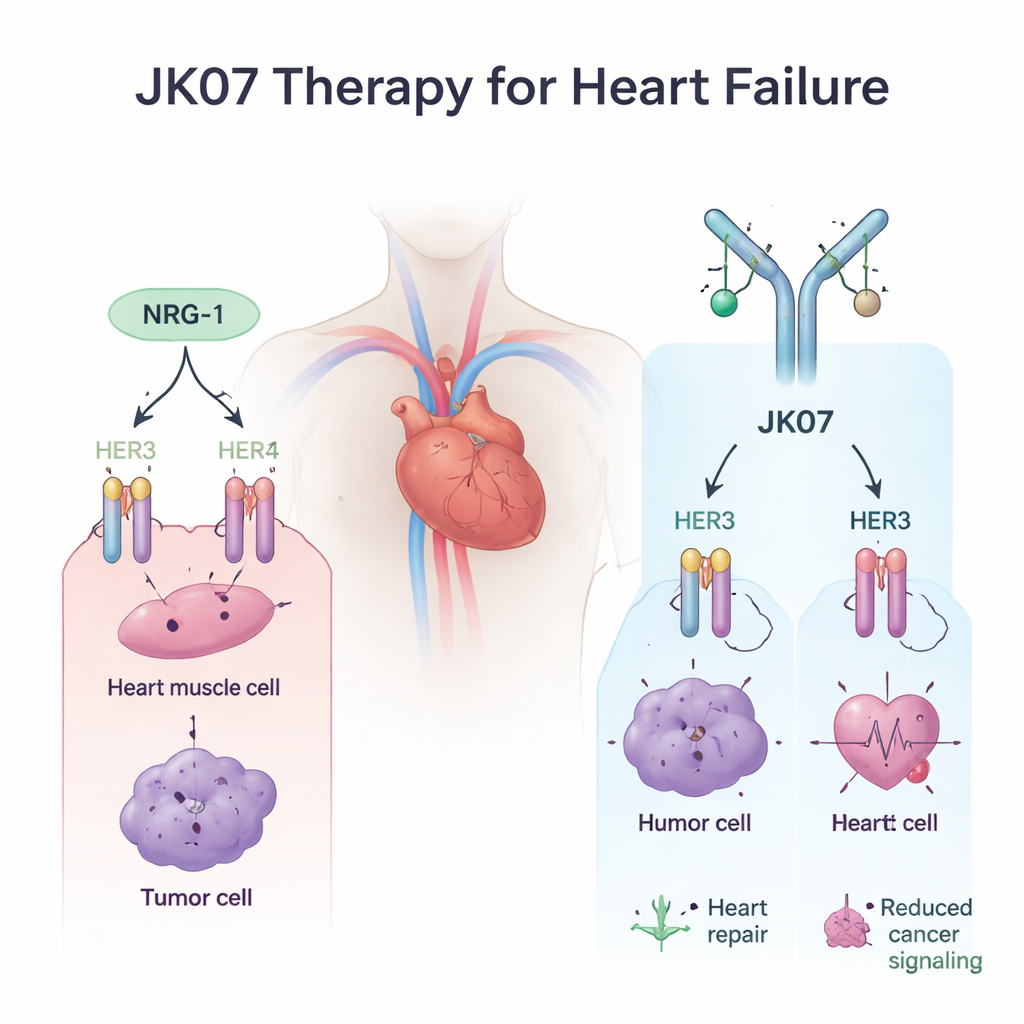
Une molécule de synthèse avec un dispositif de sécurité
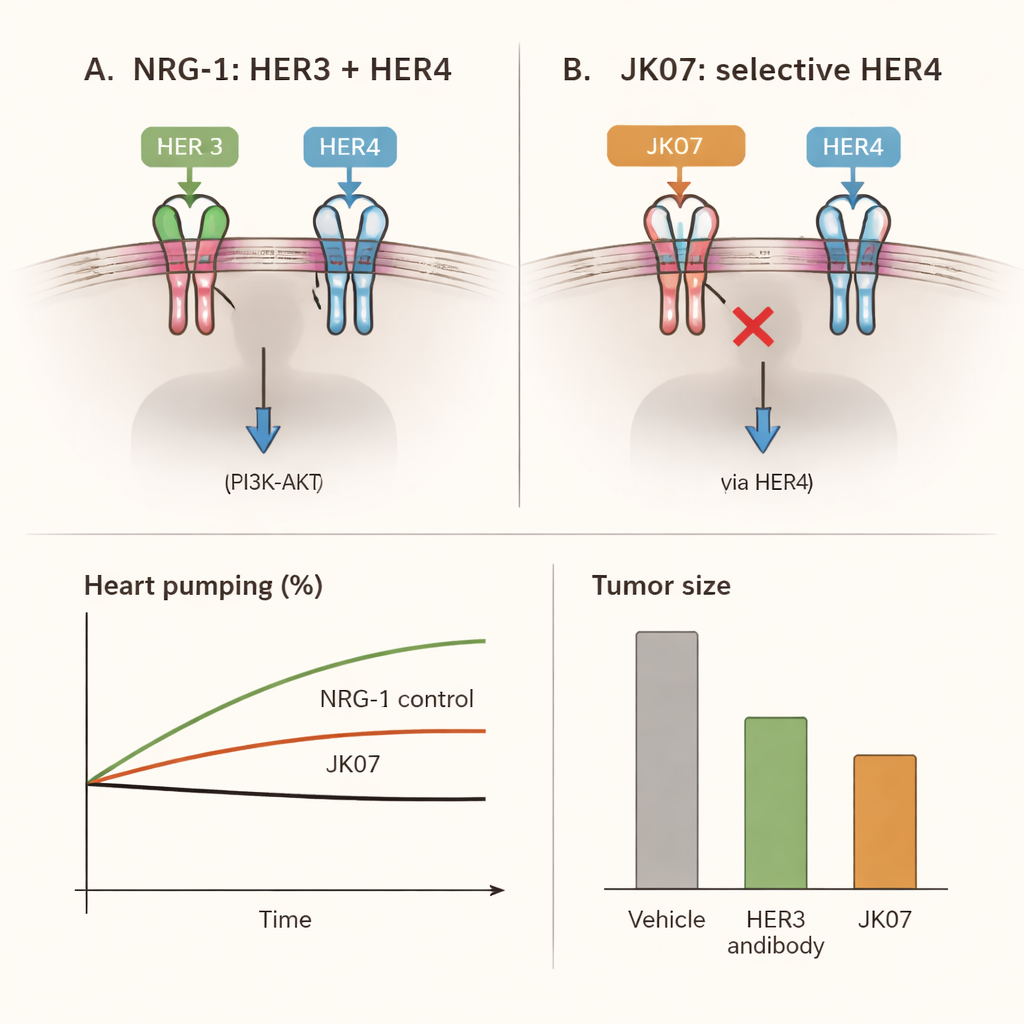
Pour résoudre ce problème, les scientifiques ont conçu JK07, une molécule de fusion composée de deux éléments soigneusement choisis. Une extrémité est un anticorps entièrement humain conçu pour bloquer HER3, le récepteur lié au cancer. L’autre extrémité est le fragment actif de la NRG‑1 qui déclenche les signaux bénéfiques, attaché en double de sorte qu’il puisse toujours atteindre les cellules cardiaques. Dans des expériences in vitro, JK07 se liait fermement à HER3 tout en maintenant le fragment de NRG‑1 correctement replié et actif. Dans des modèles cellulaires de cancer dépendants de HER3, JK07 a fortement réduit les signaux nécessitant HER3, ralenti la croissance cellulaire par rapport à la NRG‑1 seule, et chez des souris porteuses de tumeurs pilotées par HER3 il a réduit la taille des tumeurs de manière dépendante de la dose. Ces résultats montrent que la portion anticorps agit effectivement comme un verrou de sécurité sur HER3.
Préserver le signal bénéfique pour le cœur
De manière cruciale, JK07 devait conserver les effets bénéfiques via HER4, le récepteur principalement associé à la réparation cardiaque plutôt qu’au cancer. En utilisant des lignées cellulaires spécialisées et des cardiomyocytes dérivés de cellules souches humaines, l’équipe a montré que JK07 favorisait l’hétérodimérisation de HER4 avec HER2 et activait une voie protectrice clé à l’intérieur des cellules cardiaques, connue sous le nom d’AKT, aussi fortement que la NRG‑1 non modifiée. Les cellules cardiaques de rat ont réagi de la même façon. En d’autres termes, JK07 n’affaiblissait pas le signal de secours du cœur ; il le redirigeait simplement loin de HER3 et vers HER4.
Des rongeurs aux singes : l’effet de JK07 sur le cœur
Les chercheurs ont ensuite vérifié si ce signal sélectif pouvait réellement sauver des cœurs en insuffisance. Chez des rats ayant subi un infarctus induit chirurgicalement, la capacité de pompage cardiaque chutait d’environ un tiers, reproduisant fidèlement l’insuffisance cardiaque humaine. Les animaux traités par JK07 à plusieurs reprises pendant quatre semaines ont montré une récupération nette : la fraction d’éjection, mesure standard du volume de sang éjecté par battement, a augmenté d’environ un tiers par rapport à l’état pré‑traitement. Les cavités cardiaques dilatées ont diminué vers une taille plus normale, le collagène lié aux cicatrices dans les zones endommagées a diminué, et la structure microscopique du muscle cardiaque est apparue plus organisée et saine. Ces améliorations étaient comparables à celles observées avec un médicament témoin à base de NRG‑1 qui ne bloque pas HER3, indiquant que HER4 seul suffit à apporter les bénéfices cardiaques.
Plus proche de la clinique : résultats chez le macaque
Pour tester JK07 dans un modèle animal plus proche de la maladie humaine, l’équipe a étudié des macaques rhésus d’âge moyen ayant développé naturellement une insuffisance cardiaque chronique, incluant les formes à fraction d’éjection réduite (HFrEF) et à fonction de remplissage altérée (HFpEF). Chez les singes présentant une diminution de la contractilité, deux études indépendantes ont montré que des perfusions hebdomadaires de JK07 ont conduit la plupart des animaux à gagner au moins cinq points de pourcentage en fraction d’éjection, certains approchant des améliorations absolues de 20 points—des résultats comparables à ceux obtenus avec le médicament établi sacubitril/valsartan. Chez les animaux dont le problème principal était le remplissage et la relaxation plutôt que la contraction, JK07 a amélioré le grade de dysfonction diastolique chez la plupart des sujets, tandis que le sacubitril/valsartan n’a aidé que rarement. Dans l’ensemble des études, aucun problème de sécurité majeur n’est apparu aux doses testées.
Ce que cela pourrait signifier pour les patients
Pour un public non spécialiste, le message essentiel est que cette étude montre qu’il pourrait être possible d’exploiter le système de réparation propre au cœur de façon plus ciblée et plus sûre. JK07 est conçu pour stimuler le récepteur « bon » (HER4) qui soutient la réparation cardiaque tout en bloquant le récepteur « risqué » (HER3) lié au cancer. Chez les rongeurs comme chez les singes, cette approche sélective a amélioré la contraction cardiaque, réduit les dommages structurels et la fibrose, et a même montré une activité anti‑tumorale dans un modèle de cancer. Bien que des essais humains restent nécessaires pour confirmer les bénéfices et la sécurité à long terme, JK07 ouvre la voie à un avenir où les traitements de l’insuffisance cardiaque seraient non seulement plus efficaces mais présenteraient aussi un risque réduit d’alimenter un cancer.
Citation: Murphy, S.L., Tang, W.H.W., Zhuang, X. et al. Preferential HER4 stimulation preserves neuregulin-induced improvement of myocardial function. npj Drug Discov. 3, 10 (2026). https://doi.org/10.1038/s44386-026-00038-5
Mots-clés: insuffisance cardiaque, néureguline-1, HER4, thérapie biologique, remodelage cardiaque