Clear Sky Science · fr
Élaboration d’un protocole pour contrer l’activation spontanée in vitro des fibroblastes intestinaux par planification expérimentale
Pourquoi il est important de garder les cellules réparatrices de l’intestin au repos
Dans les maladies intestinales chroniques comme la maladie de Crohn, le tissu cicatriciel peut progressivement rétrécir l’intestin au point que les aliments ont du mal à passer, conduisant souvent à une intervention chirurgicale. Cette cicatrisation, appelée fibrose, est provoquée par des cellules de soutien appelées fibroblastes qui deviennent hyperactives et déposent trop de tissu conjonctif. Pour comprendre ce processus et, un jour, le prévenir, les chercheurs s’appuient sur des fibroblastes cultivés en laboratoire. Mais il y a un problème : les simples boîtes en plastique utilisées dans la plupart des laboratoires poussent ces cellules à un état d’activation artificiellement élevé, ce qui complique l’étude des premières étapes qui transforment un intestin sain en intestin fibreux.
Quand la boîte de culture envoie le mauvais signal
Les auteurs ont d’abord montré à quelle vitesse les fibroblastes intestinaux s’activent sur le plastique standard de culture. En seulement 24 heures, à la fois une lignée cellulaire établie et des cellules primaires provenant de donneurs masculins et féminins sont passées d’un état calme à une forme activée, de type musculaire. Elles produisaient de fortes quantités de protéines associées à la contraction et à la cicatrisation, comme l’α-actine des muscles lisses et la protéine d’activation des fibroblastes, et ce sans aucun déclencheur inflammatoire ajouté. Cela signifie que de nombreux modèles de laboratoire existants peuvent partir d’un état qui ressemble déjà à une maladie avancée plutôt qu’aux changements précoces et réversibles.
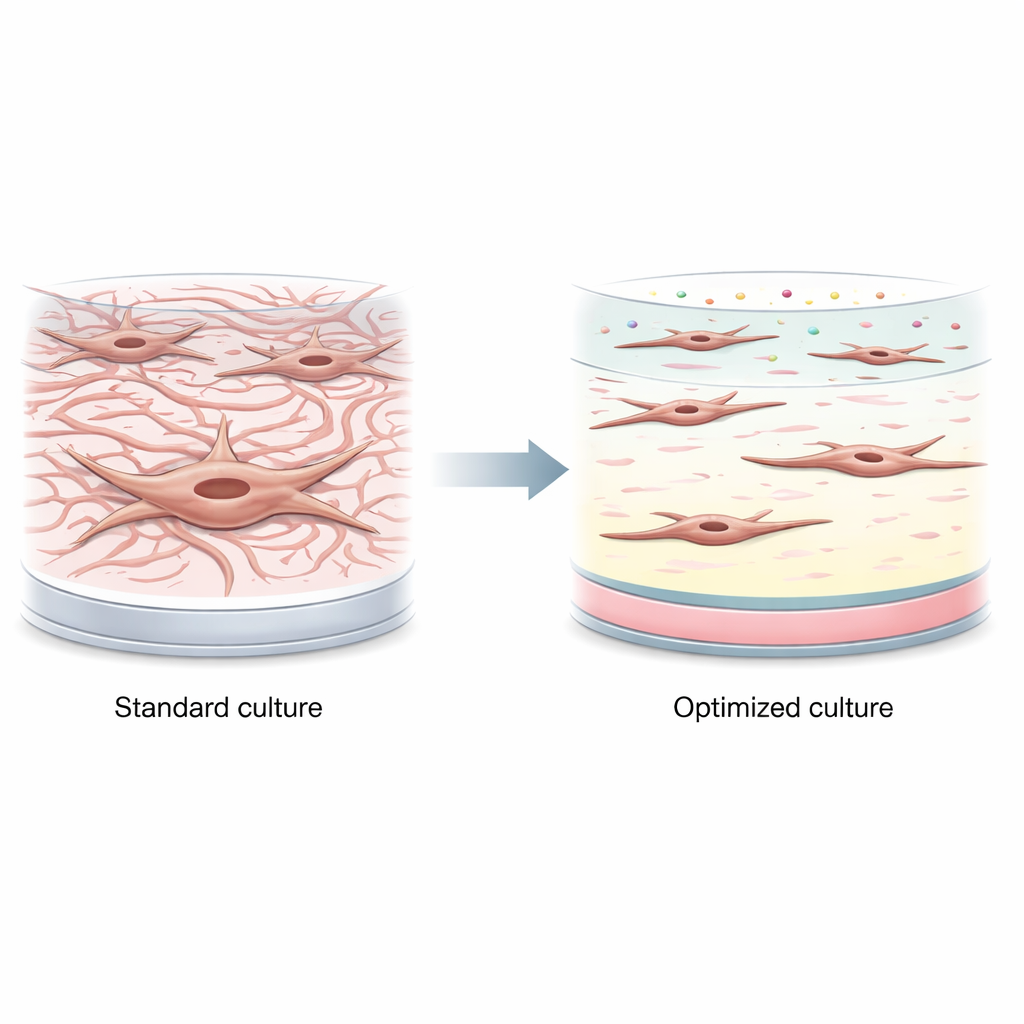
Tester des ingrédients isolés ne suffit pas
Pour calmer à nouveau les cellules, l’équipe a exploré des composants du microenvironnement naturel des fibroblastes dans l’intestin, incluant des protéines de la matrice essentielles (collagènes de types I et III, et laminine) et des facteurs solubles (vitamine D et facteur de croissance des fibroblastes basique, FGF). Ils ont testé ces éléments un par un, soit comme revêtements de surface, soit comme additifs au milieu de culture. Certaines conditions ont légèrement réduit les marqueurs d’activation : par exemple, des doses modérées de vitamine D ont fait chuter un marqueur majeur de cicatrisation de plusieurs fois, et certaines densités de revêtement ont eu des effets modestes. Mais ces bénéfices ont été contrebalancés par des problèmes, comme une survie cellulaire réduite à des doses élevées de vitamine D, et globalement ces ajustements isolés n’ont pas permis de maintenir de façon fiable les fibroblastes dans un état de faible activité.
Laisser les statistiques explorer l’espace des possibles
Plutôt que d’ajuster un paramètre à la fois, les chercheurs ont utilisé une approche formelle de « planification d’expériences » pour explorer efficacement de nombreuses combinaisons. Ils ont fait varier cinq entrées — les trois protéines matricielles plus la vitamine D et le FGF — sur une large gamme de doses, générant 42 conditions de culture soigneusement choisies. Pour chacune, ils ont mesuré quatre résultats liés à la cicatrisation : un marqueur d’activation clé, la sécrétion d’une protéine matricielle majeure (la fibronectine), la croissance cellulaire et la survie cellulaire. Des modèles statistiques ont ensuite révélé quels facteurs, et quelles associations entre eux, avaient la plus grande influence. La vitamine D est apparue comme un acteur puissant mais sensible à la dose, affectant tous les paramètres mesurés, tandis que le FGF tendait à réduire l’activation et à soutenir la croissance et la survie des cellules. Le collagène I, le collagène III et la laminine modulaient la façon dont ces signaux solubles étaient interprétés, certaines combinaisons atténuant l’activation bien plus que n’importe quel facteur seul.
Élaborer une recette pour des fibroblastes calmes mais en bonne santé
À partir de ces modèles, l’équipe a demandé au logiciel d’identifier des conditions qui diminueraient simultanément les marqueurs d’activation et la production de matrice tout en maintenant la viabilité cellulaire, sans exiger une faible prolifération. La meilleure recette combinait une forte densité de collagène I, peu de collagène III et une laminine élevée sur la surface de culture, associées à une vitamine D à dose moyenne et à un FGF élevé dans le milieu. Avec ce protocole, les fibroblastes restaient fins et en forme de fuseau plutôt que diffus et étoilés, exprimaient des niveaux bien plus faibles de gènes et de protéines liés à la contraction et à la fibrose, et sécrétaient beaucoup moins de collagène et de fibronectine. Parallèlement, leur viabilité était aussi élevée, voire meilleure, que celle des cellules cultivées sur du plastique nu. Fait important, ces effets se sont observés non seulement pour la lignée modèle, mais aussi pour des fibroblastes primaires issus de donneurs humains masculins et féminins, montrant la robustesse du protocole.
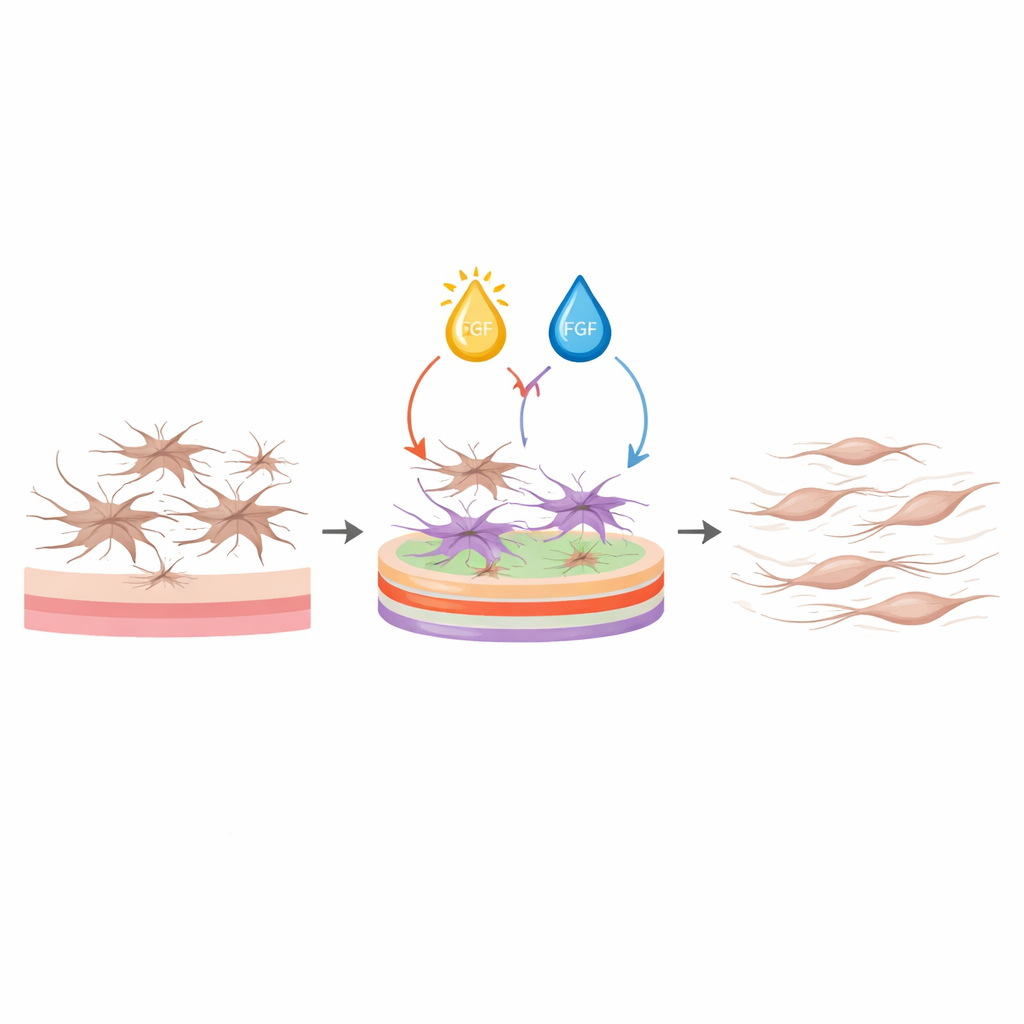
Ce que cela signifie pour la recherche future sur la fibrose intestinale
En ajustant soigneusement le « voisinage » des fibroblastes intestinaux — à la fois la surface à laquelle ils adhèrent et les facteurs qui les baignent — cette étude propose un protocole simple qui maintient ces cellules dans un état non activé mais sain en utilisant des matériaux de laboratoire standard. Pour les chercheurs, cela fournit un point de départ propre pour ajouter des signaux inflammatoires ou mécaniques spécifiques et observer comment la fibrose débute, plutôt que de travailler avec des cellules déjà cicatricielles. Plus largement, le travail démontre comment la planification expérimentale statistique peut révéler des combinaisons d’ingrédients subtiles et non intuitives qui maîtrisent des comportements cellulaires complexes, ouvrant la voie à de meilleurs modèles de cicatrisation et, éventuellement, à des stratégies plus ciblées pour prévenir ou inverser la fibrose intestinale.
Citation: Mohammadalizadeh, Z., Sudi, S., Basto Moreno, D.A. et al. Developing a protocol to counteract spontaneous in vitro activation of intestinal fibroblasts using design of experiments. npj Biomed. Innov. 3, 25 (2026). https://doi.org/10.1038/s44385-026-00079-5
Mots-clés: fibrose intestinale, activation des fibroblastes, protocole de culture cellulaire, vitamine D et FGF, planification d’expériences