Clear Sky Science · fr
Déduire les anomalies des voies de signalisation à partir d'images histopathologiques via un graphe hétérogène gène-voie contraint par la logique
Voir les signaux cellulaires cachés dans les lames de cancer
Quand les médecins examinent un cancer au microscope, ils observent principalement des formes et des couleurs, pas les conversations moléculaires complexes qui ont lieu à l’intérieur des cellules. Pourtant, ces « conversations » de signalisation invisibles entre gènes et voies déterminent souvent la façon dont une tumeur croît et comment elle peut répondre à un traitement. Cette étude présente un nouveau système d’intelligence artificielle qui lit des images de pathologie de routine et infère quelles voies de communication cellulaires, ou voies de signalisation, dysfonctionnent—offrant un moyen d’apercevoir le comportement moléculaire sans tests de laboratoire supplémentaires.
Des indices sur des gènes isolés à une vue d’ensemble
Les approches traditionnelles tentent de prédire le statut de gènes individuels à partir d’images tissulaires : un gène particulier est-il muté ou non ? C’est utile, mais le cancer dépend rarement d’un seul gène défaillant. À la place, des groupes de gènes agissent de concert pour perturber des voies de signalisation entières qui contrôlent la croissance, la survie et l’immunité. Les auteurs soutiennent que se concentrer sur des gènes isolés fait manquer ce comportement coopératif et peut échouer à expliquer pourquoi les tumeurs apparaissent et se comportent de telle ou telle manière au microscope.
Construire une carte entre images, gènes et voies
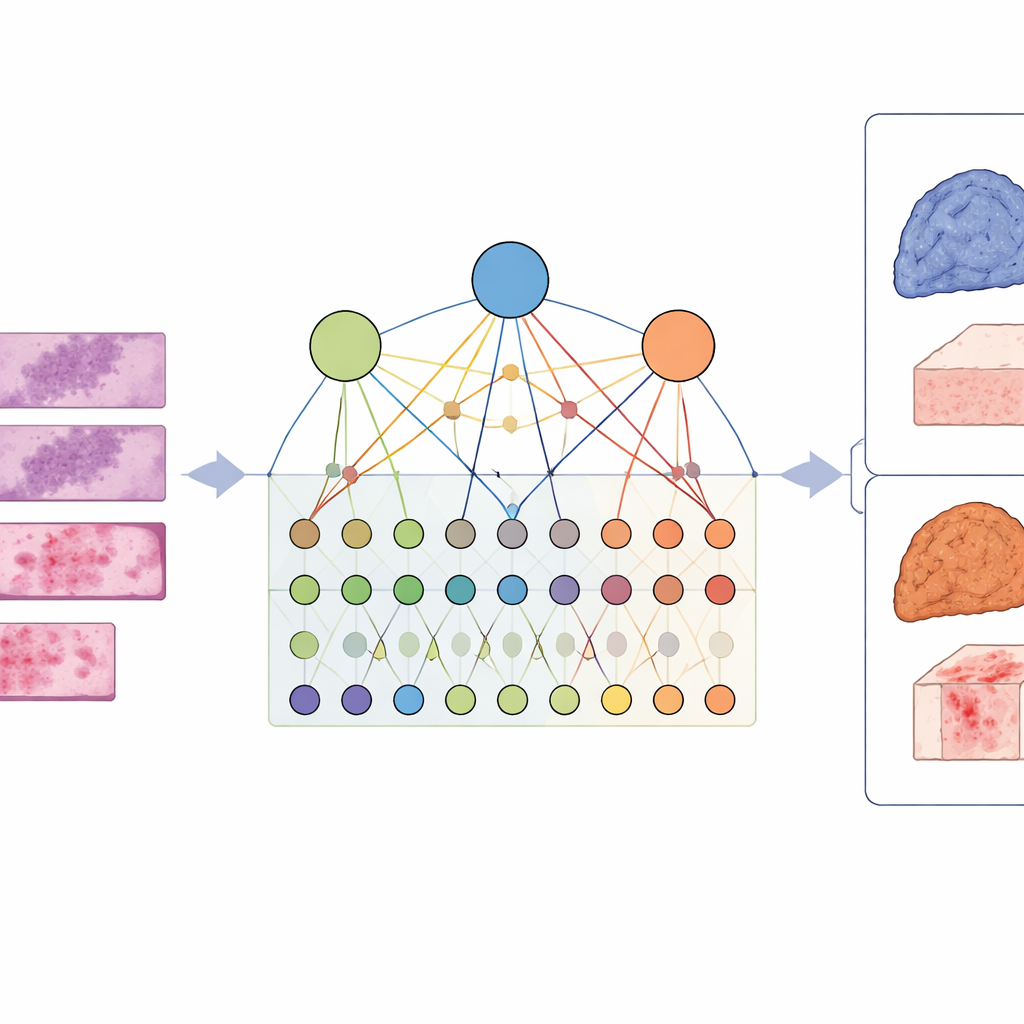
Pour saisir cette complexité, les chercheurs ont conçu un cadre appelé LCG-HGNN qui relie trois couches d’informations. D’abord, ils divisent chaque lame entière d’adénocarcinome pulmonaire en nombreux petits patchs et représentent ces patchs sous forme de graphe, où des régions proches ou d’apparence similaire sont connectées. Ensuite, ils relient des marqueurs géniques aux voies de signalisation en utilisant des bases de données biologiques établies, construisant un second graphe qui encode quels gènes appartiennent à quelles voies. Enfin, ils laissent un modèle d’IA faire circuler l’information à travers ce graphe combiné, de sorte que les motifs d’image, les gènes et les voies s’influencent mutuellement plutôt que d’être traités isolément.
Enseigner à l’algorithme la biologie connue
Une innovation clé est que le modèle n’est pas autorisé à apprendre librement sans orientation. Les auteurs intègrent des énoncés clairs, de type règle, dérivés de décennies de recherche sur le cancer. Par exemple, certaines mutations n’apparaissent presque jamais ensemble dans la même tumeur, et certaines voies sont en amont ou en aval d’autres. Ils codent ces règles sous forme de contraintes logiques qui orientent en douceur les connexions internes et les prédictions de l’IA. Si le modèle propose une combinaison de changements géniques et de voies qui entre en conflit avec la biologie connue ou avec des similarités entre les lames des patients, ces règles le poussent vers des alternatives plus réalistes.
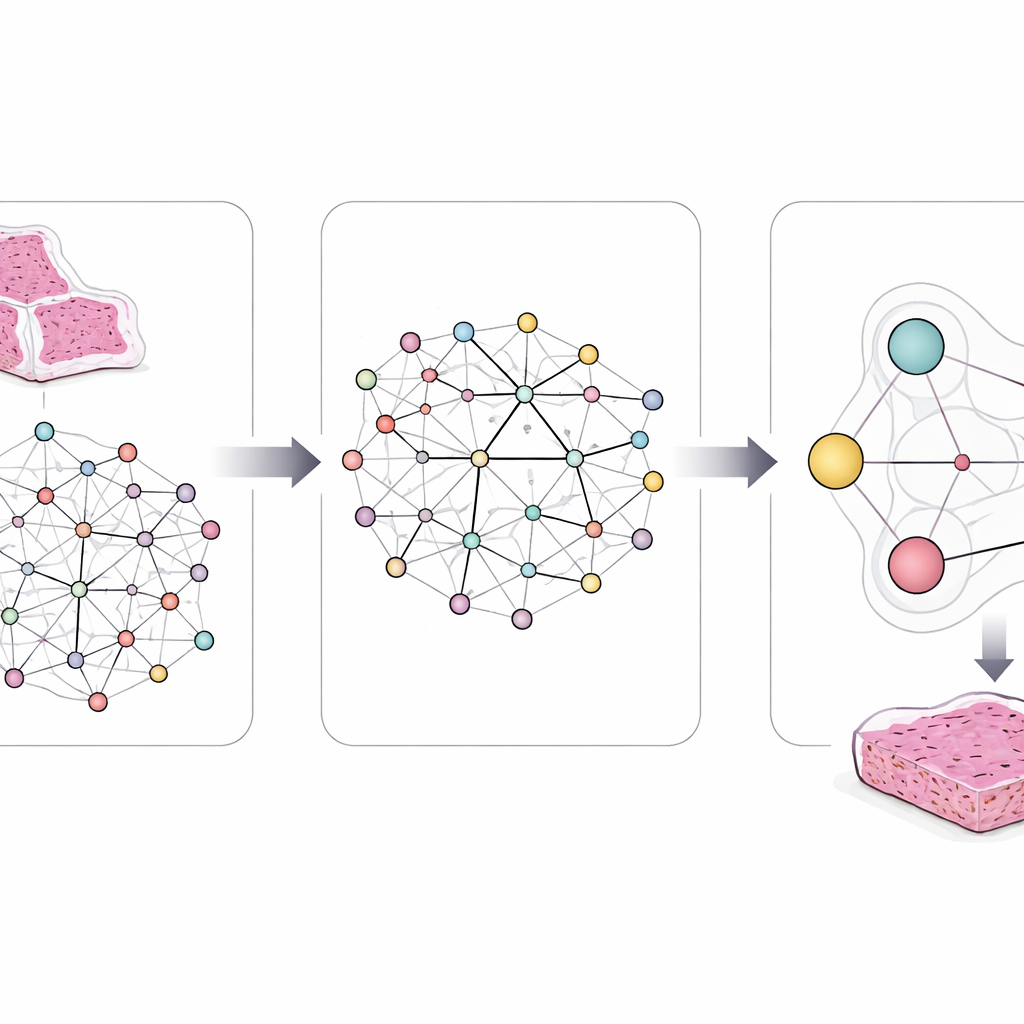
Tester la précision par rapport aux méthodes existantes
L’équipe a évalué son système sur plus de 1 600 lames de cancer du poumon liées à des données génétiques. Ils l’ont comparé à des modèles d’apprentissage profond standard qui se concentrent sur des gènes uniques et à des méthodes plus avancées qui traitent de nombreux gènes à la fois mais ignorent la structure des voies. Sur plusieurs voies importantes, y compris celles impliquées dans les signaux de croissance cellulaire et l’armature tissulaire, le nouveau modèle a prédit les altérations de groupes de gènes et les anomalies de voies avec plus de précision. Il a également produit des patchs d’image dont l’apparence correspondait étroitement à des exemples cliniques réels connus pour être associés à des mutations spécifiques, suggérant qu’il se focalisait sur des motifs microscopiques pertinents plutôt que sur des artefacts d’image aléatoires.
Pourquoi cela compte pour les patients
Pour un non-spécialiste, le résultat principal est que cette approche transforme une lame de pathologie de routine en une source riche d’informations moléculaires. Au lieu de commander des tests génétiques séparés, souvent coûteux, pour chaque cible possible, les médecins pourraient à terme utiliser de tels modèles pour dépister des voies perturbées directement à partir des images qu’ils recueillent déjà. Bien que la méthode nécessite encore une validation plus large en conditions réelles et ne remplace pas encore les tests génomiques, elle ouvre la voie vers un avenir où la vue au microscope fait aussi office de fenêtre sur le câblage interne de la tumeur—aidant à orienter des soins du cancer plus précis et mieux informés biologiquement.
Citation: Yu, Y., Shi, W., Chen, X. et al. Inferring signaling pathway abnormalities from histopathological images via logic-constrained gene-pathway heterogeneous knowledge graph. npj Biomed. Innov. 3, 23 (2026). https://doi.org/10.1038/s44385-026-00078-6
Mots-clés: voies du cancer, IA en histopathologie, réseaux de neurones sur graphes, adénocarcinome pulmonaire, pathologie numérique