Clear Sky Science · fr
Modèles in vitro biofabriqués en 3D comme nouvelles méthodologies d’approche pour des alternatives aux animaux
Repenser la manière dont nous testons les nouveaux médicaments
Pendant près d’un siècle, la plupart des nouveaux médicaments ont été testés sur des animaux avant d’entrer en essais humains. Pourtant, plus de 9 candidats sur 10 qui semblent sûrs chez l’animal échouent chez l’homme. Cet article examine comment une nouvelle génération de tissus humains « bioprintés » en 3D pourrait changer cette trajectoire — offrant des moyens plus précis et plus humains de prédire la réponse de nos organismes aux médicaments, et potentiellement accélérer l’arrivée de traitements plus sûrs pour les patients.

Des animaux de laboratoire à des tests centrés sur l’humain
Une législation américaine récente, connue sous le nom de FDA Modernization Act 2.0, a supprimé l’obligation automatique de tester systématiquement chaque nouveau médicament sur des animaux. Désormais, les régulateurs peuvent accepter des « nouvelles méthodologies d’approche » — des systèmes d’essai pertinents pour l’humain conçus pour mieux prévoir les réponses réelles des patients. Parmi eux, la bioimpression 3D se distingue. Elle utilise des imprimantes spécialisées pour déposer des cellules humaines vivantes et des matériaux gélifiés souples en formes complexes qui imitent de vrais tissus et mini-organes. Le processus commence souvent par des images médicales comme des scanners ou des IRM, qui servent de plan. Les chercheurs choisissent ensuite des biomatériaux appropriés, incorporent les types de cellules adéquats pour créer une « bio-encre » imprimable, et impriment des structures en couche ou volumétriques qui mûrissent en modèles tissulaires fonctionnels dans des bioréacteurs.
Comment la bioimpression 3D construit des tissus vivants
La bioimpression n’est pas une technologie unique mais une famille de méthodes. Les imprimantes de type jet d’encre pulvérisent de minuscules gouttelettes de fluide contenant des cellules pour construire des couches fines avec un grand niveau de détail, ce qui les rend utiles pour des tissus miniatures tels que des patchs cutanés ou des barrières pulmonaires. Les imprimantes par extrusion poussent des fils continus de bioencres plus denses, qui peuvent contenir de nombreuses cellules et des fibres de soutien, permettant la construction de structures plus larges et robustes comme des valves cardiaques, des modèles de tumeurs hépatiques ou des réseaux vasculaires. Une classe plus récente, appelée photopolymérisation en cuve, projette de la lumière programmée dans un liquide pour solidifier des formes complexes sans forcer les cellules à passer par des buses. Des variantes de cette méthode peuvent sculpter des caractéristiques à l’échelle micrométrique, imprimer un petit organe entier en quelques secondes, ou même façonner des tissus à l’intérieur d’un bain transparent, tout en maintenant la viabilité cellulaire.
Remplacer et affiner les tests pharmaceutiques
Ces tissus imprimés sont déjà utilisés pour repenser la chaîne du médicament. En découverte précoce, des constructions spécifiques au patient ou à la maladie — comme des modèles tumoraux bioprintés — permettent aux chercheurs de tester de nombreux candidats-médicaments dans des environnements 3D réalistes qui ressemblent mieux aux maladies humaines que des couches cellulaires plates en culture. En préclinique, des tissus imprimés de peau, de poumon et de foie se révèlent plus précis que les animaux pour détecter des toxicités ou effets secondaires spécifiques à l’humain. Certaines études vont plus loin en imprimant de « essais cliniques sur puce », où des tissus issus de cellules de différents donneurs sont exposés en parallèle à un médicament, révélant qui pourrait en bénéficier ou en être lésé. Les régulateurs encouragent désormais les entreprises à soumettre les données issues de ces modèles en complément des études animales, afin de constituer les preuves nécessaires à une acceptation plus large.
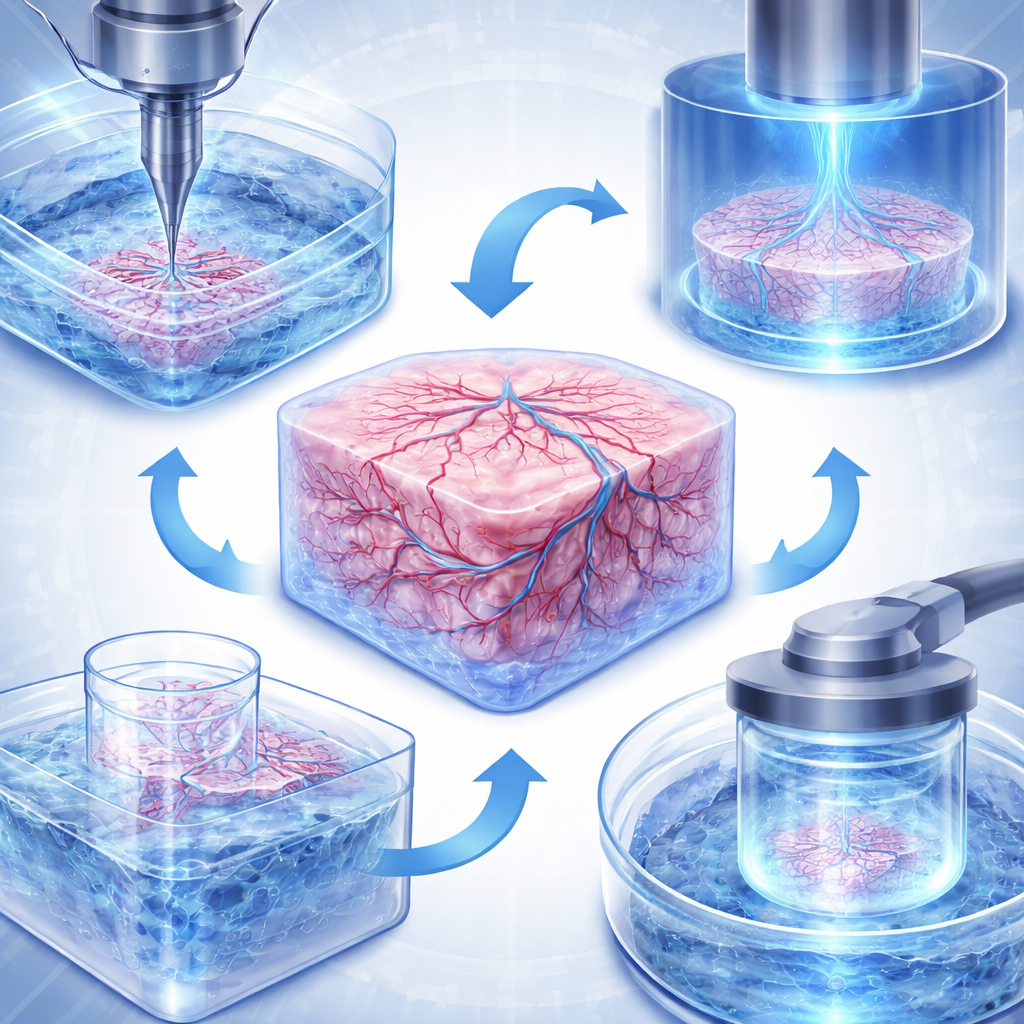
Ingénierie d’organes sans corps
Malgré les progrès rapides, plusieurs obstacles demeurent avant que les tissus bioprintés puissent remplacer couramment les tests sur animaux. Un défi majeur est l’alimentation en sang : de vrais organes contiennent des réseaux de vaisseaux allant des artères de gros calibre jusqu’aux capillaires très fins, tandis que les constructions imprimées doivent surmonter une limite naturelle à la diffusion de l’oxygène et des nutriments. Les chercheurs s’attaquent à cela par de nouvelles stratégies d’impression qui créent des canaux ramifiés, par des bains de support qui maintiennent les tissus mous en place pendant la formation de minuscules vaisseaux, et par des imprimantes volumétriques ultra-rapides qui réalisent des structures épaisses et denses en cellules avant que celles-ci ne commencent à souffrir. Un autre défi est le réalisme : les tissus vivants sont des mélanges de nombreux types cellulaires baignés dans des signaux chimiques complexes et, souvent, influencés par le microbiome et des organes distants. Les modèles avancés combinent désormais plusieurs populations cellulaires, des gradients contrôlés d’oxygène et de pH, et même des systèmes « multi-organes » reliés qui connectent intestin, foie, système immunitaire et tissus cérébraux par des flux de liquide pour imiter des réponses à l’échelle du corps entier.
Un avenir plus humain et prédictif pour le développement de médicaments
Pris ensemble, ces progrès suggèrent un avenir où des modèles tissulaires fidèles et basés sur l’humain deviendront centraux dans l’évaluation des médicaments. L’article conclut que la bioimpression 3D passe d’une technique de laboratoire de niche à un outil clé pour construire des systèmes d’essai standardisés et acceptables par les régulateurs. Pour concrétiser pleinement cette promesse, scientifiques et autorités devront s’accorder sur les usages et les limites de ces modèles, démontrer qu’ils prédisent de manière fiable les résultats humains, et résoudre les défis techniques restants comme la construction d’une vascularisation stable et d’organes anatomiquement complexes. Si cela réussit, ce basculement pourrait réduire la dépendance aux tests sur animaux, diminuer les coûteux échecs tardifs en développement, et fournir des thérapies plus sûres et plus efficaces tout en reflétant mieux la biologie qui compte le plus : la nôtre.
Citation: Hua, W., Gaharwar, A.K. 3D biofabricated in vitro models as new approach methodologies for animal alternatives. npj Biomed. Innov. 3, 20 (2026). https://doi.org/10.1038/s44385-026-00073-x
Mots-clés: bioimpression 3D, alternatives aux tests sur les animaux, développement de médicaments, modèles tissulaires, bioimpression volumétrique