Clear Sky Science · fr
Ingénierie des macrophages pour l’immunothérapie du cancer : nouvelles perspectives et potentiel thérapeutique
Transformer l’équipe de nettoyage du corps en combattants contre le cancer
Nos organismes regorgent de macrophages — des cellules « nettoyeuses » mobiles qui engloutissent microbes et débris cellulaires. Cet article de synthèse examine comment les scientifiques apprennent à rediriger ces cellules contre le cancer. Parce que les macrophages sont abondants au sein des tumeurs, y compris dans celles qui résistent aux immunothérapies actuelles, les comprendre et les modifier pourrait ouvrir de nouvelles options pour des patients atteints de cancers difficiles à traiter.
Les multiples visages d’un seul type cellulaire
Les macrophages ne constituent pas un type cellulaire fixe ; ce sont des caméléons. Ils peuvent provenir du sang ou être résidents tissulaires, et une fois installés ils répondent aux signaux locaux. Dans les tumeurs, ces macrophages associés aux tumeurs peuvent soit contribuer à tuer les cellules cancéreuses soit, de manière paradoxale, favoriser la croissance et la diffusion tumorales. Autrefois, les chercheurs tentaient de les classer en deux catégories — « M1 » (mode attaque) et « M2 » (mode réparation ou soutien). Les nouveaux outils de cartographie génétique et spatiale révèlent désormais un spectre bien plus riche d’états, avec de multiples sous-groupes et comportements qui varient selon la tumeur et l’emplacement. Même des cellules auparavant considérées comme fermement « pro-tumeur » peuvent, dans certains contextes, mobiliser les cellules T et soutenir l’immunité antitumorale.
Percevoir leur environnement et engloutir les cellules cancéreuses
Les macrophages n’écoutent pas seulement des signaux chimiques ; ils perçoivent aussi le monde physique qui les entoure. En progressant dans le maillage dense de protéines d’une tumeur, en se frayant un chemin entre les cellules et en subissant des forces fluides, ils détectent la rigidité et la contrainte via des récepteurs spécialisés comme Piezo1. Ces indices mécaniques, conjointement aux signaux immunitaires classiques, peuvent orienter les macrophages vers des rôles plus inflammatoires ou plus apaisants. Sur le plan fonctionnel, les macrophages peuvent engloutir des cellules cancéreuses, les dégrader puis présenter des fragments (antigènes) aux cellules T, faisant le lien entre immunité innée et adaptative. Les cellules cancéreuses ripostent en envoyant des signaux « ne me mangez pas », notamment par une molécule de surface appelée CD47 qui active un frein sur les macrophages. Des médicaments bloquant cette interaction sont en essais cliniques nombreux, augmentant l’élimination des cellules tumorales mais nécessitant un réglage fin pour éviter d’endommager les cellules saines.
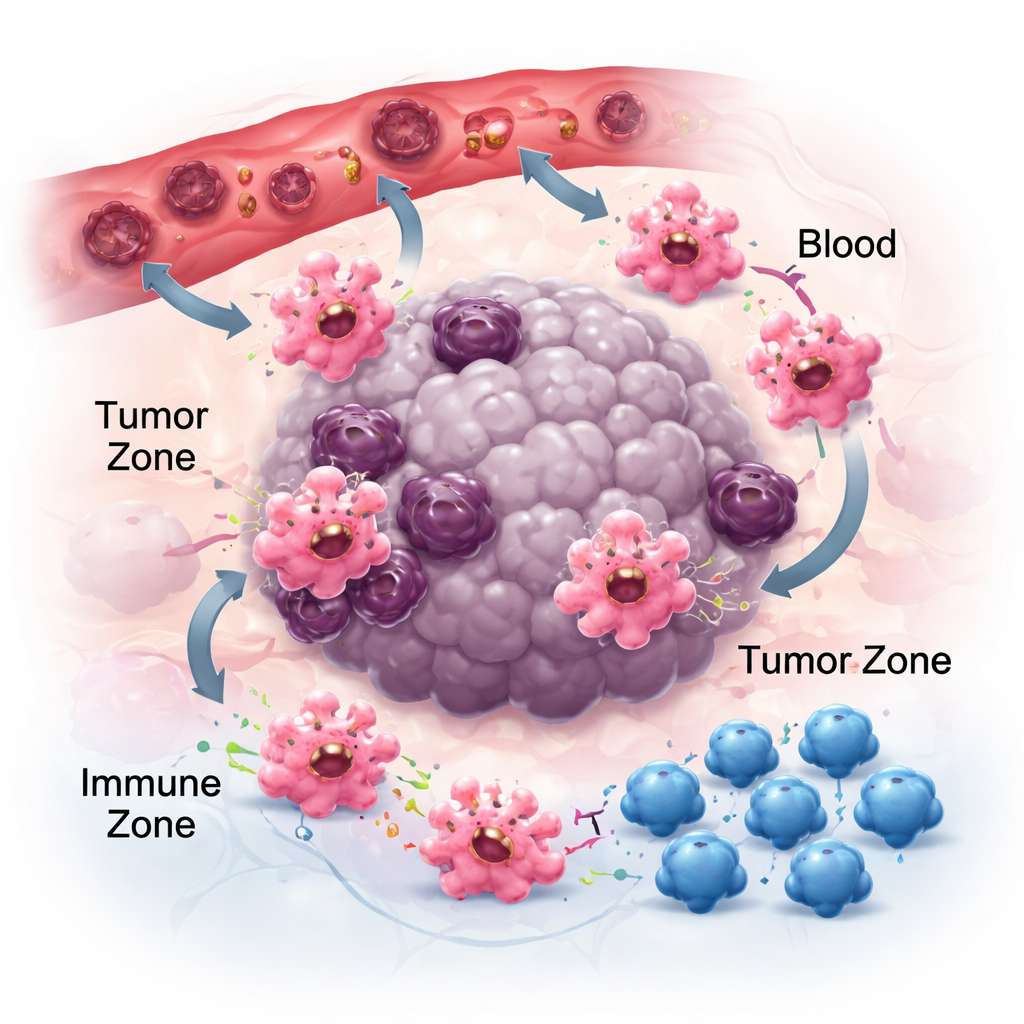
Se déplacer, adhérer et communiquer dans le voisinage tumoral
Pour être efficaces contre le cancer, les macrophages doivent d’abord atteindre les tumeurs puis se positionner dans les niches appropriées. Ils suivent des pistes chimiques — chimiokines et facteurs de croissance — libérées par les cellules tumorales et les cellules environnantes. Des paires comme CCR2–CCL2 contribuent à les attirer vers les tumeurs, et des médicaments bloquant ces signaux peuvent réduire l’accumulation de macrophages, sans l’éliminer complètement, ce qui suggère d’autres attractifs tels que CSF‑1 et VEGF. Une fois en place, la manière dont les macrophages adhèrent à la matrice locale influence aussi leur comportement. Leurs récepteurs d’adhésion, appelés intégrines, ne servent pas seulement de colle ; ils amplifient les signaux inflammatoires et peuvent pousser les cellules vers des états plus anti‑tumoraux. Parallèlement, les macrophages émettent de petites particules appelées vésicules extracellulaires qui transportent ARN et protéines vers les cellules voisines. Selon le type de tumeur, ces vésicules peuvent soit atténuer l’immunité et favoriser la dissémination, soit renforcer les réponses antitumorales, soulignant le caractère dépendant du contexte de la communication macrophagique.
Reprogrammer les macrophages par gènes et matériaux
Parce que les macrophages infiltrent naturellement mieux les tumeurs solides que de nombreuses cellules T, les chercheurs les reconfigurent aujourd’hui comme des médicaments vivants. Une stratégie génétique emprunte à la thérapie par récepteurs antigéniques chimériques (CAR) des lymphocytes T : l’ajout d’un récepteur synthétique pour créer des macrophages CAR (CAR‑M). Ces cellules conçues reconnaissent des marqueurs tumoraux, engloutissent plus efficacement les cellules cancéreuses, digèrent la matrice environnante, libèrent des signaux inflammatoires et activent les cellules T en présentant des antigènes tumoraux. Les premiers essais humains de CAR‑M ciblant HER2 montrent une sécurité et une activité biologique encourageantes, bien que davantage de travail soit nécessaire pour démontrer des bénéfices robustes et durables. Parallèlement, des approches non génétiques utilisent des particules et des « sacs à dos » fabriqués à partir de lipides ou de polymères. Les macrophages peuvent ingérer des nanoparticules chargées de médicaments et les transporter profondément dans les tumeurs comme des chevaux de Troie, ou porter des patchs fixés à leur surface qui relâchent lentement des signaux immunostimulants, les aidant à conserver une identité antitumorale sans surcharger leur intérieur. Les vésicules dérivées de macrophages sont elles aussi testées comme véhicules de livraison naturels et sans cellules.
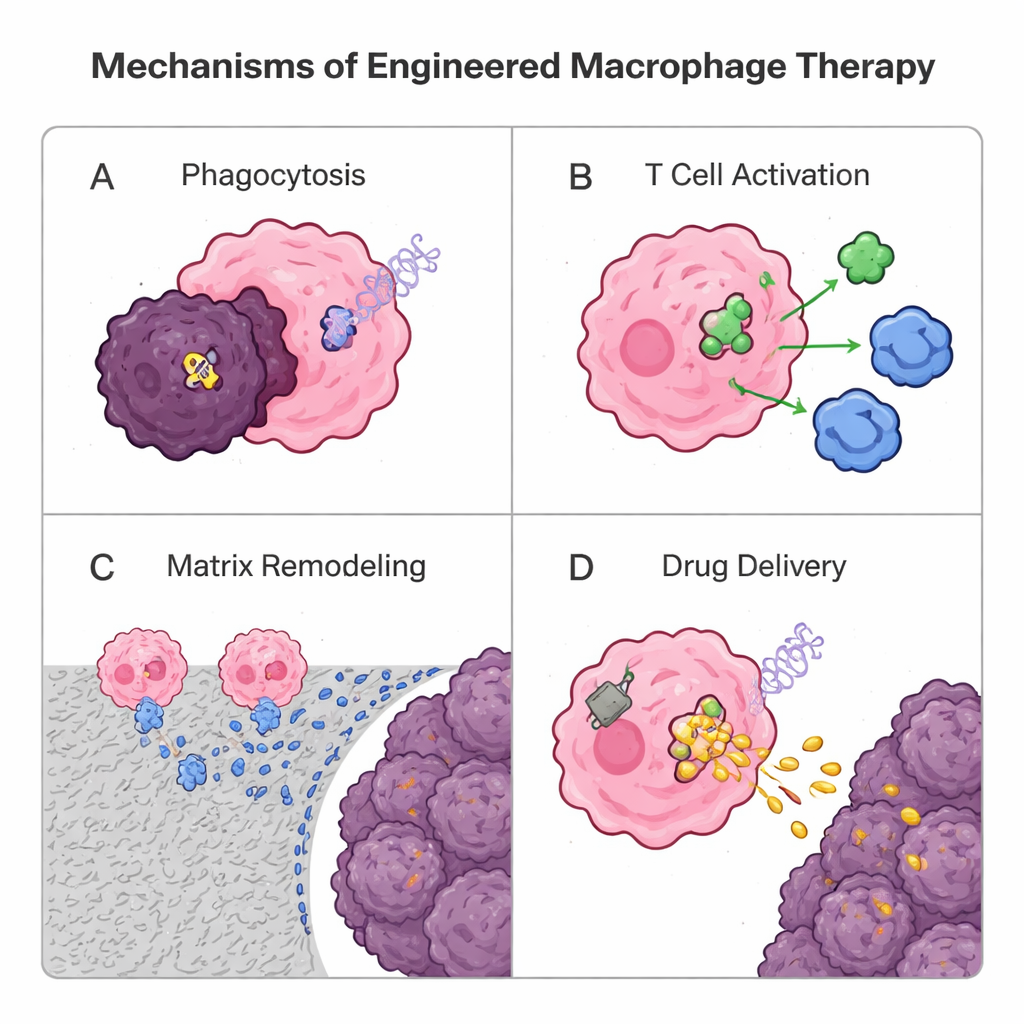
Défis à venir et raisons d’espérer
Malgré leur potentiel, les thérapies à base de macrophages doivent surmonter des obstacles pratiques. Produire en quantité suffisante des cellules cohérentes à partir de patients est long et coûteux, et une fois perfusées, ces cellules ne vivent ni ne se multiplient indéfiniment. Leur plasticité intrinsèque, utile biologiquement, complique le maintien d’un état anti‑tumoral dans un microenvironnement tumoral complexe et suppressif. Les auteurs soutiennent que des modèles bio‑ingénierés avancés — cultures 3D, organoïdes et systèmes organ‑on‑a‑chip reproduisant la mécanique tissulaire réelle — seront cruciaux pour comprendre et prédire le comportement des macrophages modifiés chez les patients. Malgré tout, leur capacité naturelle à pénétrer les tumeurs solides, à phagocyter les cellules cancéreuses et à réveiller les cellules T, combinée à des premiers retours de sécurité, suggère que les thérapies basées sur les macrophages pourraient devenir une nouvelle arme importante, notamment contre les tumeurs « froides » qui résistent actuellement à la plupart des traitements immunitaires.
Citation: Block, A., Liu, X., Zhang, D. et al. Engineering macrophages for cancer immunotherapy: emerging insights and therapeutic potential. npj Biomed. Innov. 3, 18 (2026). https://doi.org/10.1038/s44385-026-00072-y
Mots-clés: immunothérapie par macrophages, microenvironnement tumoral, macrophages CAR, phagocytose, libération de médicaments par nanoparticules