Clear Sky Science · fr
Un échafaudage électrofilé modifié en surface soutient la fonction des cellules souches limbaires dérivées d’iPSC
Redonner une chance à la vue
Lorsque la fenêtre claire à l'avant de l'œil — la cornée — est endommagée, la perte de vision peut devenir permanente. Un responsable majeur est la disparition de cellules spécialisées situées au bord de la cornée, appelées cellules souches limbaires, qui maintiennent normalement la surface claire et lisse. Cet article décrit un nouveau « pansement vivant » fabriqué en laboratoire qui pourrait, un jour, transporter des cellules souches de remplacement vers l'œil et contribuer à restaurer la vue de manière plus sûre et plus fiable que les méthodes actuelles.
Pourquoi le bord de l’œil est important
La cornée est composée de plusieurs couches et doit rester lisse et transparente pour réfracter correctement la lumière. Un petit anneau de cellules souches, situé à la frontière entre la cornée claire et le blanc de l'œil, renouvelle en permanence sa couche la plus externe. Une blessure, une infection ou une maladie auto‑immune peut détruire ces cellules limbaires, provoquant une affection connue sous le nom de déficit des cellules souches limbaires. Sans elles, des vaisseaux sanguins envahissent la cornée normalement claire, la surface se cicatrise et devient irrégulière, et les patients peuvent subir une perte de vision sévère ou la cécité. Les médecins peuvent transplanter des cellules souches saines, mais ils ont encore besoin d’un support sûr, solide et transparent pour délivrer ces cellules fragiles à l’œil endommagé.
Construire un « pansement vivant » synthétique
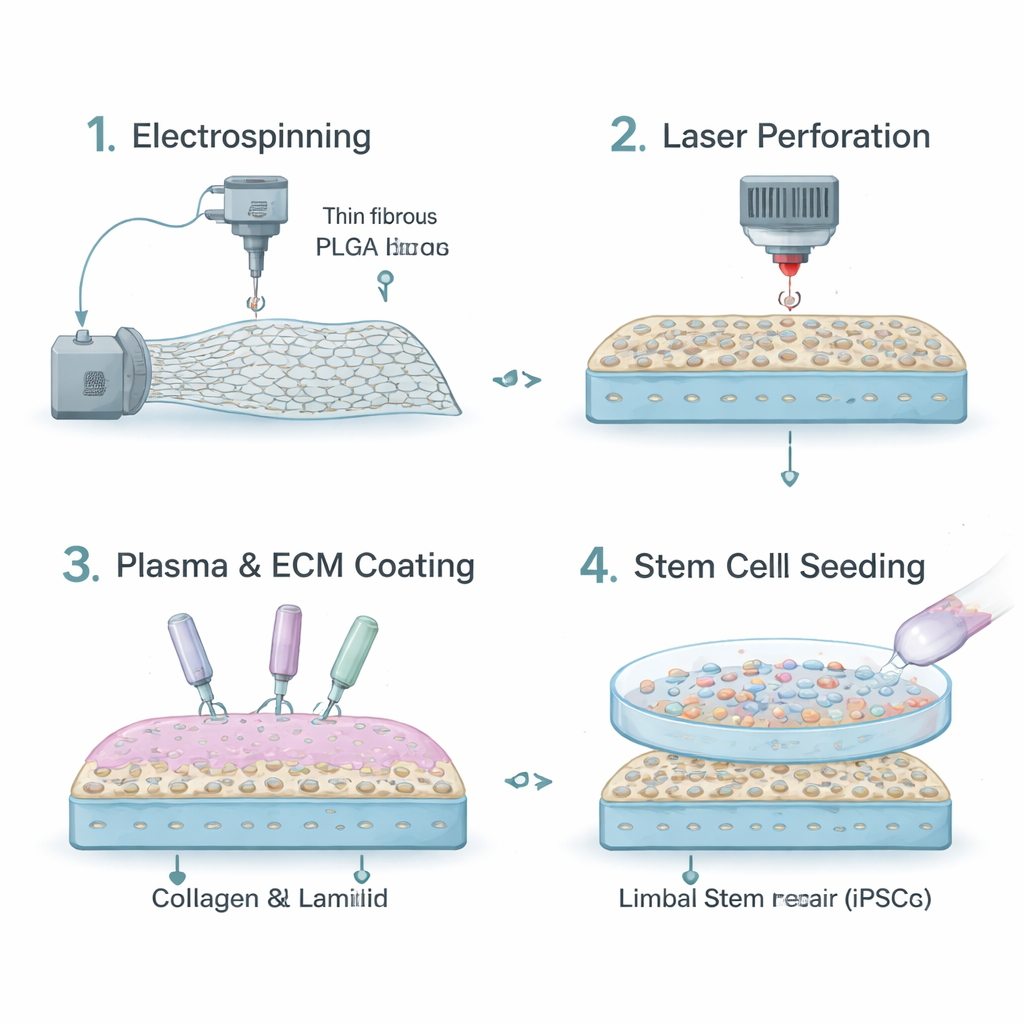
Aujourd’hui, de nombreux chirurgiens s’appuient sur des tissus naturels tels que la membrane amniotique ou des feuilles de collagène comme supports. Bien que ces matériaux soient biocompatibles, ils varient d’un donneur à l’autre, peuvent être en quantité limitée et n’autorisent pas un contrôle précis de leur durée de vie ou de leur rigidité. Les chercheurs se sont donc tournés vers un plastique biodégradable appelé PLGA, déjà utilisé dans certains dispositifs médicaux. Grâce à une technique appelée électrofilage, ils ont transformé le PLGA en un tapis de fibres microscopiques qui ressemble à la couche de soutien naturelle de l’œil. Cette feuille fibreuse est suffisamment résistante pour être manipulée pendant la chirurgie et peut être ajustée pour se dissoudre lentement au fur et à mesure de la cicatrisation de l’œil.
Rendre l’échafaudage favorable aux cellules et transparent
Le PLGA nu, toutefois, repousse l’eau et n’attire pas naturellement les cellules. Pour rendre sa surface plus accueillante, l’équipe a traité les fibres par plasma atmosphérique, qui ajoute des groupes chimiques capables de capturer des protéines. Ils ont ensuite recouvert l’échafaudage de collagène IV et de laminine‑521, deux composants clés de l’« habitat » naturel des cellules souches autour de la cornée. Pour améliorer la transparence, ils ont utilisé un laser précis pour percer des trous microscopiques dans la membrane. Ces micro‑perforations ont augmenté la quantité de lumière traversant l’échafaudage d’environ 44 % à près de 60 %, rapprochant ainsi sa clarté de celle de la cornée réelle tout en conservant suffisamment de fibres pour l’adhésion cellulaire.
Tester les cellules souches sur la nouvelle surface
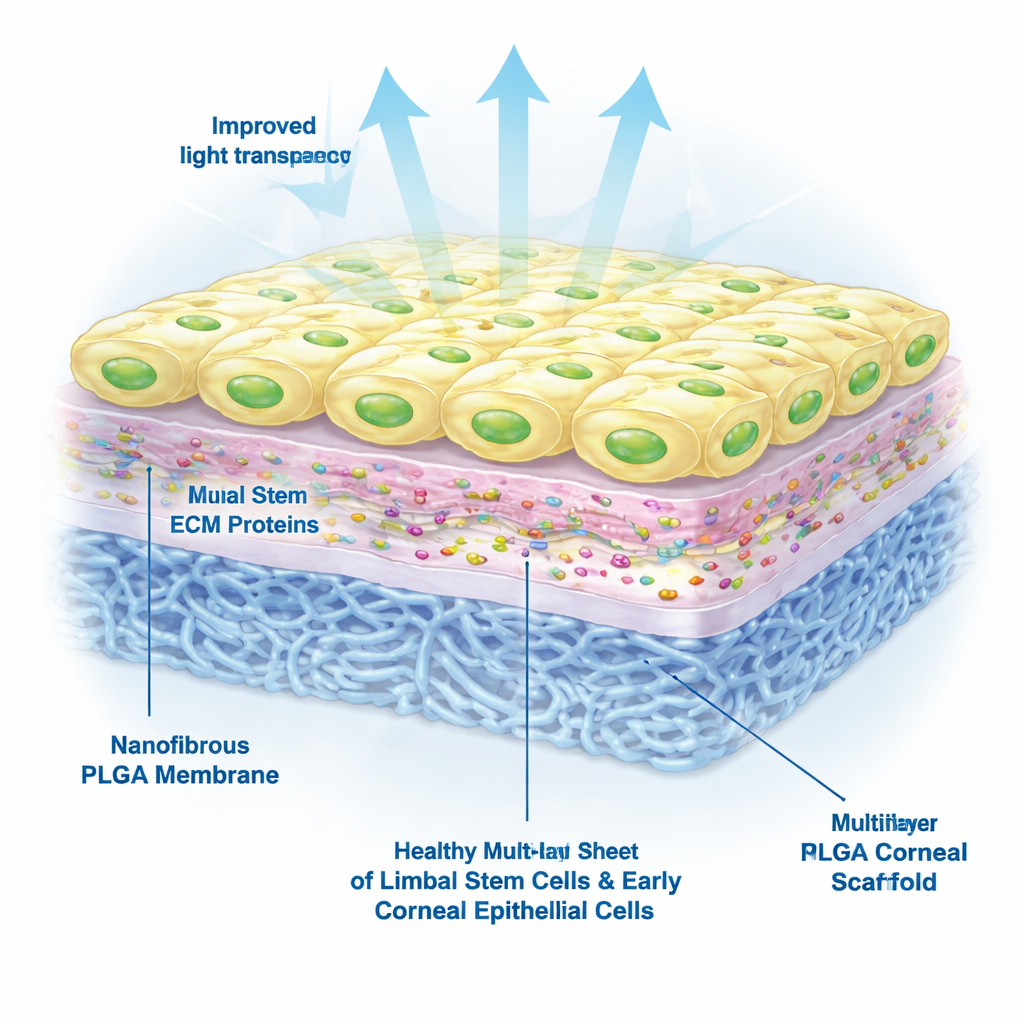
L’équipe a ensuite évalué la croissance de cellules souches limbaires dérivées de cellules souches pluripotentes induites — des cellules adultes reprogrammées dans un état souple, proche de la cellule souche — sur l’échafaudage. Ils ont comparé différents traitements de surface et constaté que la laminine‑521 était essentielle : les échafaudages traités au plasma et recouverts de laminine‑521, avec ou sans collagène IV, favorisaient une bonne adhésion, survie et croissance des cellules pendant au moins une semaine. En revanche, les cellules placées sur du PLGA non traité ou recouvert uniquement de collagène IV mouraient souvent ou se détachaient. Au microscope, les cellules sur l’échafaudage optimisé formaient des nappes compactes en « pavés », similaires à la surface cornéenne normale.
Maintenir les cellules souches prêtes à réparer
Au‑delà de la simple survie, les cellules transplantées doivent rester dans un état leur permettant à la fois de se renouveler et de produire de nouvelles cellules de surface cornéenne. Les chercheurs ont utilisé des marquages protéiques et des tests génétiques pour examiner l’identité des cellules sur leur échafaudage. Ils ont observé des signaux forts pour des marqueurs associés aux cellules souches limbaires et aux cellules cornéennes précoces, et seulement des signaux faibles pour des marqueurs de cellules pleinement matures. Ce profil suggère un mélange sain de cellules souches actives et de progéniteurs précoces prêts à reconstruire la surface cornéenne, plutôt qu’une population épuisée.
Ce que cela pourrait signifier pour les patients
Globalement, l’étude montre qu’un échafaudage entièrement synthétique et soigneusement conçu peut imiter de nombreuses caractéristiques de l’environnement naturel des cellules souches oculaires. En combinant un matériau fibreux réglable, des micro‑perforations pour une meilleure vision et un revêtement protéique soutenant spécifiquement les cellules souches limbaires, les auteurs ont créé un support prometteur pour de futures transplantations cellulaires. Bien que ce travail ait été réalisé en laboratoire et que des essais animaux et cliniques restent à réaliser, cette approche pourrait à terme offrir une solution plus cohérente, évolutive et personnalisée pour restaurer une surface cornéenne claire et saine et permettre à des personnes atteintes d’une perte de vision auparavant irréversible de retrouver la vue.
Citation: Mahmood, N., Zha, D., Gullion, S. et al. Surface modified electrospun scaffold supports iPSC-derived limbal stem cell function. npj Biomed. Innov. 3, 14 (2026). https://doi.org/10.1038/s44385-026-00066-w
Mots-clés: régénération cornéenne, cellules souches limbaires, échafaudage électrofilé, biomatériaux, cellules souches pluripotentes induites