Clear Sky Science · fr
Optimisation de l’induction de l’inflammation dans des organoïdes épithéliaux intestinaux dérivés de nourrissons prématurés
Pourquoi cela importe pour des nouveau‑nés fragiles
Les bébés nés très prématurément affrontent une combinaison dangereuse : un intestin immature et une communauté microbienne en rapide évolution. Ensemble, ces facteurs peuvent déclencher une inflammation incontrôlée qui endommage l’intestin et conduit à des affections potentiellement mortelles comme l’entérocolite nécrosante. Comme il est impossible d’expérimenter directement sur ces nourrissons, les chercheurs ont besoin de modèles de laboratoire réalistes de leur intestin pour tester ce qui déclenche l’inflammation et comment l’enrayer. Cette étude perfectionne un tel modèle en utilisant de petits tissus intestinaux cultivés en laboratoire, offrant une méthode plus claire pour examiner quels signaux microbiens font basculer la défense normale vers une inflammation nuisible.
Faire pousser un intestin prématuré en culture
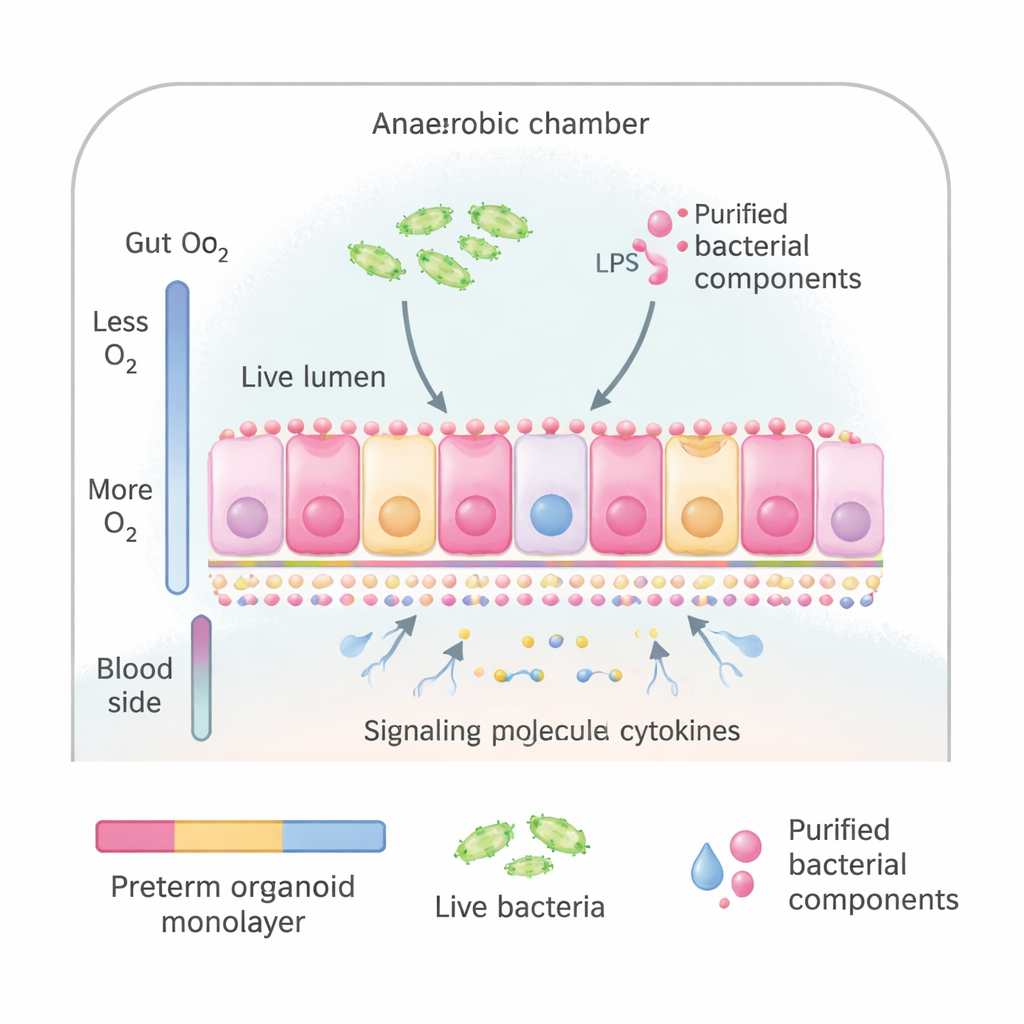
Les chercheurs ont utilisé des organoïdes intestinaux—de petites versions de la muqueuse intestinale cultivées à partir de cellules souches prélevées chez des nourrissons prématurés lors d’interventions chirurgicales. Ces organoïdes peuvent être aplatis en une fine couche cellulaire qui ressemble et se comporte comme la surface interne de l’intestin grêle, avec le bon sens « haut » (vers la lumière intestinale) et « bas » (vers la circulation sanguine). L’équipe a placé ces couches dans un système de culture spécial qui reproduit le gradient naturel d’oxygène de l’intestin : faible oxygène du côté exposé aux microbes et oxygène plus élevé du côté sanguin. Cela leur a permis d’exposer la surface « intestinale » soit à des bactéries entières issues de nourrissons prématurés, soit à des composants bactériens purifiés connus pour alerter le système immunitaire.
Tester ce qui déclenche le mieux l’alarme inflammatoire
Les scientifiques ont comparé plusieurs façons de provoquer l’inflammation : un mélange de bactéries vivantes couramment retrouvées chez des prématurés malades ; ces mêmes bactéries tuées par la chaleur ; et deux signaux bactériens purifiés, le lipopolysaccharide (LPS) des parois bactériennes et la flagelline provenant des flagelles bactériens. Ils ont mesuré la libération d’IL‑8, une protéine de signalisation qui attire les cellules immunitaires et sert de marqueur général d’inflammation, et ont utilisé une analyse protéique à grande échelle pour observer comment le fonctionnement interne des cellules intestinales évoluait. De manière surprenante, les bactéries vivantes ou tuées n’ont pas fortement augmenté l’IL‑8 dans ce système, même après 24 heures. En revanche, la flagelline et surtout la combinaison flagelline + LPS ont déclenché une hausse nette d’IL‑8 en seulement trois heures, montrant que ces signaux purifiés pouvaient activer de façon fiable un état inflammatoire.
Trouver le dispositif le plus réaliste et efficace
Pour mieux reproduire la biologie intestinale réelle, l’équipe a ensuite tenu compte du lieu d’action naturel de chaque signal. Le LPS est généralement perçu du côté de la muqueuse orienté vers la lumière intestinale, tandis que la flagelline est principalement détectée du côté tissulaire. En utilisant des doses beaucoup plus faibles et plus physiologiques que dans des expériences antérieures, ils ont appliqué le LPS sur la face supérieure (côté lumière) et la flagelline sur la face inférieure (côté sanguin) de la feuille d’organoïde. Ce simple ajustement a produit une réponse forte et étendue en trois heures : de multiples messagers inflammatoires—dont IL‑8, TNF et plusieurs chimiokines—ont été sécrétés depuis les deux faces du tissu. Parallèlement, des centaines de protéines cellulaires ont vu leur abondance modifiée, indiquant une activation à grande échelle des voies de défense.
Inflammation, freins et réparation dans le même modèle
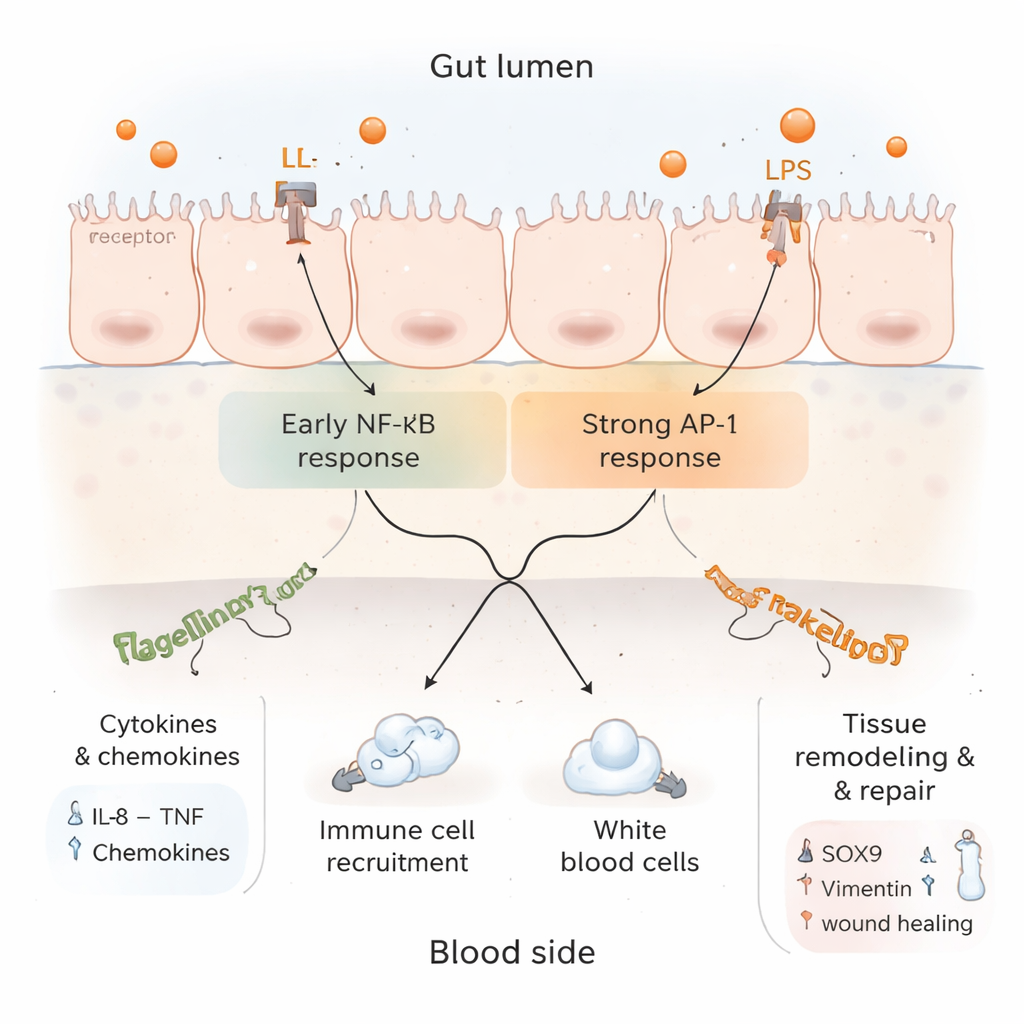
En approfondissant l’analyse protéique, les chercheurs ont dégagé un tableau complexe. D’un côté, des marqueurs d’inflammation active et de recrutement de cellules immunitaires ont été renforcés, et des voies de signalisation liées au TNF et à l’IL‑17—toutes deux centrales pour la défense intestinale—ont été activées. De l’autre, plusieurs composants de la voie classique NF‑κB, qui pilote de nombreux gènes inflammatoires, ont été atténués, tandis qu’une voie alternative impliquant AP‑1 restait active. Cela suggère qu’après l’alerte initiale, le tissu commence à appliquer des freins pour éviter des dommages incontrôlés. En même temps, des protéines associées à la régénération tissulaire, au remodelage structural et à la mort cellulaire contrôlée ont augmenté, laissant entendre que la muqueuse n’était pas seulement enflammée mais cherchait aussi à se remodeler et à se réparer.
Ce que cela signifie pour les traitements à venir
En comparant systématiquement différents stimuli microbiens, doses, positions et durées d’exposition, les auteurs concluent qu’une exposition de trois heures à de faibles doses de LPS sur la face intestinale combinée à de la flagelline sur la face sanguine est la manière la plus robuste et reproductible d’induire l’inflammation dans des organoïdes intestinaux dérivés de prématurés. Ce modèle affiné capture non seulement l’emballement inflammatoire, mais aussi les dispositifs de régulation, les mécanismes de tolérance et les réponses de réparation propres à l’intestin prématuré fragile. Il fournit une feuille de route pratique pour d’autres laboratoires souhaitant étudier comment des microbes spécifiques, des médicaments ou des facteurs nutritionnels peuvent aggraver ou calmer l’inflammation intestinale chez les tout‑petits très prématurés—une étape essentielle vers des stratégies ciblées et plus sûres pour prévenir des maladies intestinales dévastatrices dans ce groupe vulnérable.
Citation: Chapman, J.A., Frey, A.M., Dueñas, M.E. et al. Optimising the induction of inflammation within preterm infant-derived intestinal epithelial organoids. npj Gut Liver 3, 5 (2026). https://doi.org/10.1038/s44355-026-00054-2
Mots-clés: intestin de nourrisson prématuré, organoïdes intestinaux, inflammation intestinale, microbiome, entérocolite nécrosante