Clear Sky Science · fr
Transduction chimio-mécanique hors d’équilibre du dépliage de protéines entraîné par l’ATP dans le protéasome 26S
Comment une minuscule machine maintient l’ordre de nos protéines
À l’intérieur de chaque cellule, un broyeur microscopique appelé protéasome 26S détruit en permanence les protéines endommagées ou devenues inutiles, maintenant ainsi la cellule en bonne santé. Au cœur de cette machine se trouve un moteur en forme d’anneau qui consomme du carburant chimique (ATP) pour saisir, déplier et tirer les protéines vers une chambre centrale où elles sont découpées. Cet article utilise des simulations informatiques avancées pour révéler comment ce moteur convertit l’énergie chimique en mouvement mécanique, offrant un portrait détaillé et quantitatif d’un processus qui sous-tend le vieillissement, les maladies cérébrales, l’immunité et le cancer.
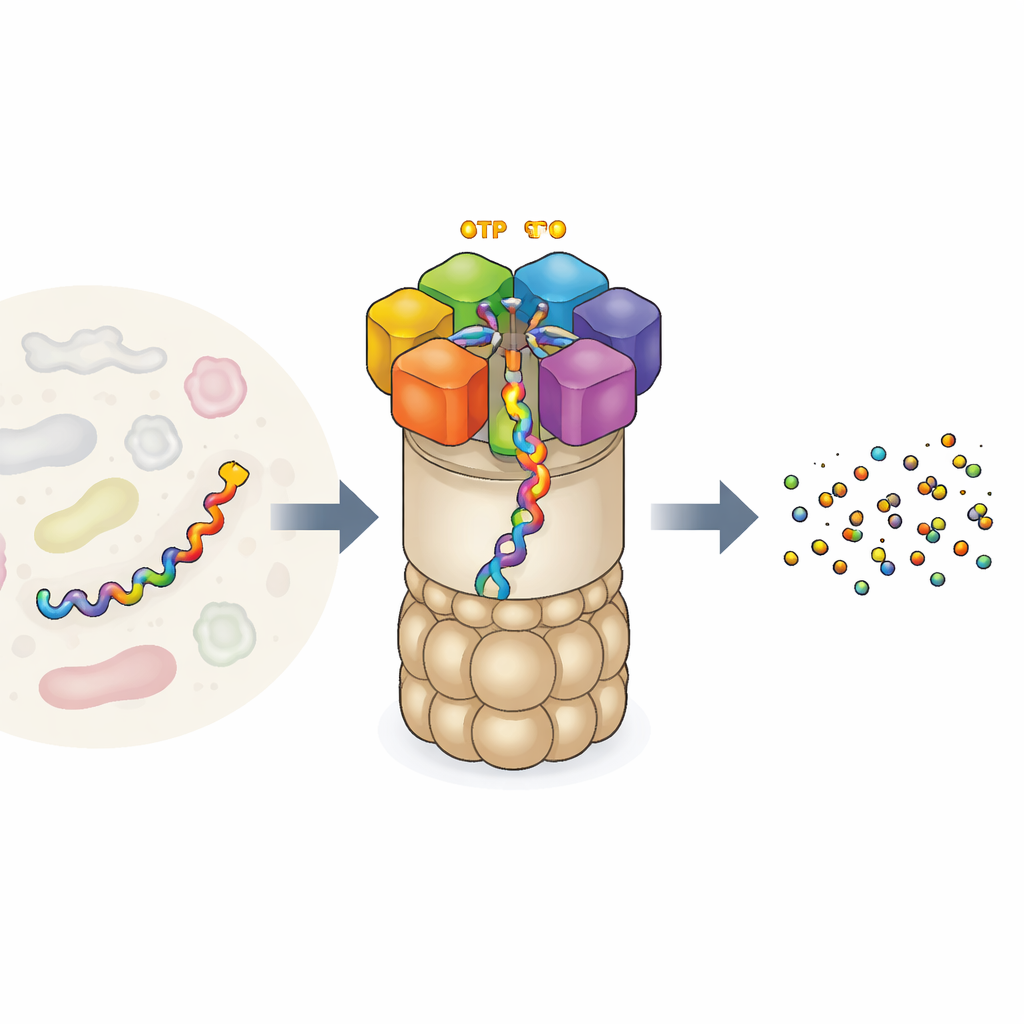
L’usine de recyclage des protéines de la cellule
Le protéasome 26S est l’une des machines protéiques les plus grandes et les plus complexes de nos cellules. Il se compose d’un noyau en forme de baril qui coupe les protéines et d’un capuchon régulateur qui reconnaît les protéines à détruire. À la porte se trouve un anneau de six unités motrices distinctes. Chaque unité peut lier l’ATP, la monnaie énergétique universelle de la cellule, et utilise cette énergie pour agripper une chaîne protéique et la tirer dans le noyau pour la dégradation. Ce moteur n’agit pas au hasard : des expériences antérieures suggéraient que les six unités fonctionnent de manière coordonnée, « main par main », passant la protéine comme des alpinistes sur une corde. Mais les expériences ne fournissaient que quelques instantanés de cette action, laissant des questions ouvertes sur la séquence complète des mouvements et sur la manière exacte dont la combustion du carburant est liée au travail mécanique.
Simuler une partie de tir à la corde moléculaire
Les auteurs ont construit un modèle informatique probabiliste qui traite le moteur comme un système sautant entre de nombreuses conformations possibles tandis que des molécules d’ATP et leurs produits se lient et se détachent. Ils ont défini 30 conformations principales de l’anneau où une, deux ou trois sous-unités motrices perdent leur prise sur la protéine, plus un état spécial étroitement fermé dans lequel les six tiennent la chaîne. À l’aide d’un algorithme standard pour simuler des événements chimiques aléatoires, ils ont suivi des centaines de milliers d’étapes où se produisent la fixation de l’ATP, sa rupture et les changements de conformation du moteur. À partir de ces simulations, ils ont pu prédire la vitesse à laquelle une protéine est tirée selon différentes conditions, comme des concentrations variables d’ATP, de son produit ADP, et d’un analogue d’ATP non hydrolysable souvent utilisé en expérimentation.
Quand trop de carburant ralentit le moteur
Les simulations ont reproduit plusieurs résultats expérimentaux surprenants. Lorsque le taux d’ATP augmente à partir de faibles valeurs, le moteur tire les protéines plus vite, car la fixation du carburant est l’étape la plus lente. Mais au‑delà d’environ 1 millimolaire d’ATP, la vitesse atteint un pic puis diminue : l’anneau passe plus de temps dans une conformation bloquée, non transloquante, où les six sous‑unités sont occupées par l’ATP alors que la protéine ne progresse pas. L’ajout d’ADP ou de l’analogue non hydrolysable d’ATP ralentit le moteur de manière continue, car ces molécules entrent en compétition avec l’ATP pour les poches de liaison mais ne peuvent pas accomplir le plein mouvement moteur. Le modèle prédit aussi le comportement du moteur face à des régions très fortement repliées d’une protéine, qui font office d’obstacles. Dans ces cas, le moteur passe plus de temps à lutter contre la résistance, et le taux global de dégradation diminue, correspondant aux mesures réalisées avec des domaines protéiques artificiellement stabilisés.
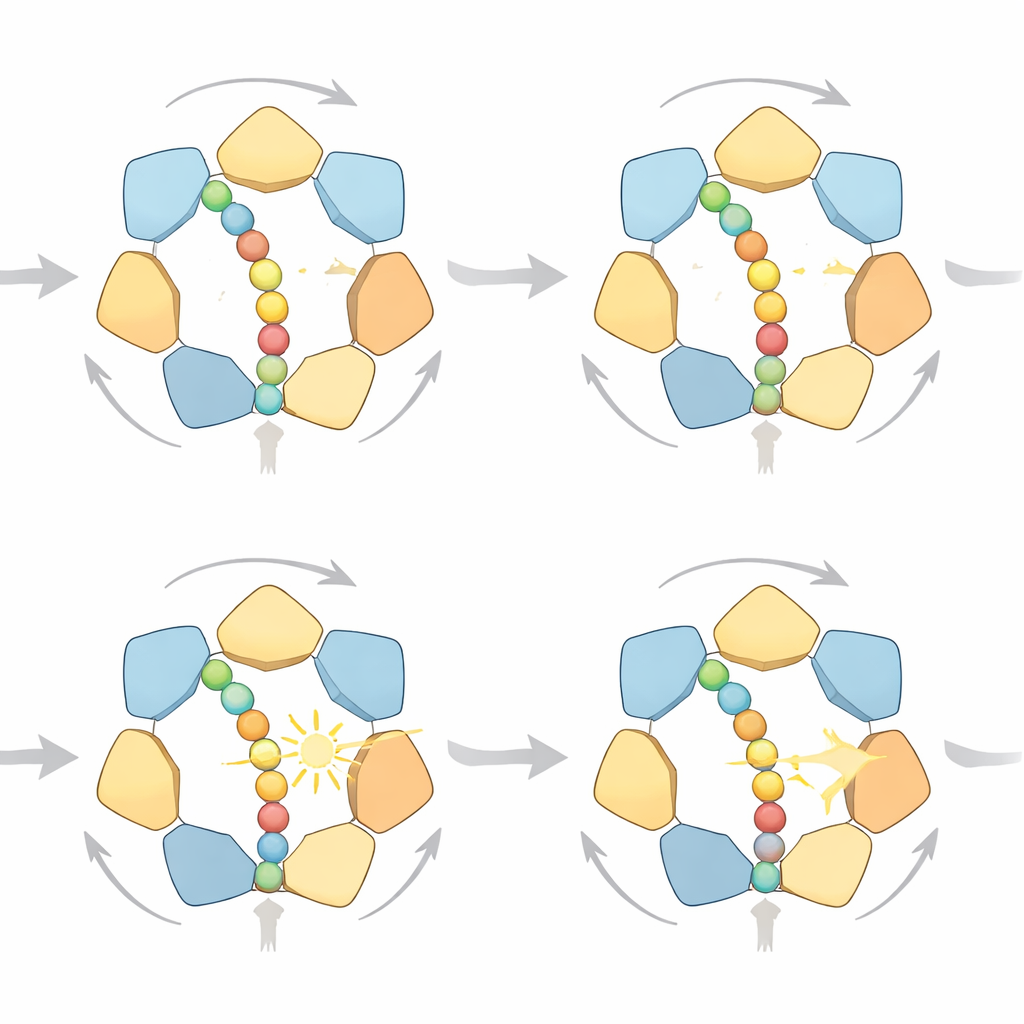
Plusieurs manières de faire un pas
En examinant en détail les trajectoires simulées, les chercheurs ont observé que l’anneau ne suit pas un cycle unique et rigide. Il existe plutôt plusieurs voies à forte probabilité qui respectent toutes la même règle directionnelle « main par main » : les sous‑unités proches de la sortie de l’anneau relâchent la protéine après la rupture de l’ATP, montent en haut d’un escalier en spirale de sous‑unités, puis reprennent la chaîne plus haut. Parfois la protéine avance d’un petit pas, parfois de deux, selon le nombre de sous‑unités qui lâchent prise ensemble. En présence d’abondant carburant, les mouvements d’un pas dominent car ils dissipent moins d’énergie contre les forces opposées ; lorsque le carburant est rare, le modèle prédit des sauts de deux pas plus fréquents. Les simulations relient aussi la charge mécanique à l’état chimique du moteur : à mesure que la résistance augmente et que la protéine cale, l’ADP tend à s’accumuler dans davantage des six poches de liaison — exactement ce que révèlent des études structurales à haute résolution.
Utilisation d’énergie et règles de conception partagées
Le modèle permet aux auteurs de cartographier comment l’énergie du moteur augmente lors de l’hydrolyse de l’ATP et diminue quand cette énergie est convertie en mouvement. Ils calculent une courbe d’efficacité montrant que le moteur fonctionne au mieux à une force opposée intermédiaire : trop peu de résistance et il brûle l’ATP de manière gaspilleuse ; trop de résistance et il freine presque jusqu’à l’arrêt. Lorsque l’équipe a comparé ses prédictions aux données d’autres machines destructrices de protéines chez les bactéries et les levures, elle a trouvé des tendances très similaires quant à la façon dont un analogue non hydrolysable de l’ATP ralentit ces moteurs. Cela suggère que de nombreux membres de cette famille d’enzymes en anneau partagent probablement un mécanisme commun et conservé pour tirer sur les protéines.
Pourquoi c’est important pour la santé et la maladie
En intégrant des instantanés structuraux et des mesures biochimiques dispersés dans un cadre unique et testable, ce travail montre de manière quantitative comment un minuscule moteur moléculaire transforme le carburant chimique en force pour recycler les protéines cellulaires. Le modèle n’explique pas seulement une large gamme d’expériences existantes, il fait aussi des prédictions sur la façon dont des variations du niveau de carburant, de la charge mécanique ou des mutations du moteur pourraient modifier la destruction des protéines. Parce que des machines similaires opèrent chez tous les êtres vivants et sont centrales dans des affections allant des neurodégénérescences au cancer, comprendre leur fonctionnement à ce niveau pourrait ultimement orienter la conception de médicaments qui règlent, stimulent ou bloquent sélectivement ces broyeurs microscopiques.
Citation: Wu, D., Ouyang, Q., Wang, H. et al. Nonequilibrium chemomechanical transduction of ATP-driven protein unfolding in the 26S proteasome. npj Biol. Phys. Mech. 3, 4 (2026). https://doi.org/10.1038/s44341-026-00034-w
Mots-clés: protéasome, moteur AAA+ ATPase, dégradation des protéines, machines moléculaires, couplage chimio‑mécanique