Clear Sky Science · fr
Détection protéique non enzymatique ultrasensible utilisant un immunodosage de proximité avec microscopie par résonateur photonique d’absorption
Pourquoi détecter des traces infimes de protéines est important
Médecins et chercheurs s’appuient de plus en plus sur les protéines sanguines pour signaler un cancer, une maladie cardiaque, une infection ou une inflammation nocive bien avant que les symptômes ne deviennent graves. Mais beaucoup de ces signaux moléculaires apparaissent à des niveaux extrêmement faibles que les tests de laboratoire standard peinent aujourd’hui à détecter rapidement ou à moindre coût. Cette étude présente une nouvelle méthode de test, appelée PINATA, capable de repérer des quantités extrêmement faibles d’une protéine liée à l’inflammation en utilisant du matériel simple et des étapes à température ambiante, ouvrant la voie à des diagnostics plus accessibles et plus sensibles.
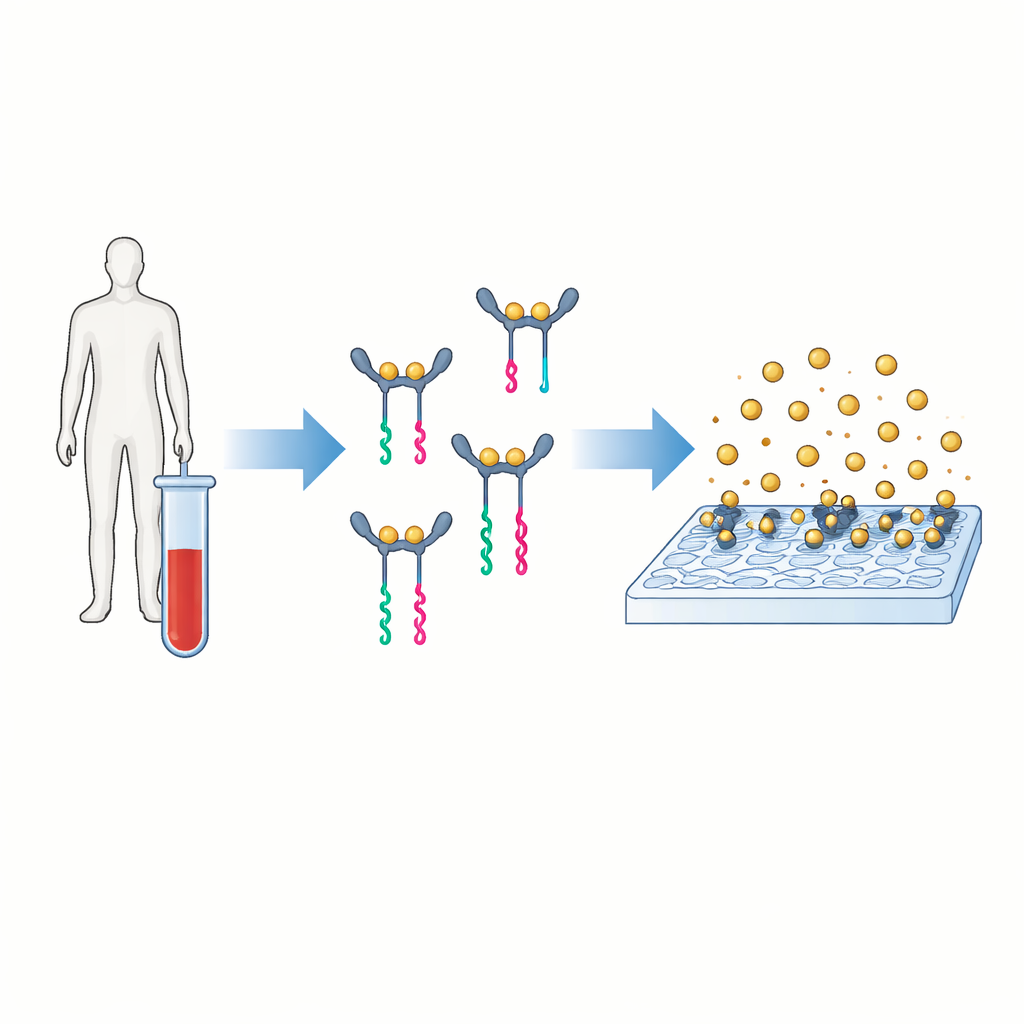
Une nouvelle manière de transformer les protéines en signaux lisibles
L’idée centrale de PINATA est de traduire la présence d’une protéine en un court fragment d’ADN facile à amplifier et à compter. Les auteurs se concentrent sur l’interleukine-6, une molécule de signalisation sanguine qui augmente dans des contextes allant de l’infection au cancer. Dans les tests conventionnels, deux anticorps se fixent sur la protéine et portent une enzyme qui génère un signal coloré ou fluorescent. PINATA conserve la notion de base des deux anticorps reconnaissant la même protéine, mais au lieu d’enzymes, elle attache de courts brins d’ADN à chaque anticorps. Lorsque les deux anticorps se lient à la même protéine et se rapprochent, leurs brins d’ADN associés coopèrent pour libérer un fragment d’ADN séparé appelé rapporteur. Chaque molécule de protéine peut ainsi déclencher la libération de nombreux rapporteurs d’ADN identiques.
Utiliser des « règles de circulation » de l’ADN au lieu d’enzymes
Au cœur de la méthode se trouvent des circuits d’ADN soigneusement conçus qui se comportent comme des systèmes de circulation moléculaire, déterminant quand des brins peuvent se lier, se délier ou échanger des partenaires. Ces circuits sont construits de sorte que, à moins qu’une protéine rapproche les deux morceaux d’ADN liés aux anticorps, l’ADN rapporteur reste verrouillé et aucun signal n’est généré. Quand la protéine est présente, son action de passerelle libère le rapporteur. Ce rapporteur libéré participe ensuite à un processus d’amplification secondaire sur une surface préparée. Là, il s’engage à plusieurs reprises dans des réactions d’échange de brins qui permettent à une seule molécule rapporteur de recruter de nombreuses nanoparticules d’or à la surface, créant un signal numérique fort sans utiliser d’enzymes ni de cycles de température.
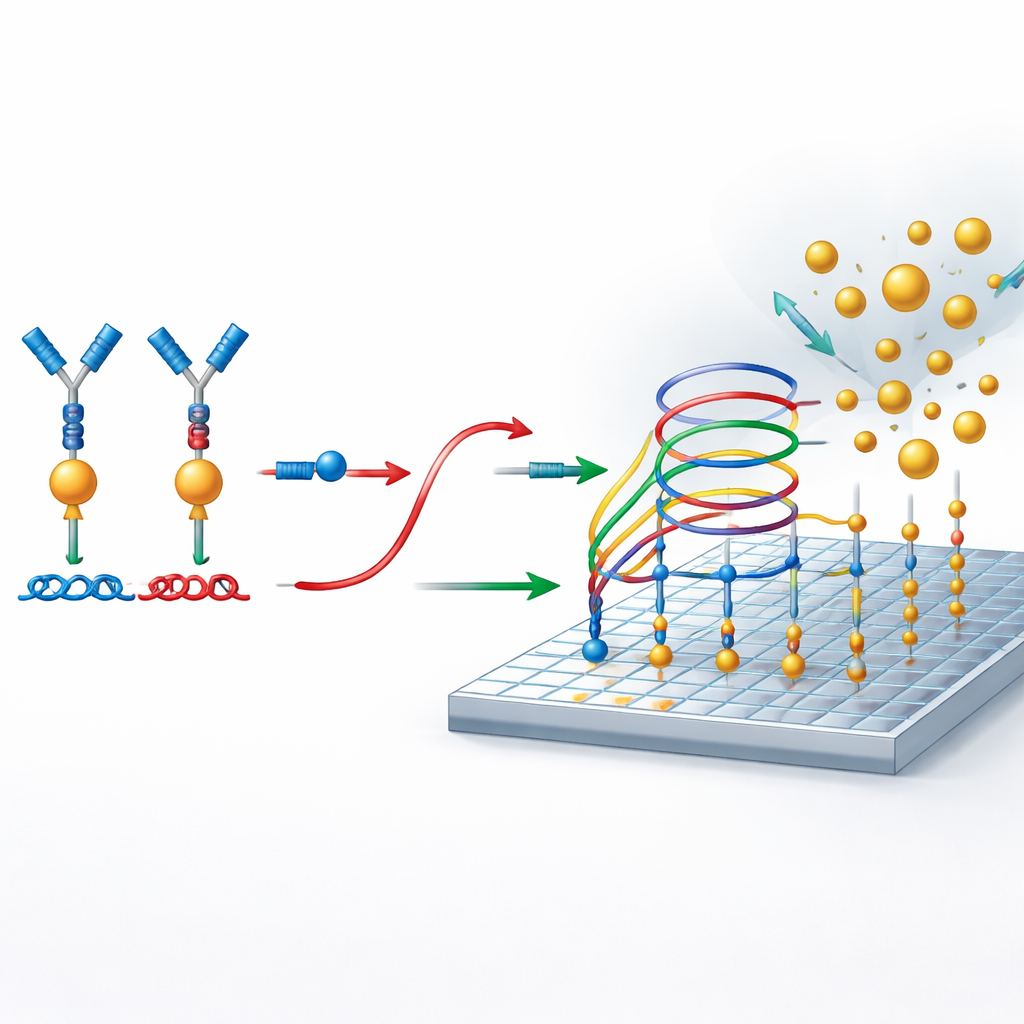
Compter des nanoparticules uniques comme des événements oui/non
Pour lire le résultat, les chercheurs utilisent la microscopie par résonateur photonique d’absorption, ou PRAM. La surface de détection est un matériau spécialement structuré qui réfléchit fortement la lumière à une couleur particulière. Lorsque des nanoparticules d’or se déposent sur cette surface, elles absorbent cette lumière et apparaissent comme des points sombres dans l’image au microscope. Parce que le système est conçu pour que les nanoparticules ne se lient que lorsque l’ADN rapporteur est présent, chaque point sombre représente un événement de détection réussi lié à une molécule de protéine. Un montage optique simple et peu coûteux et un logiciel de traitement d’image sont ensuite utilisés pour compter ces points à travers la surface, transformant le nombre de nanoparticules en une mesure précise de la concentration protéique.
Quelle est la sensibilité et la sélectivité du test ?
Avec cette approche, l’équipe montre qu’elle peut détecter l’interleukine‑6 à des niveaux aussi bas que 37 femtogrammes par millilitre — soit à peu près quelques dizaines de molécules dans une goutte — sur une plage dynamique couvrant six ordres de grandeur. Le dosage fonctionne selon un protocole simple en deux étapes de 90 minutes effectué entièrement à température ambiante. Les auteurs démontrent également que le test reste précis même lorsque l’interleukine‑6 est mélangée à des échantillons complexes comme le sérum et le plasma humains, qui interfèrent typiquement avec des mesures sensibles. Ils confirment en outre que les anticorps ciblant l’interleukine‑6 ne répondent pas à d’autres protéines apparentées, soulignant la sélectivité de l’essai.
Ce que cela pourrait signifier pour les diagnostics futurs
Pour un non‑spécialiste, la conclusion principale est que PINATA offre un moyen de détecter des protéines liées à des maladies à des niveaux extrêmement bas en utilisant un instrument optique compact plutôt que des appareils de laboratoire volumineux et coûteux. En combinant des circuits d’ADN intelligents avec le comptage numérique de nanoparticules, la méthode évite des enzymes fragiles et des étapes de chauffage, tout en atteignant ou en dépassant la sensibilité de nombreux tests protéiques avancés. Avec un développement supplémentaire et une adaptation à d’autres cibles, cette stratégie pourrait permettre des diagnostics plus précoces, un suivi plus fréquent et des tests au point de soins pour un large éventail de pathologies où de faibles variations des taux protéiques ont une forte signification clinique.
Citation: Shepherd, S., Bhaskar, S., Xu, H. et al. Ultrasensitive non-enzymatic protein detection using proximity immunoassay with photonic resonator absorption microscopy. npj Biosensing 3, 21 (2026). https://doi.org/10.1038/s44328-026-00090-1
Mots-clés: détection de biomarqueurs protéiques, diagnostics ultrasensibles, déplacement de brins d’ADN, dosage de l’interleukine-6, biosurveillance numérique