Clear Sky Science · fr
Nanoparticules microfluidiques isolant magnétiquement des vésicules extracellulaires dérivées de neurones et d’astrocytes pour différencier la maladie à corps de Lewy et la maladie d’Alzheimer
Pourquoi cela compte pour les familles et les médecins
La démence est un terme parapluie qui recouvre plusieurs maladies cérébrales aux symptômes similaires mais aux causes sous-jacentes très différentes. Deux des plus fréquentes, la maladie d’Alzheimer et la maladie à corps de Lewy, peuvent se présenter presque de la même façon en consultation, pourtant elles réagissent différemment aux traitements et comportent des risques distincts. Aujourd’hui, la seule manière de savoir avec certitude quelle maladie une personne avait est d’examiner le cerveau après le décès. Cette étude décrit un nouveau type de test sanguin qui lit de minuscules messages libérés par les cellules cérébrales, dans le but de distinguer ces deux démences alors que les patients sont encore vivants.
De minuscules colis voyageant du cerveau vers le sang
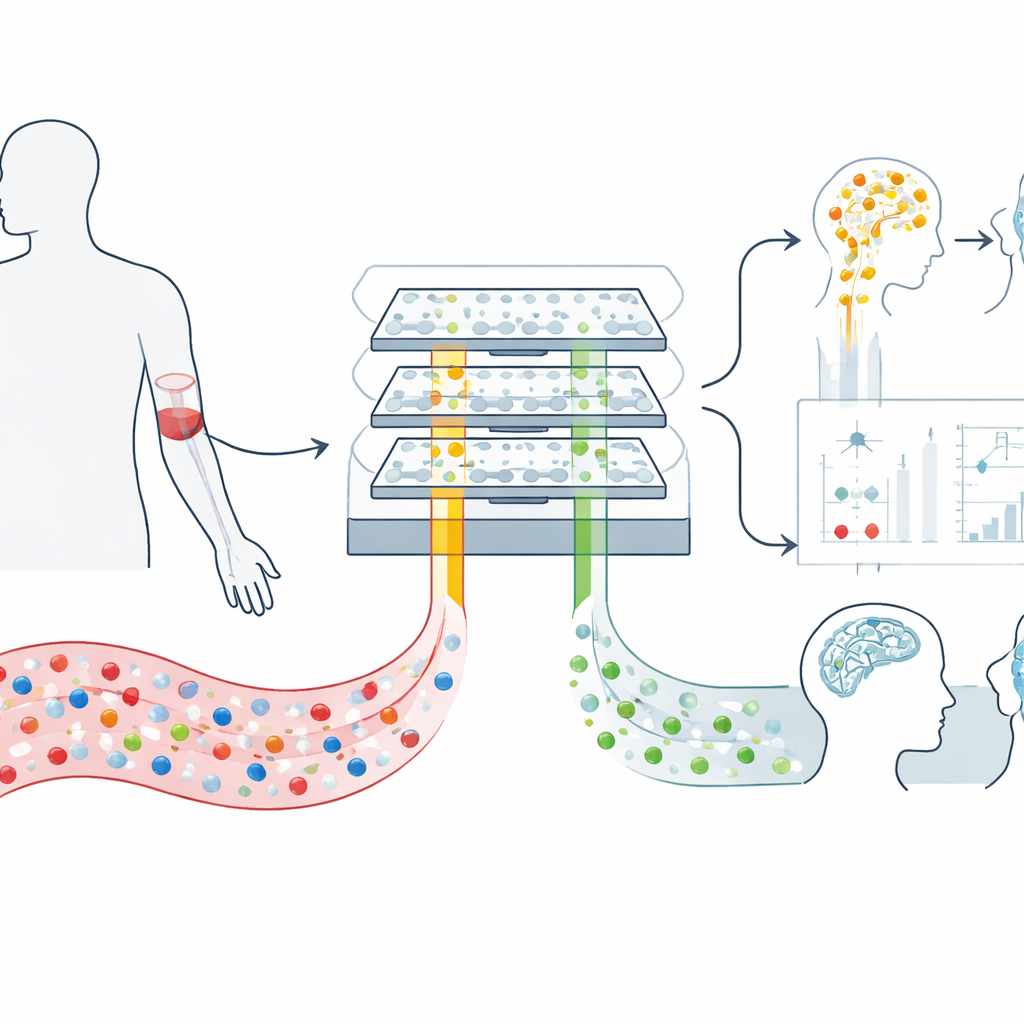
Notre cerveau libère en continu dans la circulation sanguine des bulles microscopiques appelées vésicules extracellulaires. Ces vésicules sont comme des enveloppes matelassées envoyées par les neurones et leurs cellules de soutien, transportant des fragments d’acides nucléiques et des protéines qui reflètent ce qui se passe à l’intérieur du cerveau. Parce qu’elles peuvent traverser la barrière hémato‑encéphalique et survivre dans la circulation, elles offrent une fenêtre rare et peu invasive sur la biologie cérébrale. Le défi vient du fait qu’un millilitre de sang contient des centaines de milliards de vésicules provenant de tout le corps, si bien que celles d’origine cérébrale sont largement minoritaires et difficiles à isoler avec les méthodes de laboratoire classiques.
Une puce magnétique qui trie les signaux du cerveau
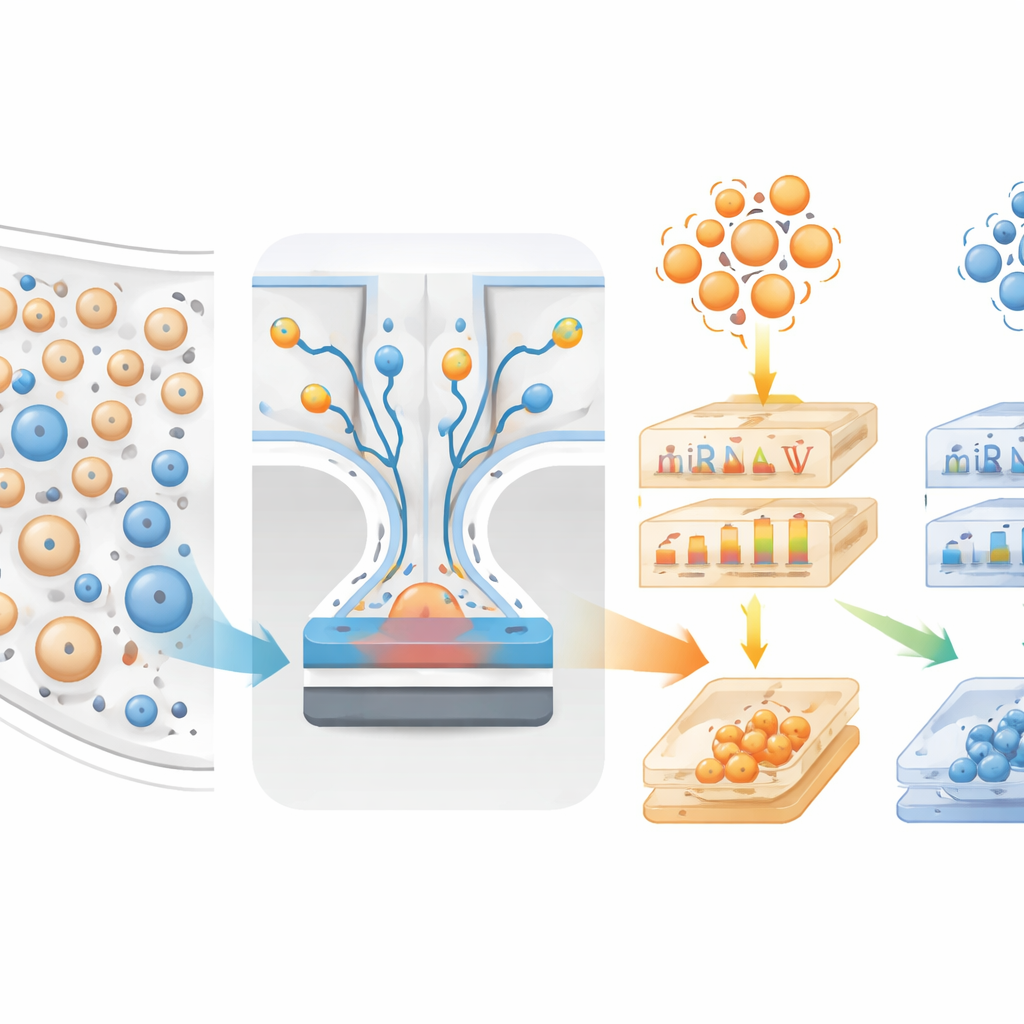
Pour répondre à cette difficulté, les chercheurs ont conçu un dispositif microfluidique appelé mTENPO qui combine une puce de la taille d’une carte et un aimant puissant. Avant que l’échantillon de sang n’entre dans la puce, les vésicules sont marquées par des nanoparticules magnétiques via des anticorps qui se lient à des protéines de surface typiquement présentes sur les vésicules neuronales (GluR2) ou astrocytaires (GLAST). Lorsque le mélange marqué circule à travers des millions de minuscules pores dans la puce, le champ magnétique attire les vésicules cérébrales fortement marquées vers les parois des pores, les retenant tandis que le reste s’écoule. De cette manière, l’équipe peut enrichir indépendamment deux populations de vésicules — principalement d’origine neuronale et principalement d’origine astrocytaire — directement à partir d’un petit échantillon de plasma.
Lire les empreintes moléculaires
À partir de 137 volontaires dont le diagnostic cérébral a été confirmé post‑mortem, l’équipe a isolé ces deux types de vésicules et a aussi mesuré des protéines plasmatiques classiques liées à la maladie d’Alzheimer, comme différentes formes de bêta‑amyloïde et de tau. Ils ont ensuite séquencé de courts ARN régulateurs (miARN) présents dans les vésicules et recherché lesquels différaient entre des personnes atteintes de maladie à corps de Lewy pure, d’Alzheimer pure, de pathologies mixtes ou sans démence. Plusieurs miARN portés par les vésicules d’origine neuronale et astrocytaire, ainsi que plusieurs protéines tau liées dans le plasma, ont montré des profils distincts entre les groupes Lewy et Alzheimer. Lorsque les chercheurs ont cartographié les gènes ciblés par ces miARN, ils ont trouvé des liens solides avec des voies impliquées dans la survie cellulaire, l’inflammation et la gestion des protéines — des processus déjà impliqués dans la neurodégénérescence.
Construire un test sanguin combiné puissant
Parce qu’aucun marqueur unique ne séparait clairement les maladies, l’équipe a utilisé des outils d’apprentissage automatique pour assembler un panel compact des signaux les plus informatifs puisés dans les trois compartiments : vésicules neuronales, vésicules astrocytaires et protéines sanguines. Le panel final de 15 caractéristiques comprenait 14 miARN spécifiques des vésicules ainsi que deux formes phosphorylées de la protéine tau. Testé avec une validation croisée répétée pour limiter le surapprentissage, ce panel multi‑marqueurs a distingué la maladie à corps de Lewy de la maladie d’Alzheimer avec environ 95 % de précision et une aire sous la courbe de 0,96 — bien supérieure à celle de n’importe quelle mesure prise isolément. Les personnes dont le cerveau présentait des mélanges de pathologies avaient tendance à montrer des niveaux de marqueurs intermédiaires, ce qui suggère que de tels panels pourraient un jour aider à reconnaître les maladies mixtes plutôt que d’imposer une étiquette binaire.
Du proof of concept à l’usage clinique futur
Cette étude constitue une démonstration précoce mais importante que les vésicules de cellules cérébrales présentes dans le sang peuvent porter suffisamment d’informations détaillées pour séparer les principaux types de démence. Le travail doit encore être confirmé sur des cohortes plus larges et diversifiées et chez des patients suivis longitudinalement, et les auteurs soulignent les limites actuelles pour identifier avec précision la cellule d’origine de chaque vésicule. Néanmoins, la combinaison d’une puce magnétique évolutive et d’un panel multimarqueurs soigneusement choisi offre une feuille de route pour de futurs tests sanguins susceptibles d’orienter les choix thérapeutiques, d’améliorer les essais cliniques et de fournir aux familles des réponses beaucoup plus claires sur la maladie spécifique à l’origine de la démence d’un proche.
Citation: Yang, S.J., Lin, A.A., Shen, H. et al. Microfluidic nanomagnetically isolated neuron- and astrocyte-derived extracellular vesicles to differentiate Lewy body and Alzheimer’s disease. npj Biosensing 3, 19 (2026). https://doi.org/10.1038/s44328-026-00086-x
Mots-clés: vésicules extracellulaires, maladie à corps de Lewy, maladie d’Alzheimer, biomarqueurs sanguins, diagnostic microfluidique