Clear Sky Science · fr
Détection multiplexée au point de soin des cytokines à l’aide d’un réseau d’électrodes HexaPie pour l’endotypage de l’asthme
Pourquoi tester l’asthme avec la salive pourrait changer les soins à domicile
L’asthme touche des centaines de millions de personnes, et pourtant les médecins peinent encore à associer chaque patient au traitement le plus adapté. Cette étude présente un petit capteur électronique, nommé HexaPie, qui lit des signaux immunitaires à partir d’un simple échantillon de salive au lieu du sang. En mesurant simultanément plusieurs molécules liées à l’inflammation, il pourrait un jour permettre aux personnes de surveiller leur asthme — et d’autres troubles immunitaires — rapidement et sans douleur, à domicile ou en cabinet. 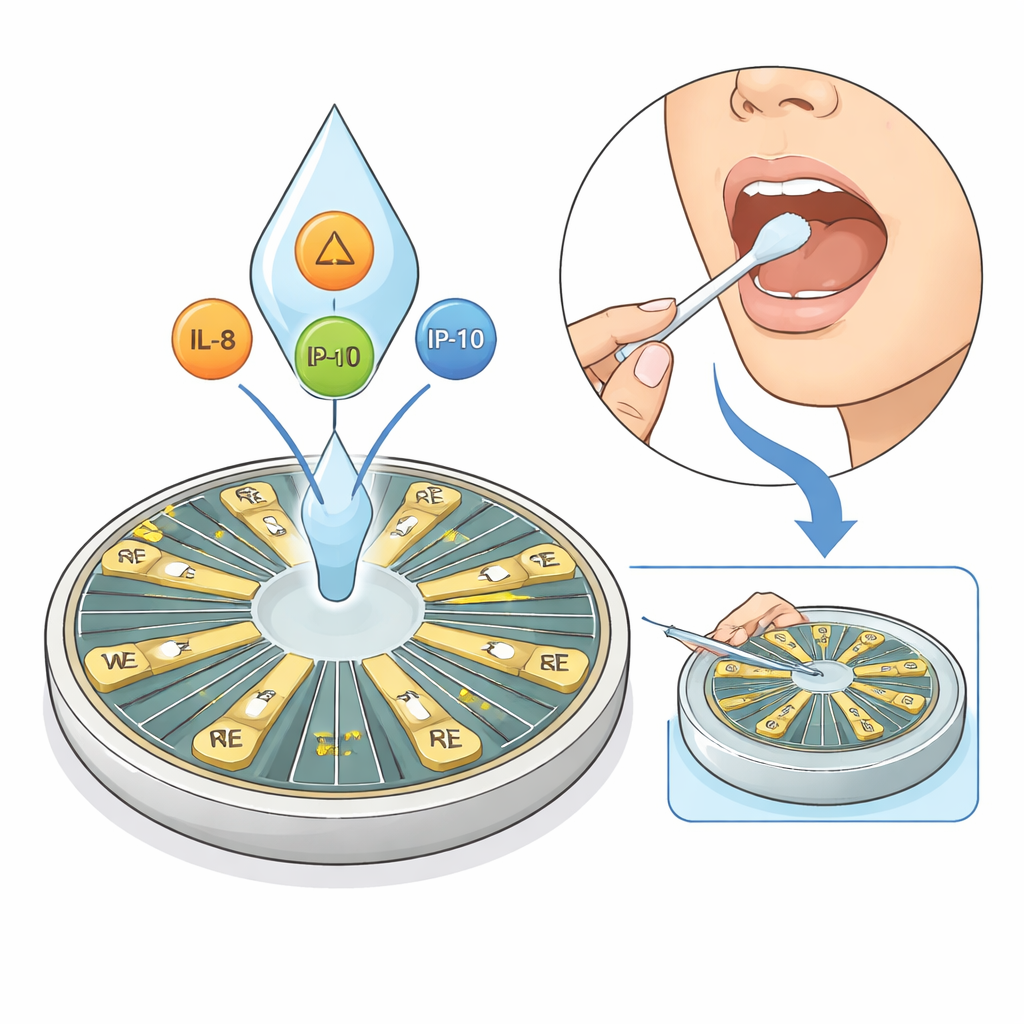
Une nouvelle façon d’écouter le système immunitaire
L’asthme n’est pas une maladie unique mais un ensemble de « types » différents, pilotés par des voies immunitaires distinctes. Les tests classiques se concentrent souvent sur un marqueur à la fois et exigent généralement des prises de sang et des appareils centralisés en laboratoire, ce qui est lent et peu pratique pour des contrôles fréquents. Le système HexaPie vise à résoudre ce problème en détectant trois médiateurs immunitaires clés dans la salive — IL‑8, IL‑10 et IP‑10 — qui ensemble dessinent une image plus large de l’inflammation des voies respiratoires, y compris des formes non éosinophiliques difficiles à traiter. Comme la collecte de salive est non invasive et simple, elle se prête bien à une surveillance répétée en dehors des grands hôpitaux.
Une minuscule matrice d’or qui détecte sans réactifs supplémentaires
HexaPie repose sur un circuit imprimé personnalisé qui porte six paires de minuscules électrodes en or disposées comme des parts d’une tarte. Chaque électrode de travail est recouverte d’un anticorps différent qui se fixe spécifiquement sur l’une des cytokines cibles, tandis que l’électrode de référence associée reste nue. Plutôt que d’utiliser des colorants ou des produits rédox ajoutés, l’appareil s’appuie sur une méthode électrique sans marquage : lorsque les cytokines de la salive se lient à leurs anticorps, elles réarrangent subtilement les particules chargées et l’eau à la surface métallique. Cela modifie la double couche électrique — une région très mince à l’interface — et le changement d’impédance électrique résultant peut être lu directement, ce qui permet la mesure simultanée des trois cytokines à partir d’une seule petite goutte.
Tester la conception par simulations et en laboratoire
Avant de construire des dispositifs complets, l’équipe a utilisé des simulations informatiques pour vérifier que la géométrie HexaPie répartirait les champs électriques et les courants de manière contrôlée entre chaque électrode de travail et sa référence. Les modèles ont montré que la tension appliquée restait bien confinée près des zones sensibles et que le courant circulait principalement à travers les interstices prévus — des conditions nécessaires à des lectures stables et répétables. En laboratoire, les chercheurs ont ensuite vérifié la chimie sur électrodes d’or en ajoutant chaque couche — lien, anticorps et antigène — tout en suivant des signaux électrochimiques standards. Au fur et à mesure que la surface se chargeait en matériel biologique, le flux d’électrons ralentissait et l’impédance augmentait par étapes prévisibles, confirmant que les couches d’anticorps s’étaient correctement formées et pouvaient capturer leurs cibles. 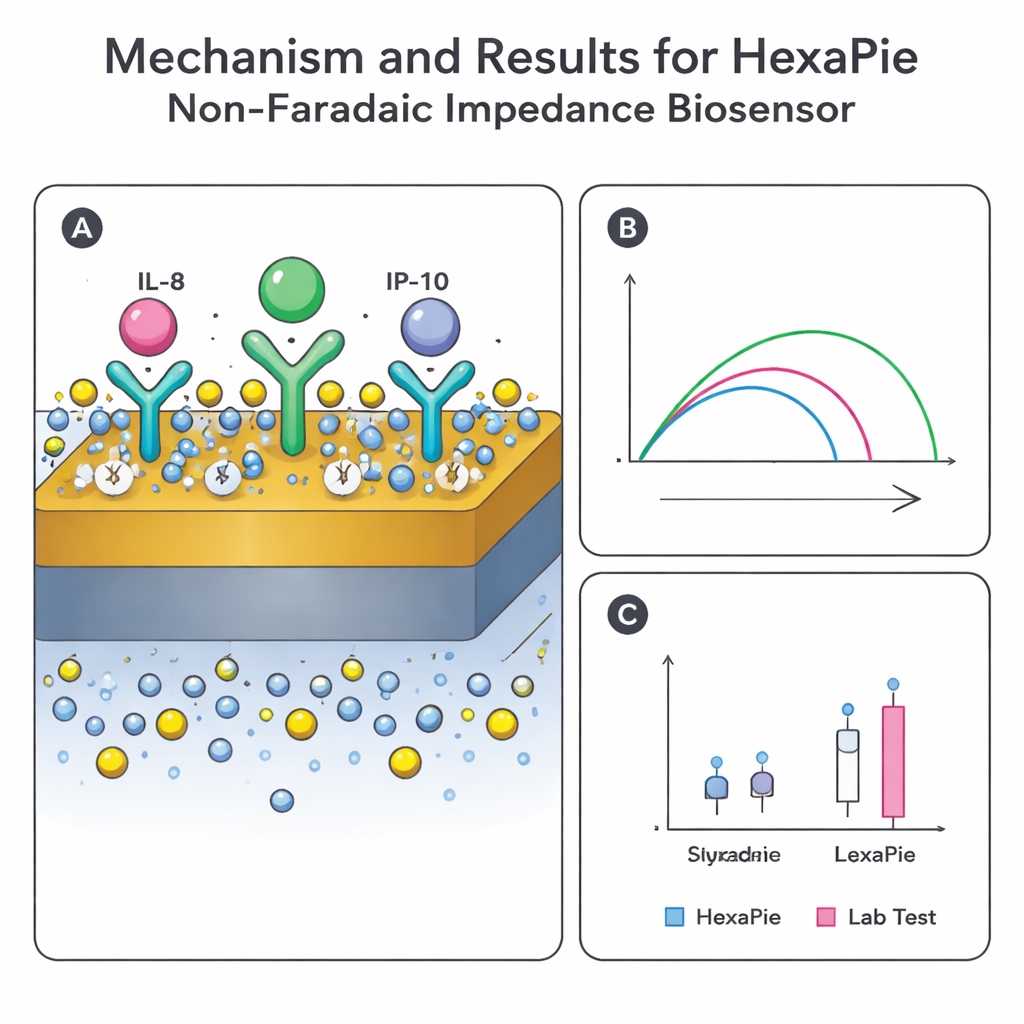
Performance du capteur sur des échantillons de salive réels
Pour vérifier si HexaPie pouvait fournir des valeurs fiables en pratique, les auteurs ont épicé des quantités connues des trois cytokines dans de la salive humaine mise en commun et ont mesuré les changements d’impédance résultants. Les signaux évoluaient de manière ordonnée et dépendante de la concentration, et en ajustant les données l’équipe a établi des courbes d’étalonnage qui convertissent les lectures électriques en niveaux de cytokines. L’appareil a atteint des limites de détection faibles — jusqu’à des trillionièmes de gramme par millilitre pour certains marqueurs — dans les plages rapportées chez les personnes ayant des voies respiratoires enflammées. Les mesures répétées sur la même puce et entre différentes puces variaient de moins de 15 %, respectant les normes cliniques acceptées. Quand les chercheurs ont ajouté des composants courants de la salive comme l’albumine, l’acide urique et la vitamine C à des niveaux élevés, les réponses du capteur ont à peine bougé, indiquant que des interférents quotidiens sont peu susceptibles de fausser les lectures.
Comparaison avec des tests de qualité hospitalière
Le test ultime a été la comparaison d’HexaPie avec des plateformes de laboratoire établies. Des échantillons de salive de personnes asthmatiques (pendant des exacerbations et en phase stable) et de témoins sains fumeurs et non‑fumeurs ont été analysés en parallèle avec HexaPie, un système d’immuno‑essai automatisé (ELLA) et un test multiplex à billes (Luminex). Bien que cette étude limitée n’ait pas révélé de différences nettes entre groupes dans les niveaux de cytokines — probablement en raison du calendrier et de la taille de l’échantillonnage — les valeurs du nouveau capteur pour IL‑8 et IP‑10 correspondaient étroitement à celles des deux méthodes de référence, avec seulement de faibles décalages moyens. L’IL‑10, naturellement peu abondante et difficile à mesurer, montrait plus de désaccord entre les plateformes, soulignant le défi plus large de détecter de manière fiable ces molécules de faible abondance dans la salive.
Ce que cela signifie pour les soins quotidiens
Pour les non‑spécialistes, la conclusion est qu’HexaPie apporte des mesures immunitaires de type laboratoire dans un dispositif compact, sans réactifs, qui fonctionne directement sur la salive. Il suit de façon fiable les augmentations cliniquement significatives de trois cytokines liées à l’asthme sans étiquettes ni manipulation d’échantillons complexe, et ses lectures concordent bien avec les tests de référence pour deux d’entre elles. Si des travaux supplémentaires sont nécessaires pour affiner la détection de l’IL‑10 et valider le système sur des cohortes plus larges, cette technologie ouvre la voie à un futur où les personnes asthmatiques et atteintes d’autres maladies inflammatoires pourraient surveiller leur statut immunitaire rapidement et sans douleur au point de soin, aidant les médecins à adapter les traitements au profil immunitaire unique de chaque patient.
Citation: Churcher, N.K.M., Rizvi, F.Z., Qureshi, A. et al. Point-of-care multiplexed detection of cytokines using a HexaPie electrode array for asthma endotyping. npj Biosensing 3, 16 (2026). https://doi.org/10.1038/s44328-026-00081-2
Mots-clés: surveillance de l’asthme, biosenseur salivaire, détection des cytokines, diagnostic au point de soin, impédance électrochimique