Clear Sky Science · fr
Bioessai amélioré par plasmons pour la détection et la quantification de l’ARN du SARS‑CoV‑2 sans amplification
Pourquoi des tests viraux plus rapides et plus simples sont importants
La pandémie de COVID‑19 a mis en lumière notre dépendance à des tests de laboratoire lents, coûteux et difficiles à déployer à grande échelle quand des millions de personnes ont besoin d’un résultat rapide. Le travail présenté ici propose un nouveau type de test de laboratoire capable de repérer et de compter de très faibles quantités de matériel génétique du coronavirus sans l’étape d’amplification habituellement utilisée en PCR. Cette approche vise à rapprocher la précision de niveau hospitalier de tests simples et peu onéreux qui pourraient être déployés plus largement lors de futures flambées épidémiques.
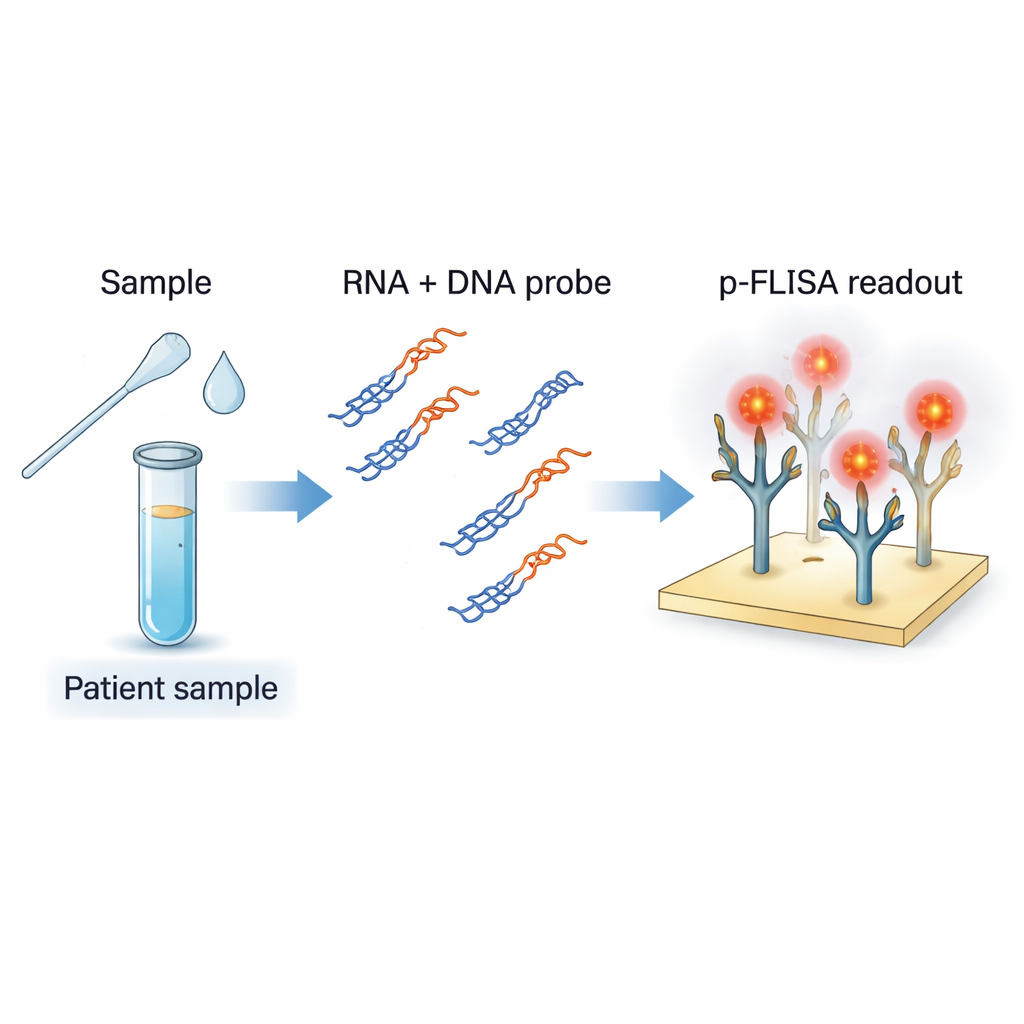
Une nouvelle manière de détecter les traces génétiques virales
Le diagnostic standard du COVID‑19 utilise la RT‑PCR, qui multiplie de nombreux exemplaires de fragments d’ARN viral pour pouvoir les détecter. Bien que très sensible, la PCR exige du matériel complexe, du personnel formé et du temps, et fournit généralement une réponse binaire plutôt qu’une charge virale précise. Les auteurs se sont donné pour objectif de concevoir un essai qui fonctionne davantage comme une version fortement améliorée d’un ELISA sanguin : un format simple sur plaque, mais réglé pour détecter directement l’ARN viral et quantifier la quantité présente. Leur méthode cible l’ARN du SARS‑CoV‑2 dans des échantillons tels que écouvillons nasaux et salive, mais est conçue pour pouvoir être facilement adaptée à d’autres virus à ARN.
Transformer l’ARN en cible capturable
L’équipe utilise de courtes séquences d’ADN conçues pour correspondre à des régions spécifiques du génome du SARS‑CoV‑2. Lorsqu’elles sont mélangées à l’ARN extrait d’un échantillon patient puis chauffées puis refroidies doucement, ces sondes d’ADN s’apparient à tout ARN viral complémentaire pour former des hybrides ADN–ARN, comme une petite fermeture éclair constituée d’un brin d’ARN et d’un brin d’ADN. Un anticorps spécial appelé S9.6 joue le rôle de capteur : il reconnaît et se lie fortement à ces hybrides, mais pas à l’ADN simple ou double brin ordinaire ni à l’ARN non apparié. En enrobant le fond d’une plaque de S9.6, l’essai capte sélectivement uniquement ces hybrides contenant les séquences virales d’intérêt, filtrant le reste du fouillis génétique de l’échantillon.
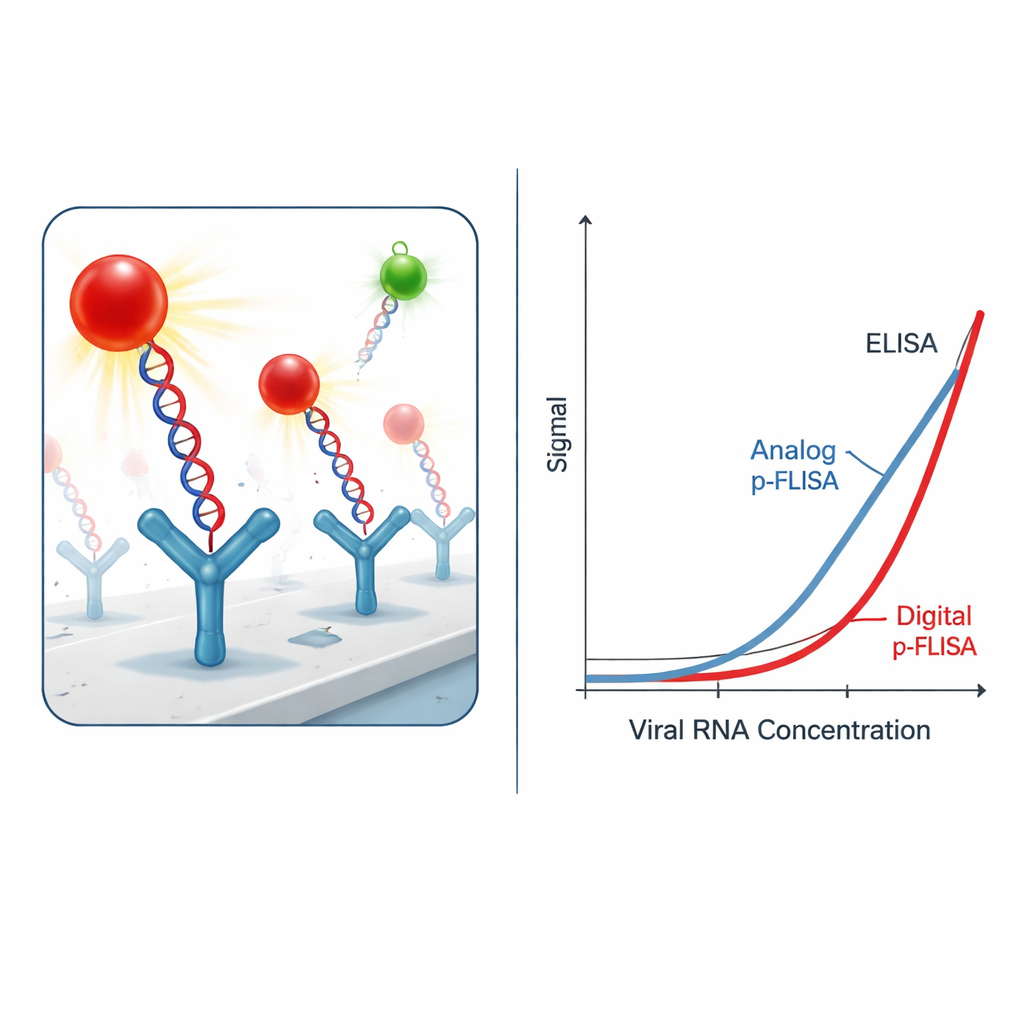
Rendre le signal ultra‑lumineux
Attraper les hybrides viraux ne suffit pas ; le défi est de les visualiser au‑dessus du bruit de fond. Au lieu des colorants fluorescents classiques, les chercheurs utilisent des nanomarqueurs « plasmoniques‑fluor » — des nanoparticules conçues pour agir comme de minuscules antennes pour la lumière. Chaque marqueur combine une nanobarrette métallique avec plusieurs molécules fluorescentes et un revêtement lui permettant de s’accrocher aux étiquettes biotine sur l’ADN ou l’anticorps. Ces marqueurs plasmoniques émettent une lumière plus de mille fois plus brillante que les colorants standards dans les mêmes conditions. En pratique, cela signifie qu’il faut beaucoup moins d’hybrides viraux pour produire une lueur détectable, améliorant drastiquement la sensibilité du test et abaissant la concentration minimale d’ARN viral mesurable.
De la lueur analogique au comptage numérique
Dans sa forme « analogique » la plus simple, l’essai mesure la luminosité globale de chaque puits de la plaque, à la manière d’un test fluorescent classique. Même dans ce mode, le système amélioré par plasmons améliore la limite de détection et le plus bas niveau quantifiable de l’ARN du SARS‑CoV‑2 d’un à trois ordres de grandeur par rapport à un ELISA traditionnel utilisant des enzymes ou des fluorophores standards. Les auteurs poussent ensuite l’idée plus loin en passant à un format « numérique » : plutôt que de moyenner la lumière sur tout le puits, ils image la surface avec un microscope à fluorescence et comptent individuellement les nanomarqueurs brillants à l’aide d’un logiciel d’analyse d’image sur mesure. Cette approche de comptage par particule unique apporte un gain supplémentaire en sensibilité d’un facteur dix à trente, conduisant globalement à des limites de détection environ 2 300 fois meilleures et à des limites de quantification 460 fois meilleures que l’ELISA.
Application du test à des échantillons réels
Pour vérifier la robustesse de la méthode en dehors d’assemblages contrôlés, les chercheurs ont testé de l’ARN extrait d’écouvillons nasaux et de salive de patients atteints de COVID‑19, y compris des infections par différentes variantes virales comme alpha/beta et delta, ainsi que des échantillons de personnes porteuses d’autres virus respiratoires. Leur essai amélioré par plasmons a détecté l’ARN du SARS‑CoV‑2 dans tous les échantillons positifs en PCR, sans signal supérieur au bruit de fond dans les échantillons négatifs en PCR ou ceux contenant d’autres virus, indiquant une excellente sensibilité et spécificité cliniques comparables à la RT‑PCR. De plus, les concentrations d’ARN mesurées présentaient une relation inverse avec les valeurs du seuil de cycle (Ct) de PCR : les échantillons nécessitant moins de cycles PCR (indiquant une charge virale plus élevée) montraient des niveaux d’ARN plus élevés avec le nouvel essai, conforme aux attentes biologiques et suggérant qu’il peut fournir une information quantitative significative sur la charge virale.
Ce que cela pourrait signifier pour de futures flambées
Pour les non‑spécialistes, le message clé est que cet essai offre une manière d’estimer la quantité de virus présente sans l’étape supplémentaire de copie qui rend la PCR lente et gourmande en équipement. En combinant un anticorps sélectif pour les hybrides ARN–ADN avec des sources lumineuses nanoscalaires ultra‑lumineuses et le comptage numérique, la méthode se rapproche des performances de la PCR tout en conservant un flux de travail simple sur plaque. Avec des validations et des améliorations supplémentaires, de tels essais améliorés par plasmons pourraient être adaptés à de nombreuses cibles ARN et éventuellement reconvertis en formats rapides au point de soins, aidant les cliniciens non seulement à diagnostiquer les infections mais aussi à estimer le stade de la maladie et la contagiosité à partir d’une mesure absolue de l’ARN viral.
Citation: Liu, L., Seth, A., Liu, Y. et al. Plasmon-enhanced bioassay for amplification-free detection and quantification of SARS-CoV-2 RNA. npj Biosensing 3, 13 (2026). https://doi.org/10.1038/s44328-026-00078-x
Mots-clés: Détection de l’ARN du SARS‑CoV‑2, nanomarqueurs plasmoniques, immunodosage numérique, diagnostics sans amplification, quantification de la charge virale