Clear Sky Science · fr
Un biosenseur microfluidique basé sur des micro-organes pour la surveillance continue de la glycémie in vivo
Pourquoi cela compte pour les personnes diabétiques
Pour les personnes vivant avec un diabète de type 1, les systèmes actuels de « pancréas artificiel » demandent encore une attention constante — annoncer les repas, gérer les alarmes et s’inquiéter des hypoglycémies nocturnes. Cette étude explore un type de capteur de glucose radicalement différent qui ne repose pas sur une seule enzyme ni sur une équation informatique, mais emprunte plutôt un petit fragment vivant du propre mécanisme de régulation du sucre de l’organisme : des grappes de cellules pancréatiques appelées îlots. En laissant ces mini-organes faire ce que l’évolution a optimisé, les chercheurs visent à concevoir des moniteurs de glycémie plus intelligents et plus sûrs, capables un jour de fonctionner plus indépendamment en arrière-plan.
Un petit organe comme capteur vivant
La plupart des biosenseurs actuels détectent les substances chimiques en utilisant des molécules purifiées ou des lignées cellulaires isolées. Ils répondent à une substance spécifique puis transmettent le signal brut à un logiciel qui tente de l’interpréter. Les auteurs soutiennent que cette approche ignore un « ordinateur » intégré puissant : des micro-organes, comme les îlots pancréatiques, qui détectent naturellement de multiples signaux à la fois et les transforment en une réponse coordonnée. Chaque îlot contient plusieurs types cellulaires producteurs d’hormones qui communiquent en permanence entre eux. Ensemble, ils maintiennent la glycémie dans une plage étroite et sûre, réagissant non seulement au glucose mais aussi aux acides aminés, aux hormones intestinales et de stress, et à l’historique récent d’élévations ou de baisses. Cette complexité intégrée, suggèrent-ils, pourrait être exploitée pour produire une information plus riche et plus fiable qu’un simple capteur à glucose oxydase.
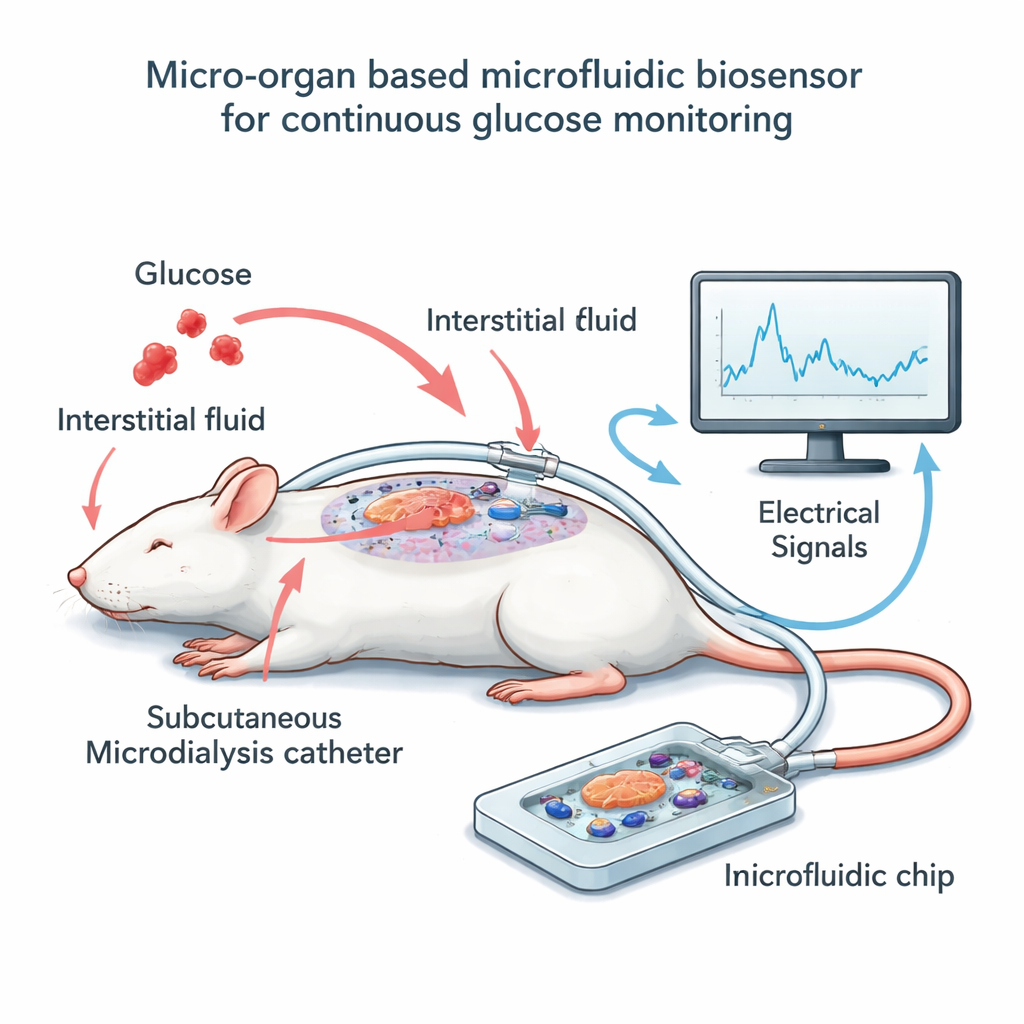
Construction du système puce-et-cathéter
Pour tester cette idée, l’équipe a construit un petit dispositif externe au corps hébergeant quelques dizaines d’îlots de souris au-dessus d’une grille d’électrodes microscopiques. Plutôt que de baigner ces cellules directement dans le sang, ils ont utilisé une technique appelée microdialyse : un fin cathéter flexible est placé juste sous la peau de rats anesthésiés et collecte lentement le liquide tissulaire environnant, qui reflète de près la glycémie mais avec un court retard. Un flux constant et faible transporte ce liquide à travers un canal étroit au-dessus des îlots sur la puce. À mesure que la concentration de glucose dans le dialysat augmente ou diminue, les îlots modifient leur activité électrique, que les électrodes enregistrent sous forme de signaux lents et ondulatoires. En parallèle, les chercheurs mesuraient périodiquement la glycémie des rats et celle du dialysat, ce qui leur a permis d’aligner la lecture électrique avec les valeurs réelles de sucre au fil du temps.
Comment le capteur vivant a réagi aux variations de sucre
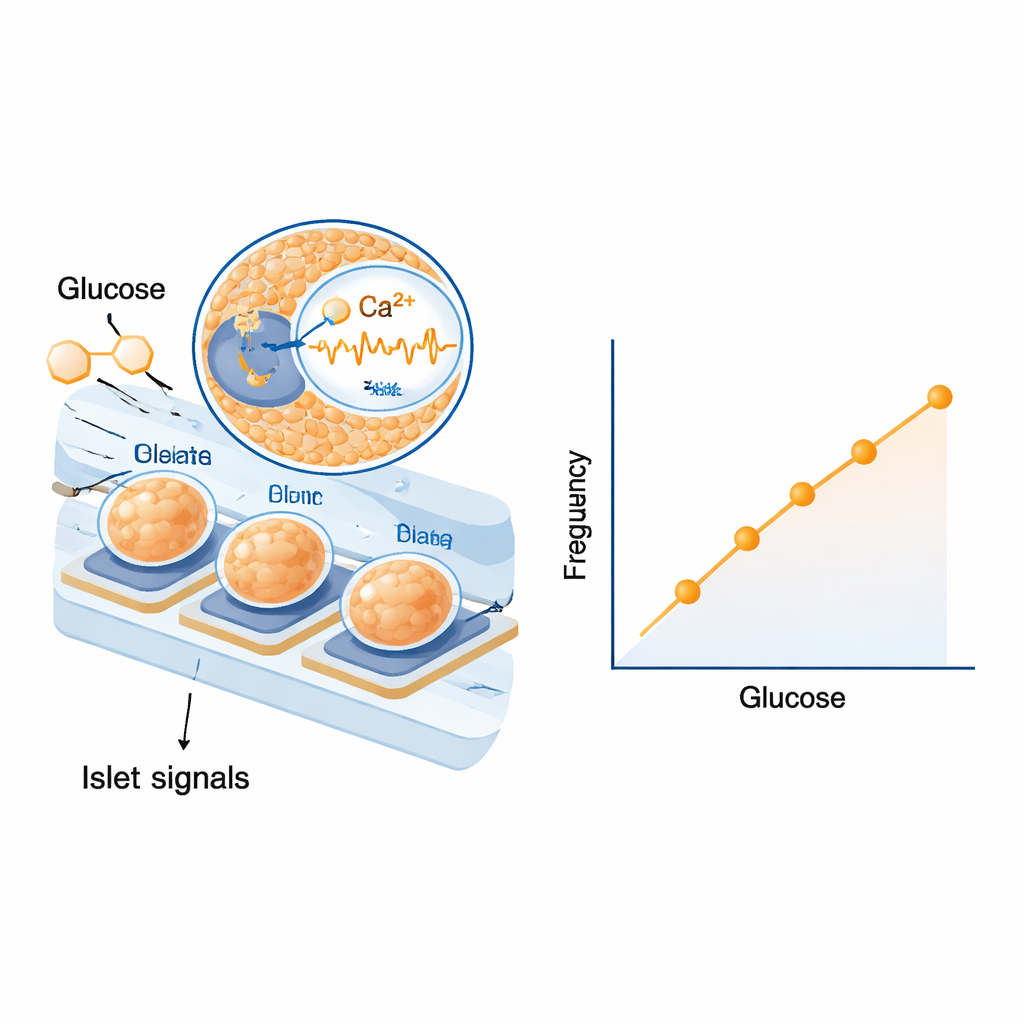
Dans un premier temps, les scientifiques ont vérifié si les îlots sur les électrodes pouvaient répondre à des composants sanguins réels plutôt qu’à de simples solutions de laboratoire. Ils les ont exposés à du sérum humain et de rat présentant différents niveaux de glucose et ont observé des variations nettes et graduées tant dans la fréquence que dans l’amplitude de leurs ondes électriques. Les réponses étaient suffisamment marquées pour distinguer de petites étapes de concentration de sucre dans la plage pertinente pour le diabète. Ils sont ensuite passés aux expériences sur rats, injectant du glucose pour élever la glycémie puis de l’insuline pour la faire baisser. Après avoir tenu compte du délai nécessaire au passage du glucose du sang au liquide tissulaire et à travers le circuit, ils ont constaté que la fréquence des signaux électriques lents des îlots augmentait et diminuait presque en synchronie avec la glycémie. L’analyse statistique sur plusieurs animaux a montré une relation remarquablement étroite et reproductible entre la fréquence du signal et le taux de glucose, tandis que l’amplitude du signal, bien qu’informative, était un peu plus variable.
Fonctions de sécurité intégrées par la biologie
Un avantage important d’utiliser des îlots entiers plutôt qu’une seule molécule est que leur comportement comprend déjà des mécanismes de sécurité façonnés par l’évolution. Des travaux antérieurs, et des indices dans cette étude, montrent que les îlots réagissent plus fortement lorsque la glycémie baisse que lorsqu’elle augmente — une forme d’« hystérésis » qui aide à protéger contre les hypoglycémies dangereuses. Les motifs électriques sont aussi modulés par les types cellulaires voisins qui amplifient ou atténuent la libération d’insuline selon les besoins du corps. Comme la puce se contente d’écouter ces signaux intégrés sans ajouter de colorants ni de modifications génétiques, elle peut enregistrer pendant des jours sans nuire aux cellules. Les auteurs soulignent des défis techniques à venir, tels qu’éviter les bulles d’air, assurer des performances de microdialyse à long terme et décider quel type d’îlots humains ou dérivés de cellules souches devrait être utilisé à terme. Néanmoins, des simulations informatiques basées sur un modèle de diabète établi suggèrent qu’un tel capteur basé sur des îlots pourrait égaler voire surpasser les moniteurs de glycémie actuels dans des conditions difficiles.
Ce que cela pourrait signifier pour les soins du diabète futurs
Ce travail montre qu’une poignée de micro-organes pancréatiques, maintenus en vie sur une petite puce et reliés au corps par un fin cathéter, peuvent suivre en continu la glycémie chez des animaux vivants grâce à leur bavardage électrique naturel. Pour un public non spécialiste, le message clé est que, au lieu de demander à un simple capteur chimique de mesurer le glucose puis de forcer un ordinateur à deviner ce que cela signifie pour le corps, cette approche écoute directement le même type de tissu vivant qui décide normalement de la quantité d’insuline à libérer. Si elle est affinée et rendue pratique pour l’usage humain, un tel biosenseur vivant pourrait devenir le cœur de systèmes de pancréas artificiel véritablement autonomes — des dispositifs qui anticipent discrètement les besoins du corps et réduisent le fardeau quotidien de la gestion du diabète.
Citation: Puginier, E., Pirog, A., de Gannes, F.P. et al. A micro-organ based microfluidic biosensor for continuous monitoring of glucose levels in vivo. npj Biosensing 3, 12 (2026). https://doi.org/10.1038/s44328-025-00077-4
Mots-clés: surveillance continue de la glycémie, pancréas artificiel, îlots pancréatiques, biosenseur microfluidique, diabète de type 1