Clear Sky Science · fr
Microscopie cohérente optique en champ plein dynamique à haute résolution : éclairer l’activité intracellulaire dans les tissus profonds
Observer les cellules vivantes en action, sans aucun colorant
Une grande partie de ce que nous savons des cellules à l’intérieur du corps provient de colorations et de marqueurs fluorescents qui peuvent modifier, voire endommager, le tissu étudié. Cet article présente un microscope avancé capable d’observer l’activité naturelle des cellules profondément à l’intérieur d’organes comme le foie et l’intestin sans aucun marquage. Il transforme de minuscules mouvements internes en images vives, presque fluorescentes, ouvrant une fenêtre sur le tissu vivant qui pourrait un jour aider les médecins à diagnostiquer des maladies en temps réel.
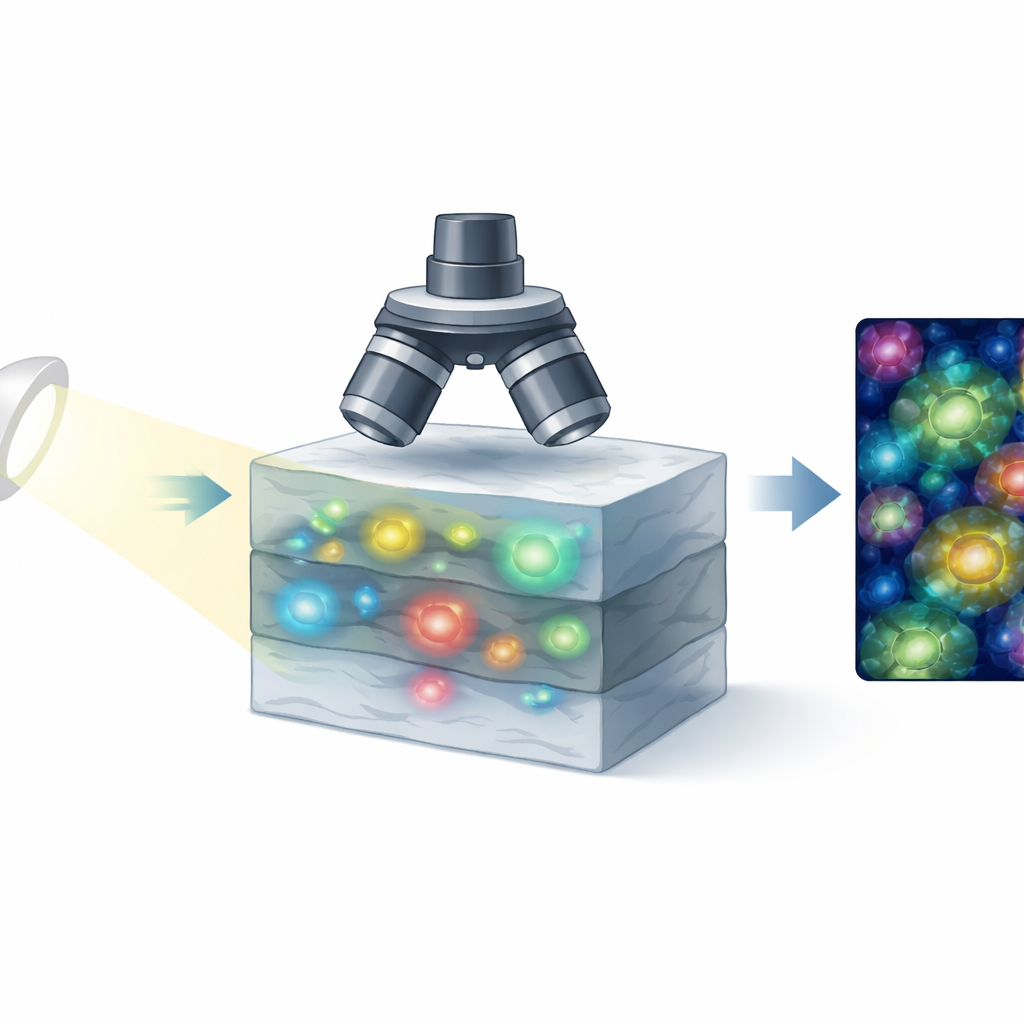
Une nouvelle façon de regarder les cellules bouger
La technique au cœur de ce travail s’appelle microscopie cohérente optique en champ plein dynamique, une forme d’imagerie optique qui détecte la façon dont la lumière est renvoyée depuis l’intérieur du tissu. Plutôt que de balayer point par point, elle enregistre d’un coup un plan entier de tissu avec une caméra, puis répète l’opération rapidement. L’idée clé est que les cellules vivantes ne sont jamais vraiment immobiles : leurs composantes internes se déplacent, vibrent et se réorganisent lorsqu’elles consomment de l’énergie et accomplissent leurs fonctions. Ces mouvements microscopiques modifient subtilement le signal lumineux au fil du temps. En analysant soigneusement la fluctuation du signal en chaque point, le système construit des images dans lesquelles les structures actives ressortent, comme elles le feraient en microscopie à fluorescence, mais sans aucun colorant ajouté.
Aller profondément dans des tissus réels et opaques
Imager en profondeur dans de vrais organes est difficile car le tissu diffuse et brouille la lumière, et les microscopes doivent généralement choisir entre netteté et profondeur. Les auteurs ont repensé le microscope dynamique pour dépasser ces limites. Ils ont utilisé d’objectifs à immersion huileux puissants 100×, qui collectent et focalisent la lumière de façon très serrée, et les ont combinés avec une source de lumière blanche spéciale alimentée par un laser. Cette source est à la fois extrêmement lumineuse et spatialement incohérente, ce qui évite les motifs de speckle granuleux qui affectent de nombreux systèmes à base de laser. Avec cette combinaison, le microscope atteint une résolution de l’ordre de quelques centaines de nanomètres — suffisante pour distinguer de fines structures cellulaires — tout en conservant une profondeur d’observation d’environ 120 micromètres dans des tissus fortement diffusants comme le foie. Un bras de référence motorisé et intelligent ajuste en continu le chemin optique à mesure que la mise au point s’enfonce, maintenant un contraste élevé sur tout le volume.
Révéler l’architecture cachée du foie
Pour tester le système, les chercheurs ont imagé du foie de souris frais. Les versions standard de la technique donnaient des vues assez ternes : des hépatocytes denses avec des contours flous et des zones sombres correspondant aux noyaux. Lorsqu’ils sont passés à l’imagerie dynamique et ont analysé les fluctuations temporelles, les images se sont transformées. Les limites cellulaires sont devenues nettes ; des réseaux filamenteux compatibles avec l’activité mitochondriale sont apparus dans de nombreuses cellules hépatiques ; et les sinusoïdes — les petits canaux sanguins qui se faufilent entre les nappes cellulaires — se sont mis en évidence sur une large gamme de vitesses de fluctuation. Dans des vues agrandies, des globules rouges individuels et de petits éléments mobiles vraisemblablement des plaquettes ou des cellules immunitaires pouvaient être distingués à l’intérieur de ces canaux, même à plusieurs couches de profondeur. La méthode a aussi capturé des différences de vitesse de fluctuation entre diverses régions du tissu, en cartographiant mouvements lents, intermédiaires et rapides par des couleurs différentes.
Plonger dans le paysage microscopique de l’intestin
L’équipe s’est ensuite tourné vers l’intestin grêle, l’imaginant depuis la face interne (mucose) et la face externe (séreuse). Depuis la surface muqueuse, ils ont pu voir les villosités en forme de doigts qui tapissent l’intestin, avec les entérocytes formant une mosaïque serrée aux extrémités. Des noyaux et des structures compatibles avec des microvillosités étaient visibles à la surface cellulaire, ainsi que probablement des cellules caliciformes sécrétant du mucus, et une variété de cellules très actives dans le tissu de soutien sous-jacent. Depuis la face séreuse, le microscope a capturé des réseaux nerveux complexes connus sous le nom de plexus myentérique et sous-muqueux, ainsi que des vaisseaux sanguins qui s’y enchevêtrent. Fait remarquable, il a produit les premières images par cohérence optique de cellules de Paneth à la base des cryptes intestinales — des défenseurs spécialisés de l’intestin — ainsi que des cellules de la crypte environnantes et de possibles cellules stromales de soutien, toutes distinguées par leurs signatures dynamiques.
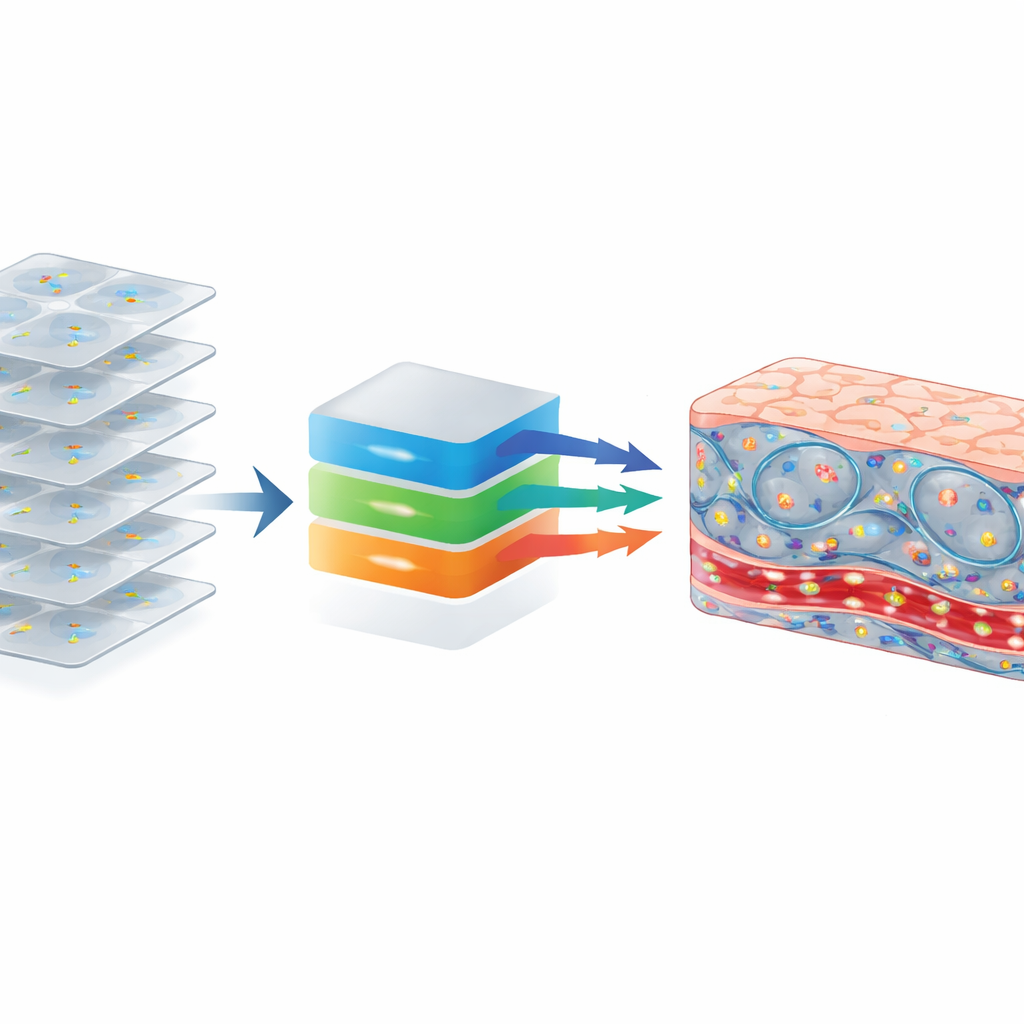
Pourquoi cela importe pour la médecine de demain
En combinant haute résolution, profondeur étendue et contraste basé sur le mouvement, ce nouveau système montre qu’il est possible d’obtenir des images riches, à l’allure fluorescente, de tissus vivants sans colorants ni modifications génétiques. Il met en évidence la fine structure et l’activité des cellules dans des organes complexes comme le foie et l’intestin, révélant l’écoulement sanguin, des candidats cellules immunitaires, des réseaux nerveux et une activité compartimentée au sein de cellules individuelles. Avec des développements supplémentaires pour gérer le mouvement et l’accès chez des animaux vivants ou des patients, la même approche pourrait être adaptée pour une utilisation in vivo. Cela offrirait aux cliniciens un moyen rapide, sans marqueur, d’observer le comportement des cellules en temps réel pendant une intervention ou un diagnostic, permettant potentiellement une détection plus précoce des maladies et des traitements plus précis et personnalisés.
Citation: Tarvydas, E., Trečiokaitė, A. & Auksorius, E. High-resolution dynamic full-field optical coherence microscopy: illuminating intracellular activity in deep tissue. npj Imaging 4, 21 (2026). https://doi.org/10.1038/s44303-026-00153-y
Mots-clés: microscopie sans marqueur, imagerie par cohérence optique, imagerie du tissu hépatique, microstructure intestinale, dynamique cellulaire