Clear Sky Science · fr
Maximiser l’utilisation des photons en microscopie de localisation monoculaire spectroscopique grâce à des prismes à double coin dispersés symétriquement
Des vues plus nettes du monde minuscule
Beauxoup des acteurs les plus importants en biologie — des molécules individuelles à l’intérieur de nos cellules — sont bien trop petits pour être vus avec des microscopes ordinaires. Au cours de la dernière décennie, de nouvelles méthodes de « super‑résolution » ont changé la donne, mais elles obligent souvent les chercheurs à sacrifier la netteté de l’image au profit de l’information spectrale ou à recourir à des expériences longues et compliquées. Cet article présente un module optique astucieux qui aide les chercheurs à visualiser plusieurs types de molécules simultanément, en 3D, avec plus de détail et moins de tracas.
Voir les molécules une par une
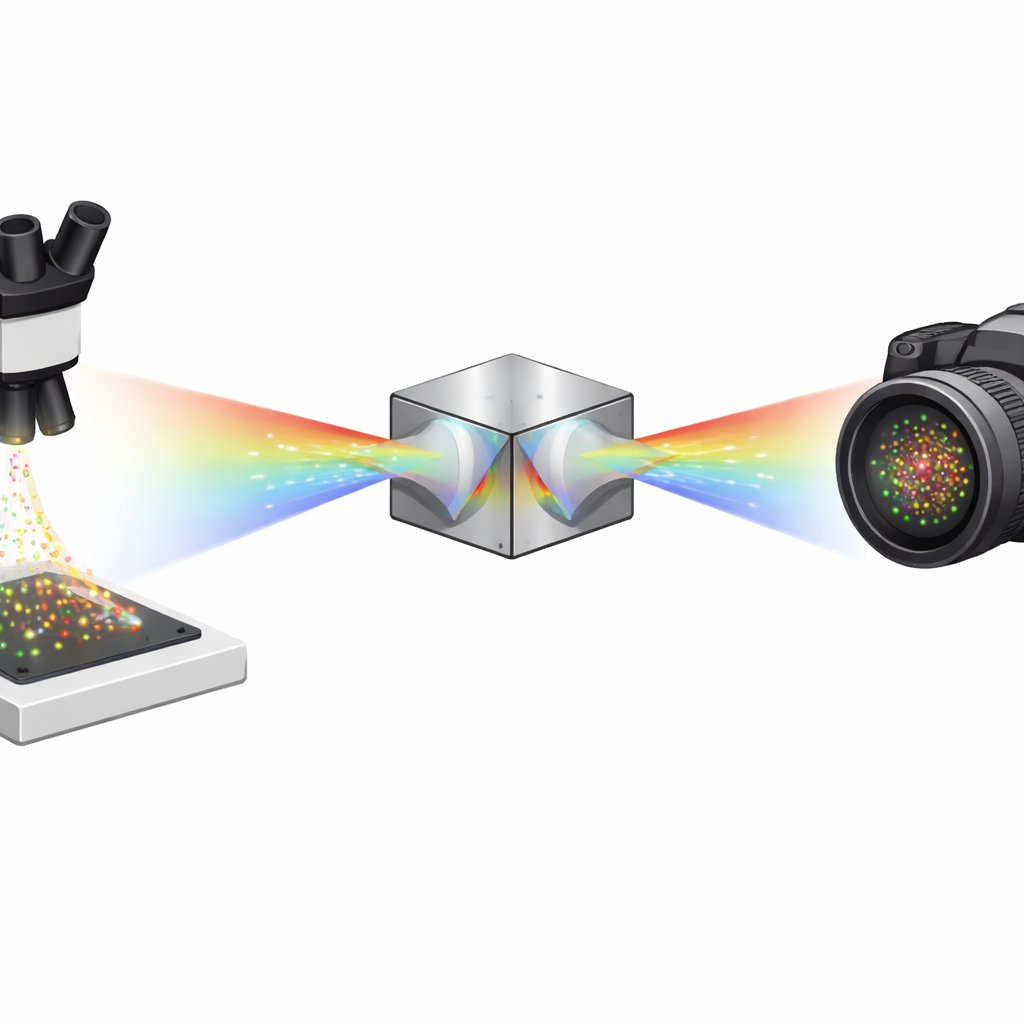
Les méthodes de super‑résolution comme STORM et PALM fonctionnent en ne faisant clignoter qu’un petit nombre de molécules fluorescentes à la fois, puis en localisant chaque clignotement avec grande précision et en combinant des milliers d’images pour obtenir une image détaillée. La microscopie de localisation monoculaire spectroscopique (sSMLM) va plus loin : elle localise non seulement chaque molécule, mais mesure aussi son spectre de couleur. Cette information spectrale supplémentaire est puissante, car elle permet d’utiliser plusieurs colorants aux spectres chevauchants et de les distinguer. Le revers de la médaille est que la sSMLM traditionnelle doit généralement répartir des photons précieux entre une image de position et une image spectrale, ce qui brouille l’image finale et rend les molécules faibles difficiles à détecter.
Utiliser chaque photon deux fois
Les auteurs résolvent ce problème avec un module optique compact basé sur deux prismes à double coin identiques et un séparateur de faisceau. Au lieu d’envoyer les photons dans un bras « position » et un bras « couleur » distinct, leur conception à prismes à double coin dispersés symétriquement (SDDWP) crée deux copies spectrales symétriques en image miroir de chaque molécule clignotante sur la même caméra. Parce que ces deux images sont parfaitement symétriques, un calcul simple permet de retrouver à la fois la position réelle de la molécule (à partir du point milieu entre les deux taches) et son spectre (à partir de l’écartement entre les taches). En pratique, tous les photons collectés contribuent à la fois à l’information spatiale et spectrale, améliorant de façon spectaculaire la précision de localisation et d’identification de chaque molécule.
Des couleurs plus nettes et plus claires en trois dimensions
À l’aide de modèles analytiques et d’échantillons tests soigneusement calibrés, l’équipe montre que la SDDWP améliore la précision latérale (dans le plan) d’environ 27 % et la précision spectrale d’environ 48 % par rapport à leur système précédent basé sur des prismes. Ils étendent ensuite la conception à l’imagerie tridimensionnelle en utilisant une approche « biplane », où les deux images spectrales sont légèrement hors foyer dans des directions opposées. En analysant comment la taille de chaque tache change entre les deux plans, le système peut déterminer à quelle distance, au‑dessus ou au‑dessous du plan focal, se situe une molécule, atteignant une précision axiale de l’ordre de 18 nanomètres sur une plage utile d’environ une demi‑micromètre. Malgré la complexité ajoutée par l’imagerie 3D, la nouvelle conception conserve des niveaux de netteté spectrale proches de ceux de la 2D, permettant une discrimination très fine entre des colorants dont les spectres se chevauchent fortement.
Séparer les structures cellulaires et suivre des particules en mouvement
Pour démontrer ce que cela signifie en pratique, les chercheurs ont imagé des cellules HeLa fixées en 3D en utilisant un seul laser rouge et trois colorants rouge lointain dont les spectres se chevauchent normalement. Ils ont marqué les peroxysomes, les microtubules et les mitochondries, et ont montré que le système pouvait séparer de manière fiable ces structures sur la base de leurs différences spectrales subtiles tout en conservant un fort niveau de détail spatial sur la profondeur. Ils ont également utilisé des points quantiques spectrales distincts comme petites étiquettes pour suivre de nombreuses particules se déplaçant simultanément dans une solution visqueuse. En traitant le spectre de chaque particule comme une « empreinte » unique, la configuration SDDWP a pu suivre correctement des centaines de trajectoires densément emballées qui, sinon, se seraient inextricablement emmêlées lorsque les trajets se croisent, réduisant les erreurs de suivi à seulement quelques pour cent même à des densités de particules proches des limites théoriques.
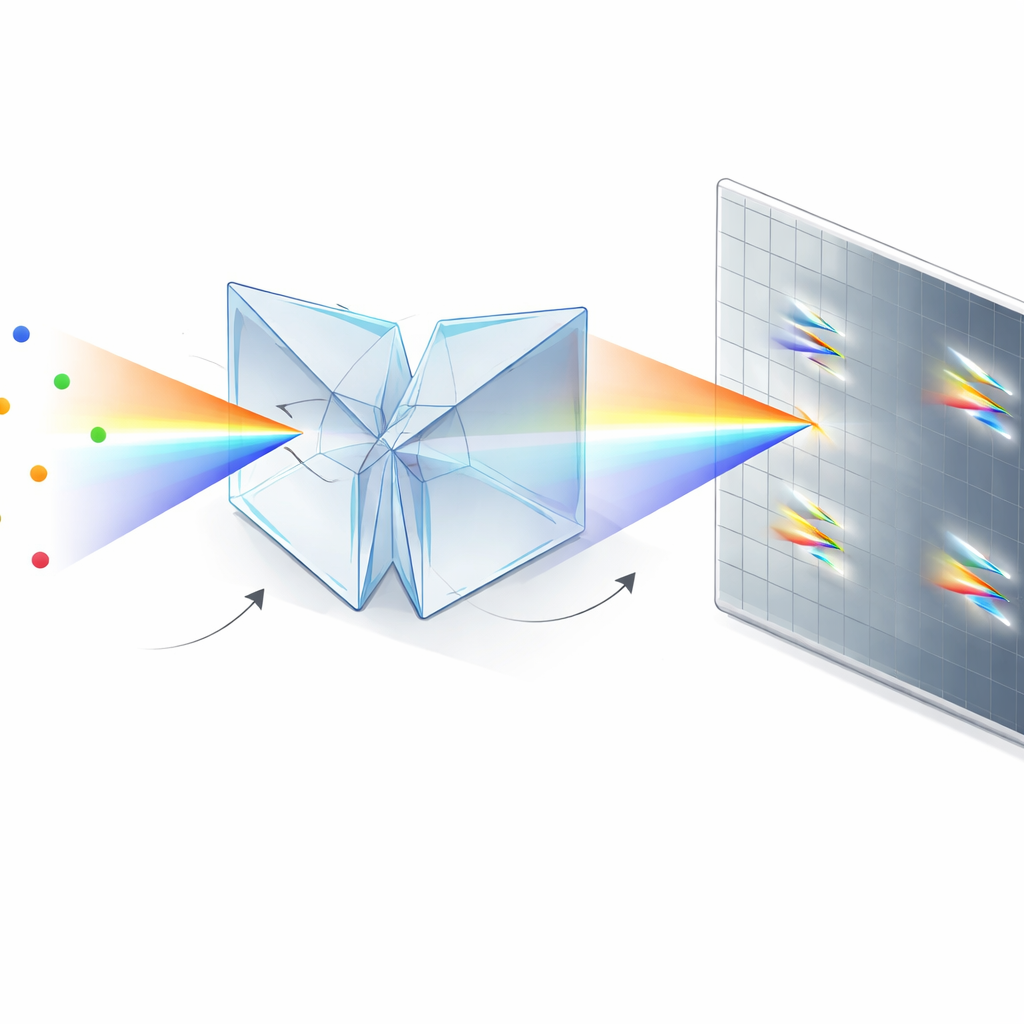
De l’optique complexe à un accessoire simple
Outre les performances, un avantage clé de cette approche est sa praticité. L’unité SDDWP est un ensemble petit et majoritairement monolithique qui se fixe sur le port latéral d’un microscope à fluorescence inversé standard et ne nécessite qu’un alignement modéré. Sa conception à base de prismes gaspille bien moins de photons que les réseaux de diffraction, et elle est mécaniquement suffisamment stable pour rester calibrée sur de longues périodes avec seulement des vérifications de routine. Cela en fait une voie de mise à niveau réaliste pour de nombreux laboratoires existants travaillant sur des molécules uniques.
Ce que cela signifie pour la microscopie future
En repensant la façon dont la lumière est divisée et recombinée, ce travail montre qu’il est possible d’obtenir à la fois des positions plus nettes et une information colorimétrique plus claire à partir du même pool limité de photons. En termes pratiques, il permet aux scientifiques de distinguer davantage de types de molécules dans des environnements tridimensionnels denses et de suivre simultanément de nombreuses particules marquées, sans sacrifier la qualité d’image. À mesure que la technique sera adoptée et adaptée — potentiellement même pour l’imagerie de cellules vivantes avec une lumière rouge douce — elle pourrait devenir un outil polyvalent pour explorer comment les assemblages moléculaires complexes et les organites sont organisés et comment ils se déplacent à l’intérieur des cellules vivantes, le tout à l’échelle du nanomètre.
Citation: Yeo, WH., Brenner, B., Shi, M. et al. Maximizing photon utilization in spectroscopic single-molecule localization microscopy using symmetrically dispersed dual-wedge prisms. npj Imaging 4, 20 (2026). https://doi.org/10.1038/s44303-026-00152-z
Mots-clés: microscopie monocellulaire, imagerie super‑résolution, imagerie spectrale, imagerie cellulaire 3D, suivi de particules uniques