Clear Sky Science · fr
Techniques d’imagerie avancées pour la navigation peropératoire des tumeurs
Voir le cancer plus clairement en salle d’opération
La chirurgie oncologique repose souvent sur un compromis délicat : retirer la moindre cellule cancéreuse tout en épargnant autant de tissu sain que possible. Cet article de synthèse explique comment une nouvelle génération d’outils d’imagerie aide les chirurgiens à visualiser réellement les tumeurs et leurs marges en temps réel pendant l’intervention. Pour un lecteur non spécialiste, l’intérêt est simple — ces technologies promettent moins de réinterventions, des résections tumorales plus précises et de meilleures chances de survie à long terme, en offrant aux chirurgiens une « carte » plus nette pendant qu’ils opèrent.
Pourquoi une meilleure vision peropératoire est importante
Le cancer est aujourd’hui l’une des principales causes de mortalité dans le monde, et la chirurgie reste une pierre angulaire du traitement. Pourtant, même le chirurgien le plus expérimenté a longtemps été limité par ce qu’il peut voir et palper, et par des examens réalisés des jours ou des semaines avant l’opération. Les outils traditionnels tels que l’échographie, le scanner, l’IRM et la TEP aident à planifier la chirurgie, mais ils sont souvent encombrants, lents ou peu adaptés à une utilisation continue pendant l’intervention. Il peut donc être difficile de savoir exactement où la tumeur s’arrête et où commence le tissu sain, ce qui augmente le risque de laisser des cellules cancéreuses ou d’enlever trop de tissu normal. La revue présente comment « l’imagerie peropératoire » — l’imagerie en direct utilisée directement en salle d’opération — change cette donne.
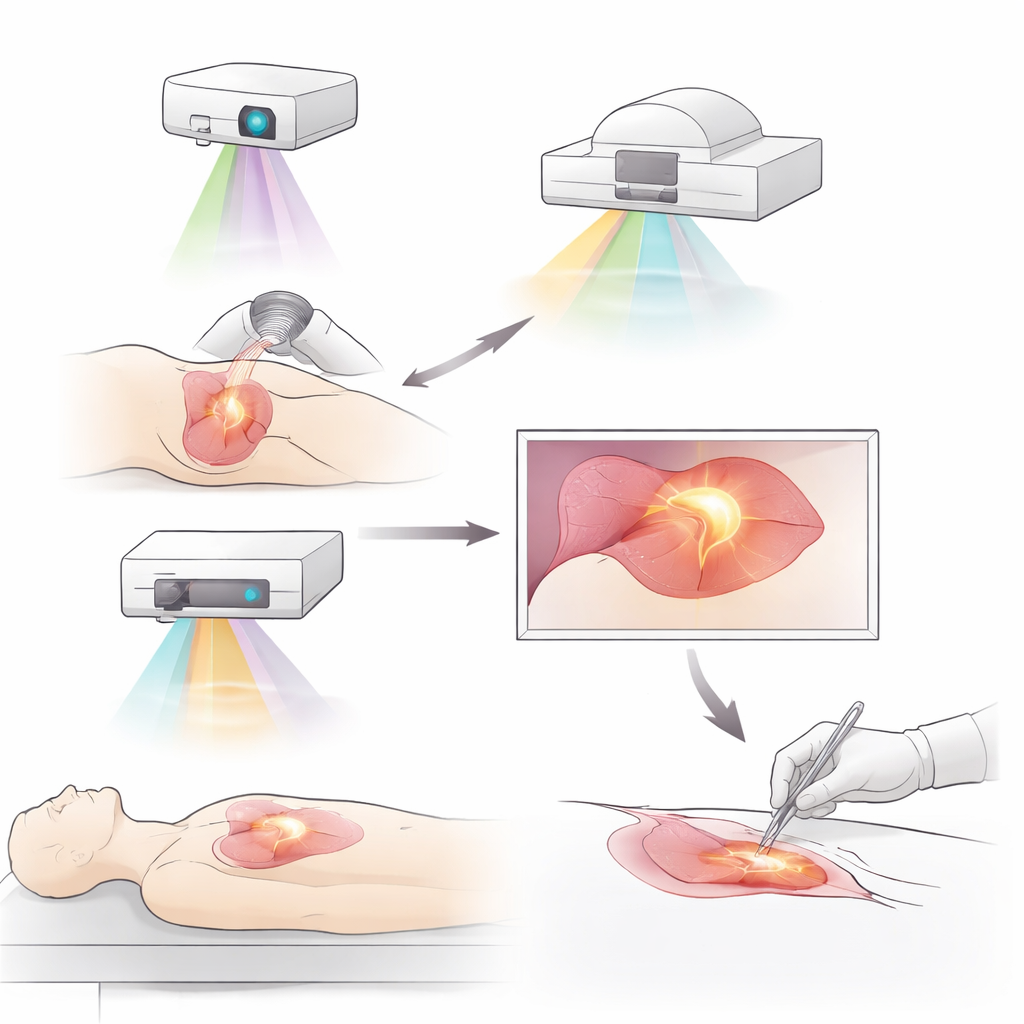
Tumeurs luminescentes et nouvelles façons de les éclairer
Une avancée majeure est l’imagerie par fluorescence, dans laquelle des colorants ou des sondes moléculaires spéciales rendent les tumeurs visibles sous lumière proche infrarouge. Des colorants plus anciens et non ciblés, comme l’indocyanine verte, ont déjà aidé les chirurgiens à délimiter les tumeurs, tracer les vaisseaux lymphatiques et localiser les ganglions clés dans les cancers du sein, du foie, du poumon et de l’estomac. Des sondes ciblées plus récentes vont plus loin en se fixant sur des molécules surexprimées par les cellules tumorales ou leur microenvironnement. Citons des sondes qui se lient aux récepteurs de facteurs de croissance, aux points de contrôle immunitaires ou à des protéines abondantes dans le tissu de soutien tumoral ou les zones hypoxiques. Certains de ces agents peuvent même être reliés à des médicaments anticancéreux, associant visualisation précise et thérapie dans une même molécule. Des essais cliniques précoces montrent que ces traceurs peuvent révéler des foyers tumoraux cachés et réduire le besoin de réintervention après des opérations conservatrices du sein.
Au-delà de la lueur : son, lumière et multiples couleurs
Si la fluorescence est centrale, la revue met en avant plusieurs approches complémentaires qui révèlent différents aspects d’une tumeur. L’imagerie photoacoustique utilise des impulsions lumineuses pour générer des ondes sonores à l’intérieur des tissus, combinant la résolution des méthodes optiques à la profondeur d’exploration de l’échographie, et a permis de mettre en évidence de très petites métastases que d’autres examens manquent. L’imagerie multispectrale et hyperspectrale décompose la lumière en de nombreuses bandes, capturant des différences subtiles dans l’absorption et la réflexion de la lumière par les tissus ; cela permet de distinguer le tissu cancéreux du tissu normal avec une grande précision dans les cancers du sein, du col et gastro-intestinaux. Les progrès en échographie — y compris les techniques mesurant la rigidité tissulaire — apportent de l’information en profondeur et aident à montrer jusqu’où le cancer a infiltré. La spectroscopie Raman, qui lit l’« empreinte » chimique des tissus basée sur la diffusion de la lumière par les molécules, offre une identification sans marqueur et très spécifique du cancer pendant la chirurgie, surtout lorsqu’elle est combinée à d’autres modalités.
Construire des cartes 3D et combiner plusieurs vues
Un autre thème de l’article est la combinaison d’images en vues tridimensionnelles et multimodales que les chirurgiens peuvent utiliser de manière intuitive. Les reconstructions tridimensionnelles des vaisseaux sanguins, des voies lymphatiques et des organes, superposées aux signaux fluorescents, aident à planifier des résections segmentaires précises du foie et du poumon et guident les dissections ganglionnaires difficiles. Les systèmes hybrides qui fusionnent la TEP avec l’imagerie optique ou associent des traceurs de médecine nucléaire à la fluorescence permettent d’utiliser la même sonde pour le bilan préopératoire corps entier et pour l’orientation peropératoire. Des plateformes émergentes intègrent l’ablation au laser, l’optical coherence tomography et la robotique pour localiser et traiter automatiquement les lésions avec une grande précision. Ces approches visent à fournir aux chirurgiens à la fois une « vue d’ensemble » de la dissémination tumorale et le niveau de détail nécessaire pour couper selon des marges sûres et nettes.
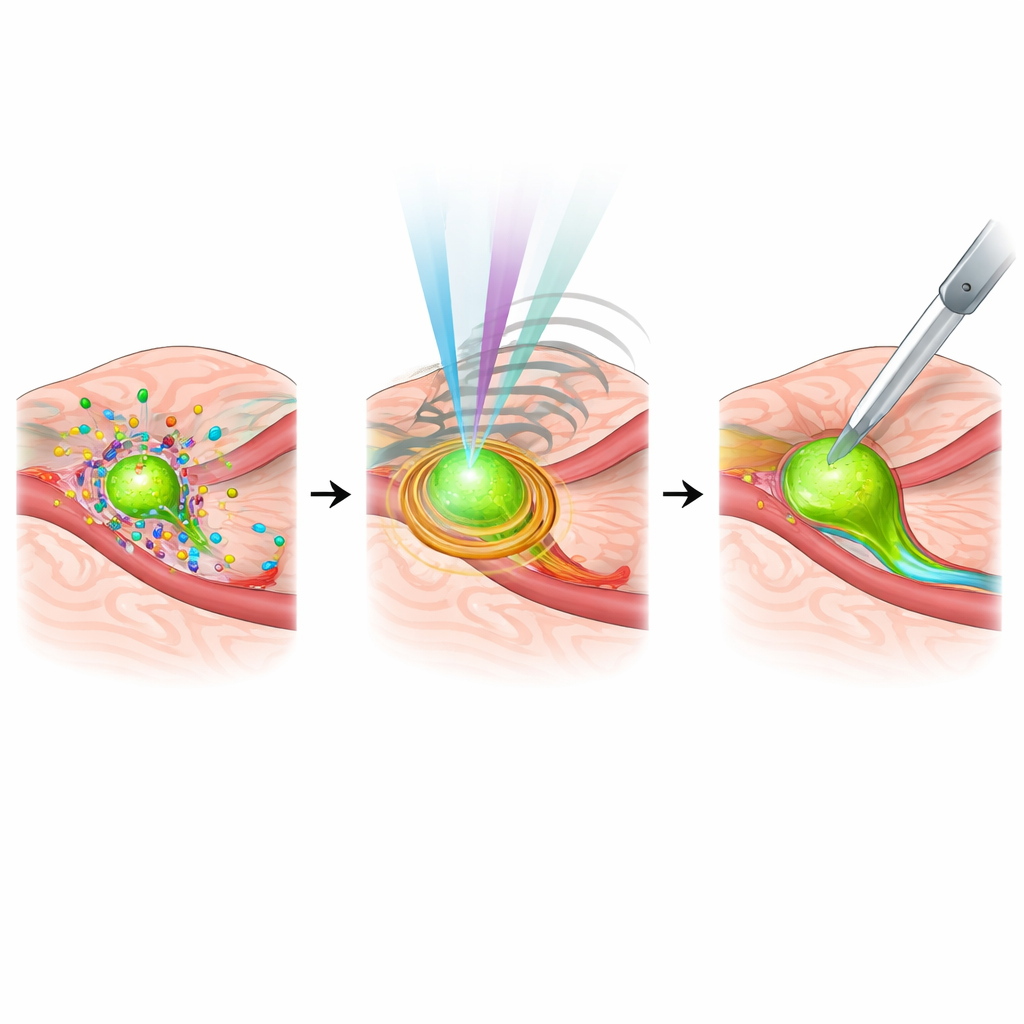
Systèmes plus intelligents, cibles personnalisées et obstacles restants
La revue se tourne aussi vers l’avenir en abordant le rôle de l’intelligence artificielle et de la médecine personnalisée. Des modèles d’apprentissage automatique aident déjà à distinguer en temps réel le tissu cancéreux du tissu normal, reconnaître des structures anatomiques critiques et même prédire l’atteinte ganglionnaire lors de chirurgies pancréatiques, réduisant potentiellement la dépendance à l’anatomopathologie rapide. Parallèlement, les sondes d’imagerie sont redessinées pour correspondre aux signatures moléculaires propres à la tumeur de chaque patient, reliant les images peropératoires aux profils génétiques et moléculaires. Néanmoins, des obstacles subsistent : de nombreux systèmes sont coûteux, complexes et difficiles à intégrer aux parcours de soins routiniers ; certains exigent des agents de contraste spécialisés dont la sécurité doit être rigoureusement contrôlée ; et les normes pour intégrer toutes ces données dans des systèmes de navigation évoluent encore.
Ce que cela signifie pour les patients
De manière accessible, la conclusion de l’article est que les chirurgiens gagnent quelque chose qu’ils n’ont jamais vraiment eu auparavant : la capacité de voir le cancer vivant avec une grande clarté pendant qu’ils opèrent. En illuminant les tumeurs, en lisant leur chimie, en les cartographiant en 3D et en combinant plusieurs types d’images — souvent assistés par l’IA — ces outils peuvent aider à retirer davantage de tumeur tout en préservant plus de tissu sain. Bien que le coût, la formation et les lacunes technologiques doivent être résolus avant que ces systèmes soient largement disponibles, la trajectoire est claire. L’imagerie peropératoire avancée est prête à devenir une composante clé de la chirurgie cancéreuse standard, offrant aux patients des interventions plus précises, moins de récidives et de meilleures chances de contrôle à long terme.
Citation: Li, K., Zhang, Y., Yang, H. et al. Advanced imaging techniques for tumor intraoperative navigation imaging. npj Imaging 4, 18 (2026). https://doi.org/10.1038/s44303-026-00150-1
Mots-clés: imagerie peropératoire, chirurgie guidée par fluorescence, détection des marges tumorales, imagerie multimodale du cancer, imagerie photoacoustique