Clear Sky Science · fr
Imagerie multimodale corrélative pour la cartographie spatiale microscopique des interactions entre collagène et activité génique dans les tissus humains
Pourquoi explorer l’intérieur des muscles compte
Les maladies qui cicatrisent lentement nos organes, comme la dystrophie musculaire de Duchenne (DMD), se déroulent à des échelles trop petites pour l’œil nu. L’activité génétique se produit à l’intérieur de cellules individuelles, tandis que le tissu de soutien qui les entoure est constitué de fibres protéiques minimes. Jusqu’à présent, les scientifiques ont rarement pu observer ces deux univers simultanément dans la même tranche de tissu humain. Cette étude présente une méthode pour le faire, révélant comment les messages génétiques et l’armature structurelle du corps interagissent à l’échelle microscopique.
Deux « caméras » sur la même coupe de tissu
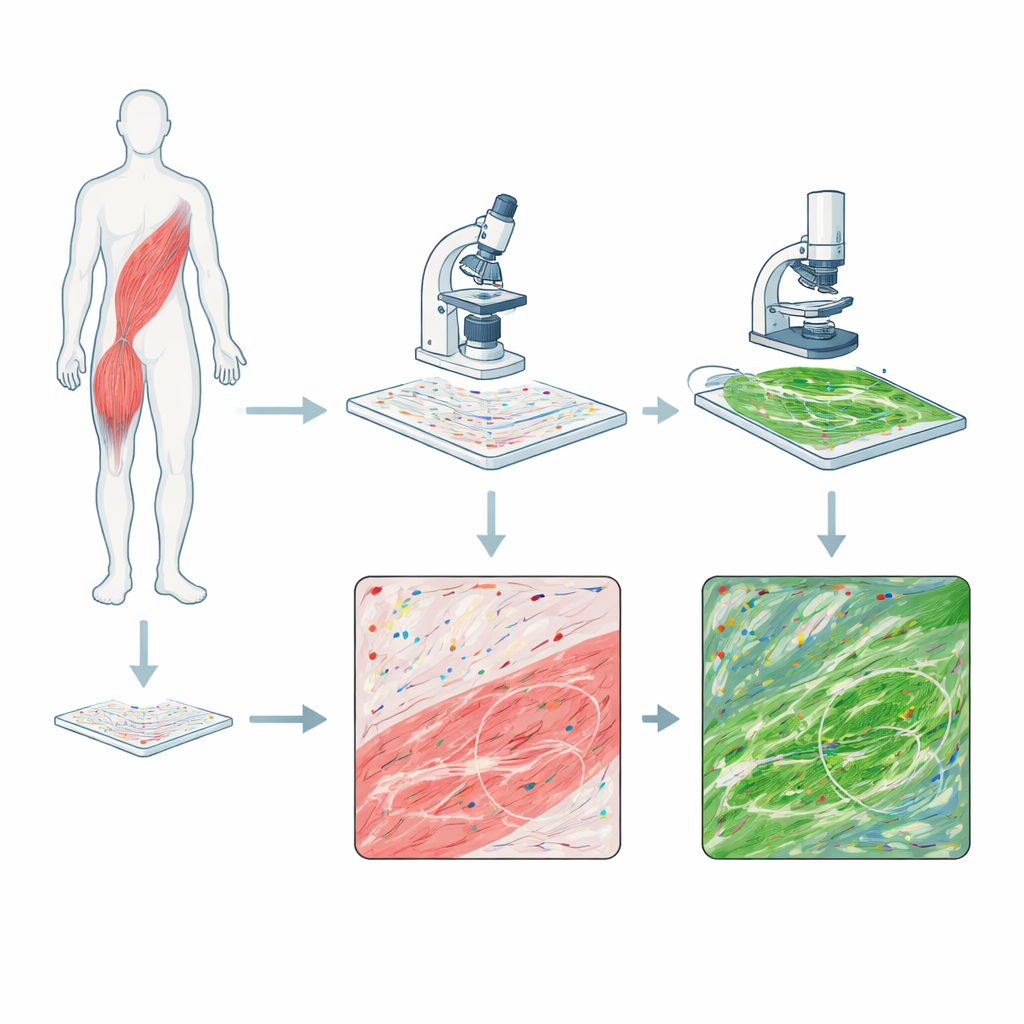
Les chercheurs ont combiné deux méthodes d’imagerie puissantes sur des coupes uniques de biopsies de muscle squelettique humaines, provenant de personnes atteintes de DMD et d’un volontaire sain. Une méthode, appelée RNAscope, colore des molécules d’ARN individuelles — les copies actives des gènes — sous forme de points colorés, montrant où se trouvent des messages génétiques spécifiques. La seconde, la microscopie multiphotonique, utilise un faisceau laser pour faire scintiller les fibres de collagène du tissu sans aucun colorant ajouté, capturant l’architecture du tissu conjonctif qui s’épaissit lors de la cicatrisation et de la fibrose. En imagerie d’abord des signaux ARN puis des signaux de collagène sur la même lame, ils ont pu aligner les deux images de sorte que chaque point d’activité génique puisse être comparé au réseau de fibres environnant, pixel par pixel.
Ce que chaque vue séparée révèle déjà
L’examen de chaque méthode d’imagerie prise isolément a déjà mis en évidence des différences nettes entre muscle malade et sain. RNAscope a montré que les muscles des patients atteints de DMD contenaient moins de transcrits de dystrophine — les molécules d’ARN nécessaires à la production de la protéine dystrophine absente — que l’échantillon sain. Les signaux restants différaient aussi en taille selon la région du gène ciblée, suggérant des différences dans le traitement du long message de la dystrophine. Parallèlement, les images multiphotoniques ont montré que les muscles DMD étaient remplis de longues fibres de collagène denses, signe visuel de cicatrisation fibreuse, tandis que le muscle sain présentait moins de fibres, plus uniformément réparties. Ces observations concordent avec l’expérience clinique : dans la DMD, le tissu musculaire est progressivement remplacé par de la graisse et du tissu cicatriciel.
Voir plus large : motifs globaux dans le tissu
Après avoir effectué l’enregistrement numérique des deux types d’images, l’équipe a divisé chaque section de tissu en une grille, traitant chaque carré comme un petit voisinage. Dans chaque case, ils ont mesuré à la fois des caractéristiques du collagène — longueur des fibres, orientation et courbure — et la densité locale des points d’ARN de la dystrophine. Cette vue en « carte thermique » a révélé une variation ponctuée, zone par zone, de l’activité génique et de la structure du collagène dans le muscle DMD. Toutefois, lorsque ces mesures ont été comparées par des tests statistiques, l’abondance en transcrits et les propriétés du collagène n’ont montré quasiment aucune relation cohérente à cette échelle grossière. Autrement dit, en moyennant sur des régions relativement larges, les zones riches en ARN de dystrophine n’étaient pas systématiquement plus ou moins fibreuses que celles avec moins de signaux ARN.
Voir de près : relations à l’échelle cellulaire
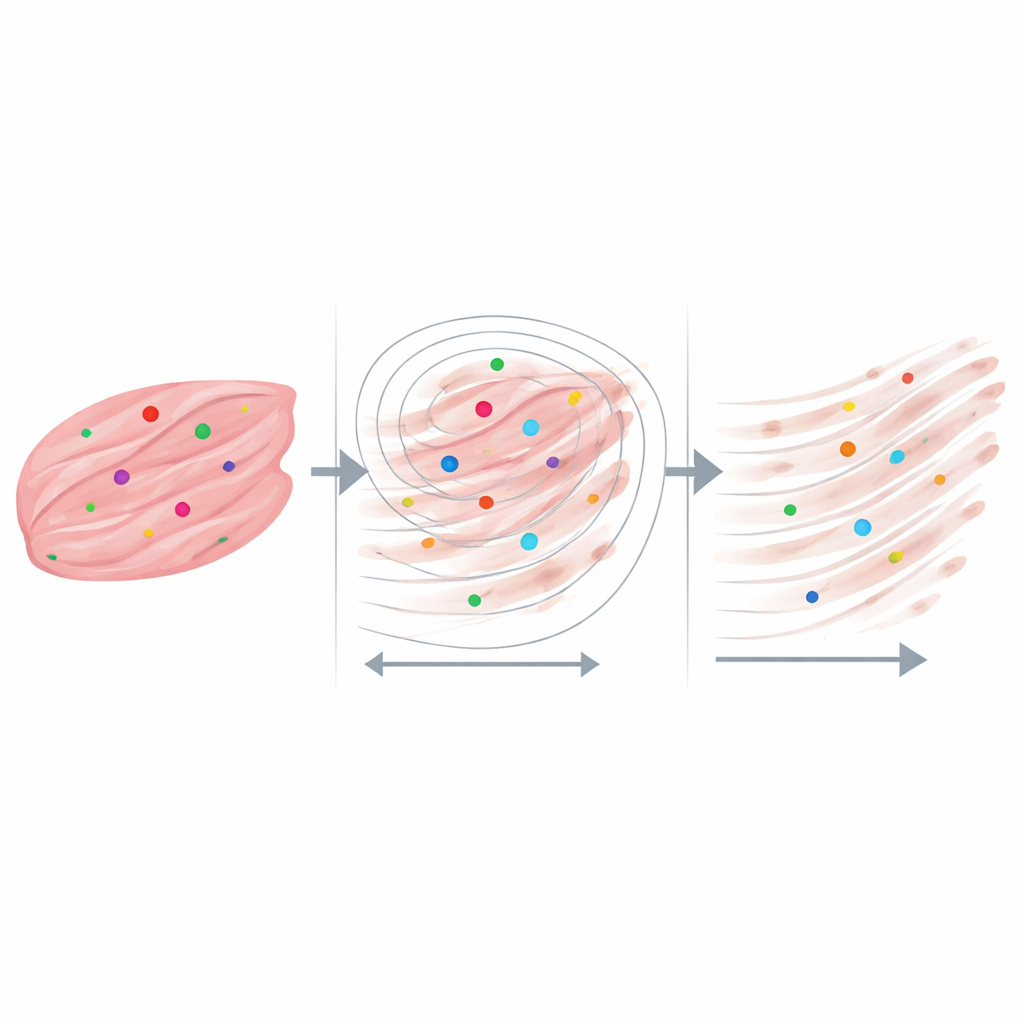
Les résultats les plus éclairants sont apparus lorsque les scientifiques se sont concentrés sur des voisinages mesurés sur seulement quelques dizaines de micromètres — à peu près la taille des fibres musculaires individuelles et de leurs environs immédiats. Pour chaque point d’ARN, ils ont tracé une série de cercles concentriques croissants et ont compté combien de fibres de collagène se trouvaient à l’intérieur, ainsi que la longueur de ces fibres. Dans les tissus DMD comme dans les tissus sains, les fibres de collagène étaient les plus longues juste à côté des signaux ARN de dystrophine et devenaient progressivement plus courtes à mesure que la distance augmentait. Dans les échantillons les plus sévèrement cicatrisés, les points de transcrits avaient presque toujours du collagène à proximité, même à très petites distances, tandis que dans l’échantillon sain de nombreux points ARN se trouvaient dans des régions avec peu ou pas de collagène proche. Des analyses de contrôle utilisant des points placés aléatoirement et des réglages d’analyse d’image légèrement modifiés ont montré que ce schéma ne pouvait pas s’expliquer simplement par le hasard ou par des artefacts logiciels.
Ce que cela pourrait signifier pour les maladies musculaires et au-delà
Ces résultats suggèrent que des liens importants entre messages géniques et structure tissulaire peuvent rester masqués lorsqu’on ne regarde que des moyennes globales, mais deviennent apparents lorsqu’on les examine à l’échelle cellulaire. Dans cette étude de démonstration, les régions enrichies en certains transcrits de dystrophine avaient tendance à se situer à proximité de fibres de collagène plus longues et plus denses, laissant entendre que l’activité génique locale et le remodelage fibrotique peuvent s’influencer mutuellement au sein de micros-environnements musculaires. Les auteurs soulignent que leur groupe de patients est restreint et que le travail n’est pas encore un test clinique. Ils présentent plutôt une plateforme flexible susceptible d’être étendue à d’autres gènes, types de tissus et méthodes d’imagerie. En reliant où les gènes sont actifs et la manière dont l’échafaudage tissulaire est organisé, cette approche ouvre la voie à la découverte de nouveaux biomarqueurs spatiaux de la fibrose, de la régénération et des réponses aux thérapies émergentes à base d’ARN.
Citation: Scodellaro, R., Mietto, M., Ferlini, A. et al. Correlative multimodal imaging for microscale spatial mapping of collagen-gene activity interactions in human tissues. npj Imaging 4, 17 (2026). https://doi.org/10.1038/s44303-026-00149-8
Mots-clés: imagerie multimodale, dystrophie musculaire de Duchenne, fibrose du collagène, expression génique spatiale, biopsie du muscle squelettique