Clear Sky Science · fr
Une stratégie d'un seul pas pour la radiomarquage en PET, SPECT et radionucléides thérapeutiques utilisant des nanoparticules comme chélateur universel
Pourquoi de petites particules radioactives ont de l’importance
Les soins modernes du cancer reposent de plus en plus sur des médicaments radioactifs qui permettent à la fois de visualiser les tumeurs lors d’examens et, dans certains cas, de les détruire de l’intérieur. Pourtant, la mise au point de chaque nouveau médicament radioactif est lente et délicate, car la plupart des conceptions doivent être adaptées à un métal radioactif spécifique. Cette étude explore une approche très différente : utiliser un seul type de nanoparticule à base de fer comme « prise universelle » capable de contenir de nombreux isotopes médicaux pour l’imagerie et la thérapie, accélérant potentiellement la création et l’optimisation de ces médicaments.
De nombreuses clés vers une seule serrure
Les médicaments radioactifs actuels s’appuient généralement sur des griffes chimiques appelées chélateurs qui saisissent les atomes métalliques et les relient à des anticorps ou d’autres molécules ciblantes. Chaque métal radioactif nécessite en général son propre chélateur et sa propre recette — des paramètres tels que la température, l’acidité et le temps de réaction varient. Pour certains métaux d’importance médicale, notamment ceux employés en thérapies par particules alpha, il n’existe toujours pas de chélateur idéal. Les auteurs soutiennent que cette approche métal par métal est devenue un goulot d’étranglement : la liste des isotopes utiles ne cesse de croître, mais la chimie pour les manipuler en toute sécurité ne suit pas.
Des nanoparticules comme prise universelle
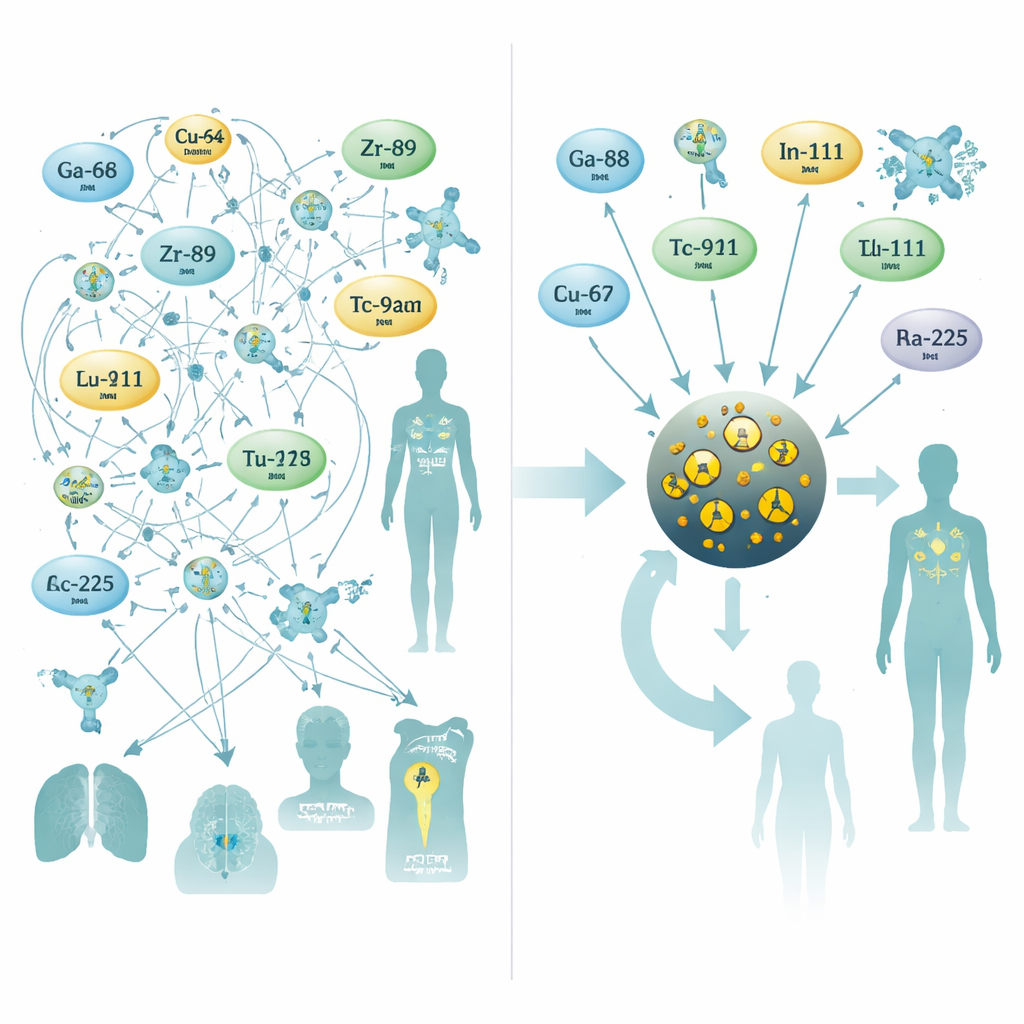
Pour répondre à ce défi, les chercheurs se sont tournés vers de très petites nanoparticules d’oxyde de fer, un matériau déjà étudié pour le contraste en IRM. Ils ont conçu des particules avec un cœur d’oxyde de fer d’environ trois nanomètres de diamètre, enveloppé d’un revêtement de citrate qui les stabilise dans le flux sanguin. Lors d’une étape de synthèse assistée aux micro-ondes d’une durée unique de 10 minutes, ils ont dopé le cœur avec l’un des dix métaux radioactifs couramment utilisés pour la TEP, le SPECT ou la radiothérapie interne. Ce procédé en une seule étape a produit des particules de taille constante avec de bons rendements et, surtout, une excellente stabilité dans le sérum humain — même pour des isotopes thérapeutiques difficiles comme le radium‑223 et l’actinium‑225, dont les produits de décroissance échappent souvent aux chélateurs traditionnels.
Imager des caillots et des tumeurs cérébrales
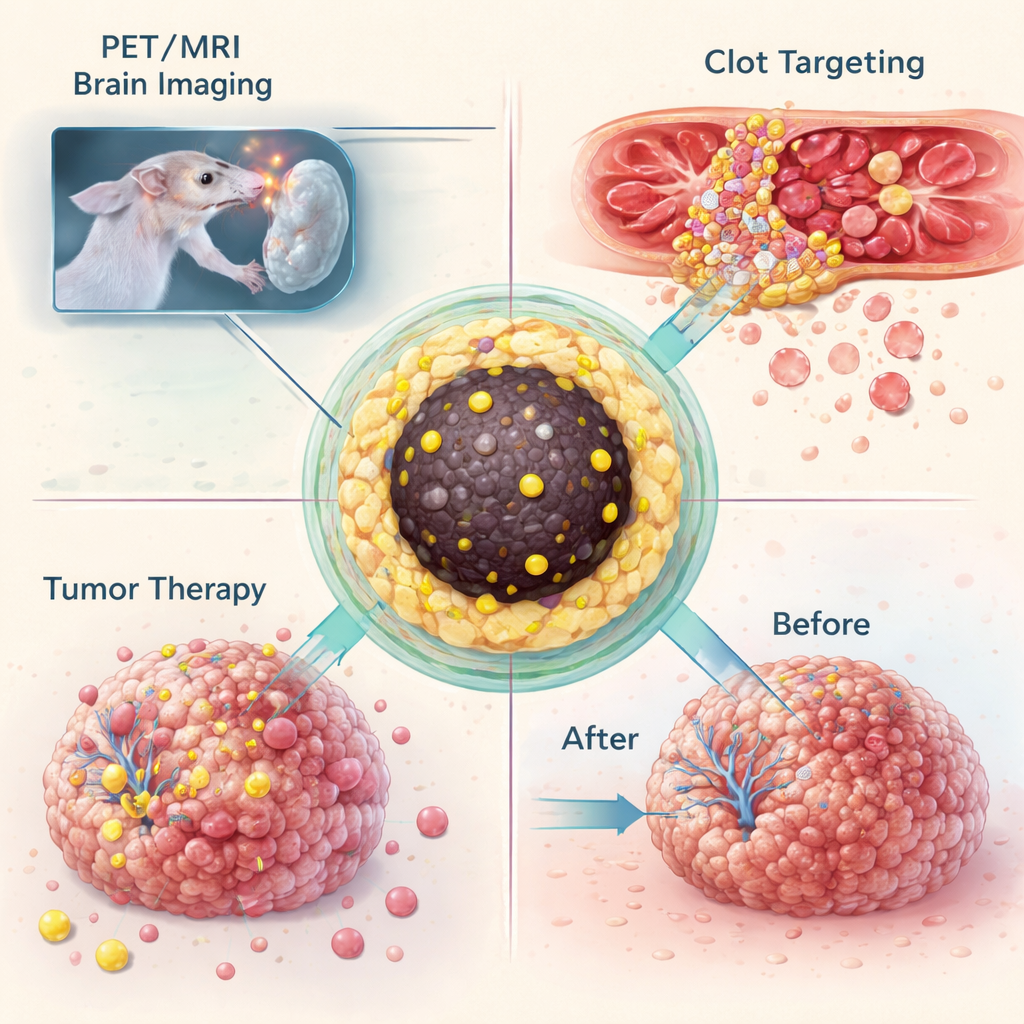
Après avoir montré qu’ils pouvaient piéger de nombreux isotopes différents dans la même conception de nanoparticule, l’équipe a testé ce que ces « nanotraceurs » permettent en conditions vivantes. Dans un modèle murin de glioblastome, une tumeur cérébrale mortelle, des particules marquées au gallium‑68 ont été injectées dans la circulation et imagées par PET combiné à l’IRM. Les particules se sont accumulées dans les tumeurs suffisamment volumineuses pour perturber la barrière hémato‑encéphalique, permettant à la même formulation d’offrir à la fois un contraste IRM marqué et un signal PET sensible. Dans une expérience séparée, les particules ont été modifiées chimiquement pour pouvoir se lier, via une réaction « click » hautement sélective, à un anticorps ciblant les plaquettes activées à l’intérieur des caillots sanguins. Chez des souris présentant une lésion de l’artère carotide, cette stratégie de « pré-ciblage » en deux étapes a produit des signaux PET nets au niveau du caillot, tandis que les animaux témoins ne montraient aucun point chaud comparable.
Du diagnostic au traitement et une évacuation corporelle plus sûre
La même plateforme a également été utilisée pour délivrer un traitement. Lorsque des nanoparticules chargées en lutétium‑177 ont été injectées directement dans des tumeurs de glioblastome chez la souris, les particules sont restées en grande partie confinées dans la masse tumorale pendant au moins deux semaines. Pendant ce temps, les tumeurs non traitées ont atteint plusieurs fois leur taille initiale, alors que les tumeurs traitées ont cessé de croître, suggérant que la dose de radiation localisée était suffisante pour arrêter la progression. Conscients que des traitements répétés pourraient surcharger le foie et la rate en fer, les chercheurs ont ensuite adapté les conditions de synthèse pour obtenir des particules encore plus petites — autour de quatre à cinq nanomètres — suffisamment petites pour être filtrées par les reins. Ces particules réduites ont conservé leur cargaison radioactive de façon stable mais ont été rapidement excrétées dans la vessie, réduisant l’accumulation à long terme dans les organes majeurs.
Ce que cela pourrait signifier pour les soins du cancer à venir
Pour les non‑spécialistes, le message clé est que les chercheurs ont mis au point une plateforme nanoparticulaire unique et flexible qui peut être associée à de nombreux métaux radioactifs différents sans réinventer la chimie à chaque fois. Dans des modèles animaux, la même particule de base peut aider à repérer les tumeurs cérébrales, mettre en évidence des caillots sanguins, délivrer la radiation directement dans les tumeurs et même être adaptée pour sortir de l’organisme par les reins. Bien que des travaux supplémentaires soient nécessaires avant que cette approche n’atteigne les patients, elle offre une voie prometteuse pour concevoir des familles d’agents diagnostiques et thérapeutiques partageant le même comportement dans l’organisme, ne différant que par le type de radiation qu’ils transportent. Cette cohérence pourrait simplifier le développement, améliorer les tests de sécurité et, en fin de compte, rendre les outils avancés de médecine nucléaire plus largement accessibles.
Citation: Herraiz, A., Rodríguez-San-Pedro, A., Casquero-Veiga, M. et al. A single-step radiolabeling strategy for PET, SPECT, and therapeutic radionuclides using nanoparticles as a universal chelator. npj Imaging 4, 8 (2026). https://doi.org/10.1038/s44303-026-00142-1
Mots-clés: radiothérapies diagnostiques, nanoparticules, imagerie PET, glioblastome, radiothérapie ciblée