Clear Sky Science · fr
Synucléinopathie accélérée et localisée dans un modèle murin hybride : implications pour les études en tomographie par émission de positons
Pourquoi cette recherche compte
La maladie de Parkinson est surtout connue pour les tremblements et les troubles du mouvement, mais au cœur du cerveau elle débute par de petites altérations difficiles à détecter. Les médecins ont un besoin urgent de méthodes pour repérer ces changements précocement et pour tester rapidement de nouveaux traitements. Cette étude décrit un modèle murin affiné qui reproduit en quelques semaines seulement des caractéristiques clés des lésions cérébrales de type Parkinson, et de façon très localisée, conçu pour être utilisé avec des techniques d’imagerie cérébrale avancées appelées PET. 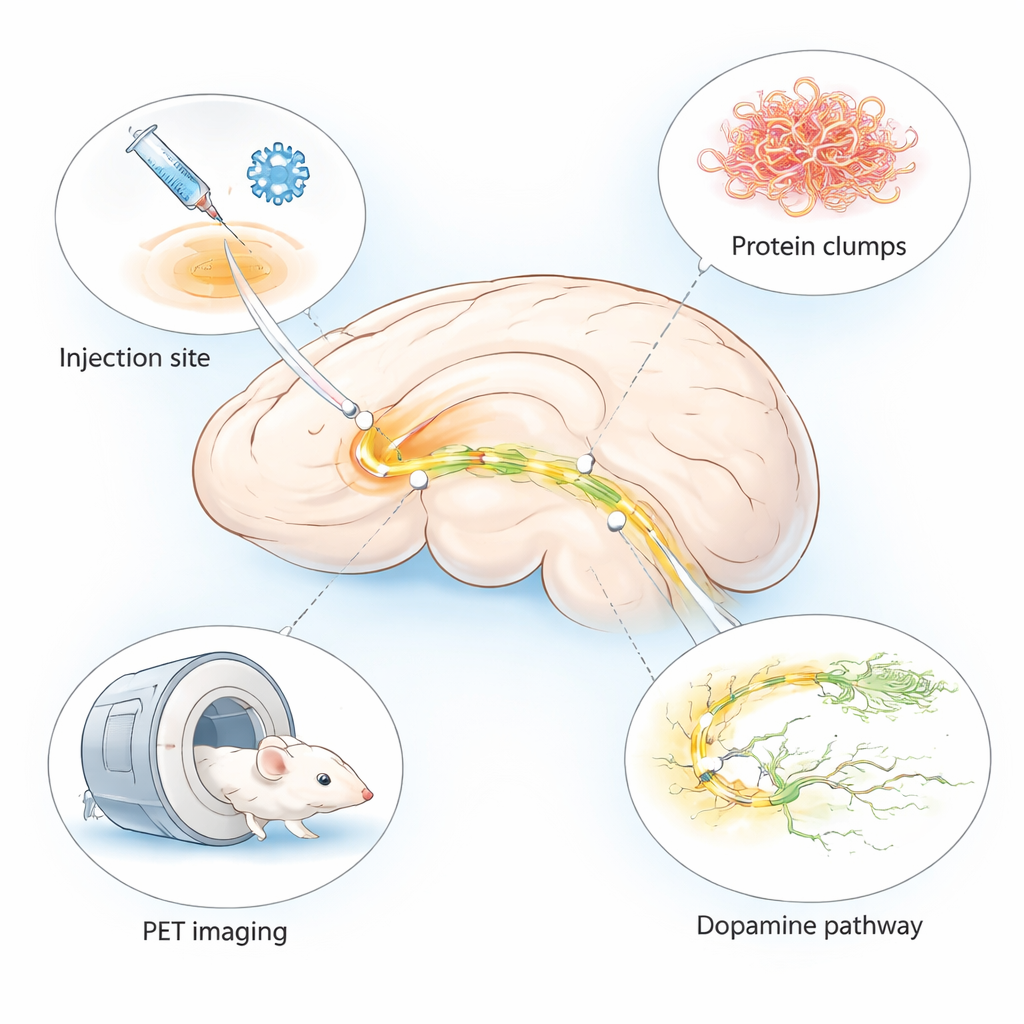
Construire un modèle de maladie plus rapide et plus ciblé
Beauxoup de modèles animaux existants de la maladie de Parkinson mettent des mois à développer des symptômes ou n’exhibent pas l’ensemble des altérations cérébrales observées chez les patients. Les auteurs ont combiné deux approches établies en un modèle « hybride ». Ils ont injecté un virus inoffensif qui pousse les cellules cérébrales à produire de l’alpha‑synucléine humaine — une protéine qui s’agglomère dans la maladie de Parkinson — conjointement avec des fibrilles préformées, qui servent de graines déclenchant l’agglomération supplémentaire. Les deux ont été délivrés dans une petite région liée au mouvement appelée la substance noire, d’un seul côté du cerveau de la souris. Ce dispositif produit des changements localisés mais intenses de type pathologique du côté injecté, tandis que l’autre hémisphère reste relativement sain pour servir de comparaison.
Suivre les agrégats protéiques et la mort neuronale
En seulement deux semaines après l’injection, les souris présentaient des niveaux élevés d’alpha‑synucléine humaine et de sa forme anormale phosphorylée dans la zone cérébrale ciblée. Au microscope, les chercheurs ont observé des structures ressemblant aux corps de Lewy et aux neurites de Lewy, qui sont des caractéristiques de la maladie de Parkinson. Au cours des semaines suivantes, ces dépôts anormaux ont augmenté. Parallèlement, les neurones producteurs de dopamine — essentiels pour un mouvement fluide — ont commencé à disparaître. Les marqueurs de ces cellules ont chuté à environ 60 % du niveau observé du côté non traité à la cinquième semaine, confirmant une perte progressive et nette du système dopaminergique.
Inflammation, effacement des synapses et centrales énergétiques fatiguées
Les cellules immunitaires du cerveau, appelées microglies, sont également passées dans un état hautement actif et inflammatoire autour de la région endommagée. Les marquages pour plusieurs protéines liées à l’inflammation étaient beaucoup plus intenses près des dépôts d’alpha‑synucléine que du côté opposé du cerveau. Plus tard dans le processus, l’équipe a détecté une perte de synapses — ces points de contact minuscules où les neurones communiquent — et des signes de dysfonctionnement des mitochondries, les usines énergétiques des cellules. Ensemble, ces observations montrent que le modèle ne crée pas seulement des agrégats protéiques ; il capture aussi la réaction en chaîne d’inflammation, de défaillance des connexions et de problèmes énergétiques qui contribuent à la mort neuronale dans la maladie de Parkinson. 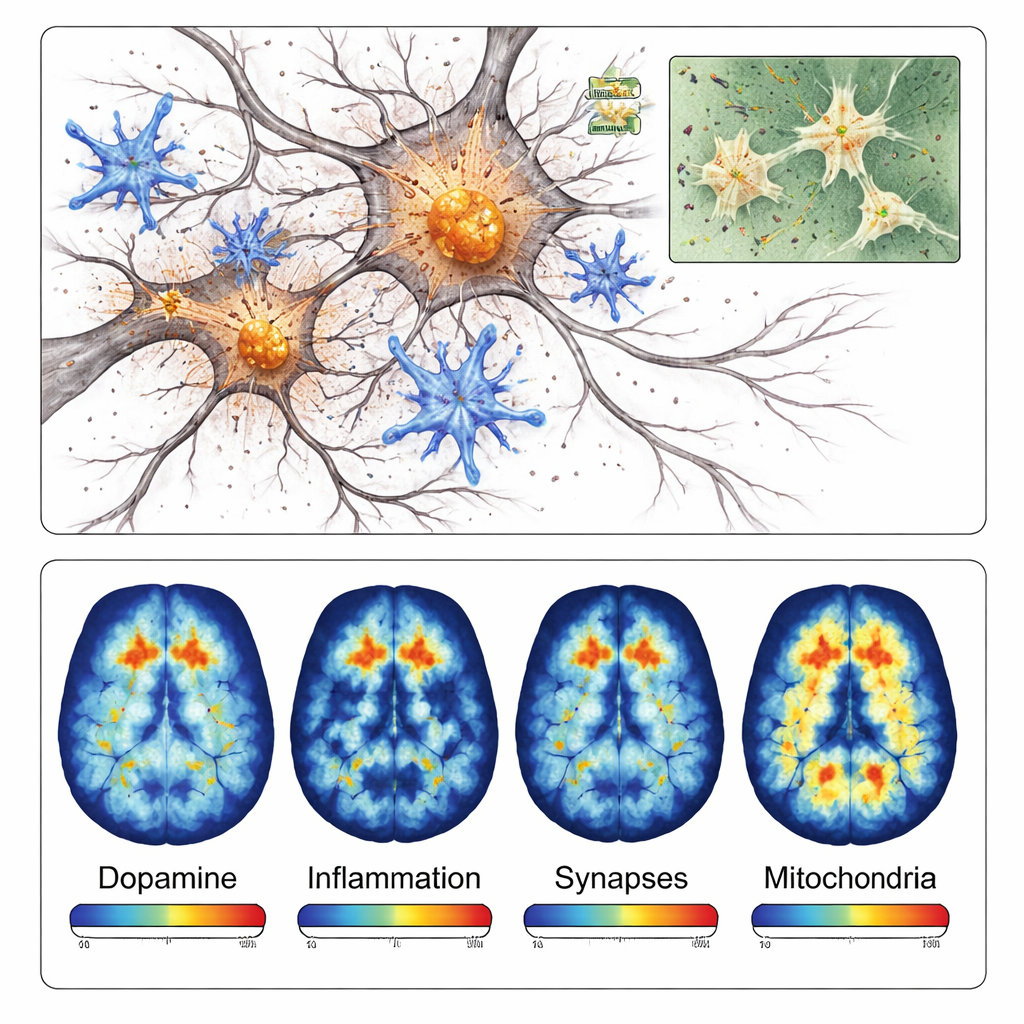
Mettre les scanners PET à contribution
Parce que ce modèle est localisé et se développe rapidement, il se prête particulièrement bien à la tomographie par émission de positons (PET), une technique d’imagerie capable de mesurer des molécules spécifiques dans des cerveaux vivants. Les chercheurs ont testé quatre traceurs PET différents qui se lient aux terminaisons nerveuses dopaminergiques, aux microglies inflammatoires, aux protéines synaptiques et aux enzymes mitochondriales. Dans chaque cas, les acquisitions PET ont montré des signaux plus faibles ou plus élevés du côté injecté d’une manière cohérente avec les observations microscopiques. Par exemple, le traceur ciblant les voies dopaminergiques a montré environ 40 % de signal en moins du côté lésé, tandis que le traceur de l’inflammation a montré plus de 40 % de signal en plus dans la région affectée.
Ce que cela signifie pour les patients et les traitements futurs
Ce nouveau modèle murin rassemble, sur une courte période, nombre des changements clés qui se produisent sur des années dans le cerveau des personnes atteintes de la maladie de Parkinson. Parce que les lésions sont confinées à une petite zone bien définie et peuvent être suivies par PET, les chercheurs peuvent tester plus efficacement de nouveaux traceurs d’imagerie et des thérapies potentielles. Aucun modèle murin ne peut reproduire entièrement la condition humaine, mais cette approche offre un outil puissant et pratique pour rapprocher les travaux fondamentaux des études chez l’homme, aidant en fin de compte à affiner le diagnostic et à accélérer la recherche de traitements meilleurs.
Citation: Xia, C.A., Tsai, HM., Diaz Garcia, S. et al. Accelerated and localized synucleinopathy in a hybrid mouse model: implications for positron emission tomography studies. npj Imaging 4, 7 (2026). https://doi.org/10.1038/s44303-026-00138-x
Mots-clés: Maladie de Parkinson, alpha‑synucléine, synucléinopathie, imagerie PET, modèle murin