Clear Sky Science · fr
Modèles d’équations différentielles ordinaires de la dynamique de réplication de SARS-CoV-2 et efficacité des antiviraux
Pourquoi les chiffres comptent pour un nouveau virus
Lorsque la COVID-19 est apparue, les médecins pouvaient observer ce que le virus faisait aux patients, mais ils ne pouvaient pas facilement prédire qui deviendrait gravement malade ni quand un médicament devait être administré pour être le plus efficace. Cet article de synthèse examine comment les chercheurs ont transformé des mesures virales issues de patients, d’animaux et de cultures cellulaires en « films mathématiques » de l’infection à l’intérieur du corps. Ces modèles utilisent des équations pour suivre la croissance du virus, la réaction de nos cellules et de notre système immunitaire, et la manière dont les antiviraux et les vaccins peuvent faire pencher la balance en notre faveur.
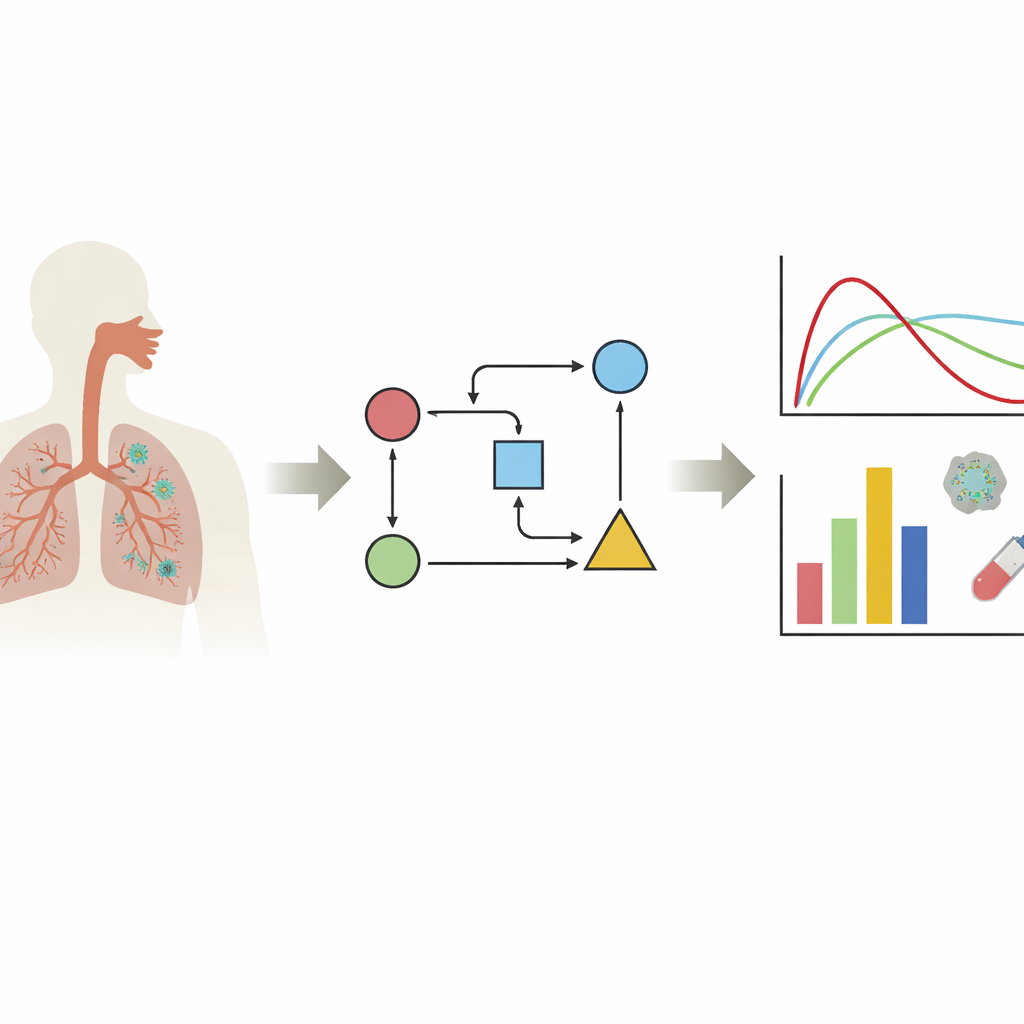
Suivre le virus à l’intérieur du corps
Les auteurs se concentrent sur une famille de modèles appelés modèles limités par les cellules cibles. En termes simples, ces modèles suivent trois acteurs principaux : les cellules saines susceptibles d’être infectées, les cellules déjà infectées et les particules virales libres. En alimentant ces équations avec des données réelles sur les niveaux viraux, les chercheurs peuvent estimer des caractéristiques cachées de l’infection : la vitesse d’infection des cellules, la durée pendant laquelle une cellule infectée produit du virus et la rapidité d’élimination du virus. La synthèse montre que la plupart des travaux portent sur les tissus les plus importants pour la COVID-19 : le nez et les voies respiratoires supérieures et inférieures, tandis que peu de modèles examinent d’autres organes. Un message clé est que le comportement viral peut paraître très différent selon le tissu étudié, le variant viral et la lignée cellulaire de laboratoire utilisée, de sorte qu’il n’existe pas de courbe d’infection « typique » unique.
Ce que nous apprenons sur le système immunitaire
De nombreux modèles ajoutent des couches représentant les premières défenses du système immunitaire et sa réponse plus lente et plus ciblée. Les études axées sur la première ligne de défense suggèrent qu’une activité rapide et bien chronométrée des cellules immunitaires innées et des molécules de signalisation peut atténuer l’infection, mais l’élimine rarement à elle seule. D’autres travaux mettent en avant le rôle crucial des cellules T et des anticorps pour contrôler finalement le virus. Les modèles captent aussi un aspect plus sombre : si la réponse ciblée est tardive ou mal orientée, les mêmes mécanismes censés nous protéger peuvent alimenter des « tempêtes de cytokines » délétères, où un excès de signaux inflammatoires endommage les tissus sains. Dans ces simulations, le délicat équilibre entre activité immunitaire utile et nuisible décide souvent si la maladie reste bénigne ou devient potentiellement mortelle.
Quand les médicaments et les vaccins sont les plus efficaces
Parce que les équations peuvent être lancées encore et encore sous différentes hypothèses, elles sont des outils puissants pour tester des stratégies thérapeutiques sur ordinateur avant de les essayer chez l’humain. Dans de nombreuses études, les modèles s’accordent sur un point central : les antiviraux sont les plus efficaces lorsqu’ils sont administrés très tôt, avant que le virus n’ait atteint son pic et n’ait infecté la majorité des cellules disponibles. Les traitements qui empêchent le virus de copier son matériel génétique apparaissent particulièrement prometteurs, notamment en association avec d’autres médicaments agissant par des mécanismes différents. À l’inverse, un traitement tardif tend à avoir peu d’impact dans les simulations, sauf si plusieurs médicaments puissants sont combinés. La vaccination est systématiquement prédite comme plus efficace que les seuls médicaments, principalement en préparant le système immunitaire à reconnaître rapidement le virus et à limiter la durée des taux viraux élevés.
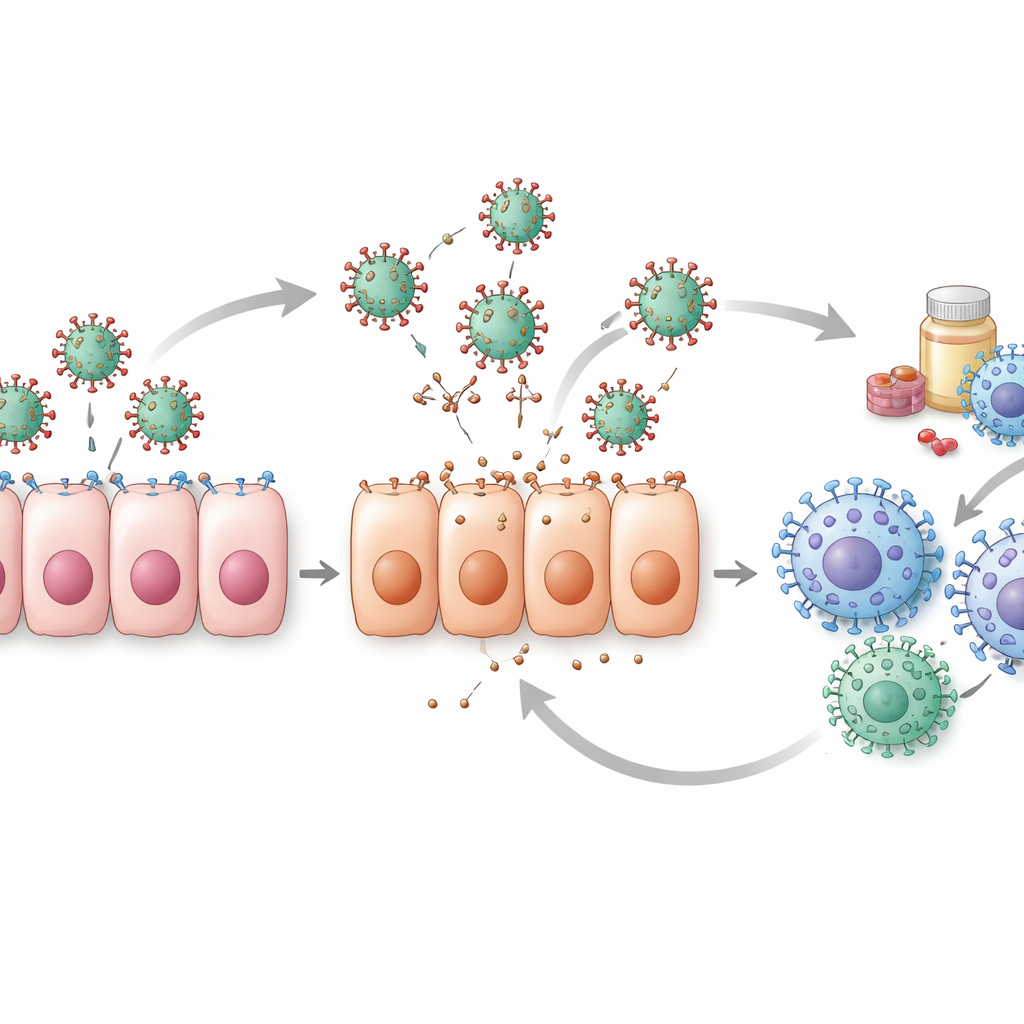
Défis cachés dans les données
La synthèse met aussi en lumière les faiblesses derrière les chiffres. La plupart des jeux de données cliniques ne commencent qu’après que les personnes ressentent déjà des symptômes, ce qui signifie que les modèles manquent souvent les premiers jours cruciaux de l’infection, lorsque les niveaux viraux augmentent le plus rapidement. Sans ces mesures précoces, différentes combinaisons de paramètres peuvent expliquer les mêmes données, rendant difficile la certitude sur la bonne explication. Seule une minorité d’études effectue des vérifications rigoureuses pour savoir si leurs estimations de paramètres sont réellement uniques et fiables. Les études animales et les expérimentations en culture cellulaire aident à combler certaines lacunes, notamment pour les premiers temps, mais les différences entre espèces et systèmes de laboratoire limitent la transposabilité directe de ces résultats à l’humain.
Ce que cela signifie pour l’avenir
Pour un non-spécialiste, la conclusion est que des modèles mathématiques soigneusement construits ont considérablement amélioré notre compréhension du comportement de SARS-CoV-2 dans l’organisme et de la manière dont le moment, les combinaisons de médicaments et la vaccination préalable influent sur les résultats. Les modèles s’accordent largement sur le fait qu’une intervention précoce et forte — en particulier grâce à la vaccination et à des antiviraux administrés à temps — offre au système immunitaire la meilleure chance de l’emporter, tandis que des réponses différées, qu’elles proviennent de l’organisme ou du traitement, sont associées à des formes plus sévères de la maladie. Les auteurs soulignent en parallèle que ces outils ne valent que par la qualité des données qui les alimentent. Pour se préparer aux futurs variants ou à de nouveaux virus, ils appellent à des prélèvements cliniques plus riches et plus précoces et à des mesures immunitaires plus larges, afin que les « chiffres derrière l’infection » puissent guider des décisions plus rapides et plus précises lors de flambées réelles.
Citation: Kapischke, T., Herrmann, S.T., Bertzbach, L.D. et al. Ordinary differential equation models of SARS-CoV-2 replication dynamics and antiviral drug efficacies. npj Viruses 4, 17 (2026). https://doi.org/10.1038/s44298-026-00183-8
Mots-clés: Dynamique virale de SARS-CoV-2, modélisation intra-hôte, calendrier de la thérapie antivirale, réponse immunitaire, vaccination contre la COVID-19