Clear Sky Science · fr
Rôles divergents des chaperons Hsp70 dans la sécrétion des protéines des orthoflavivirus et la formation de virions
Pourquoi de petits assistants de choc thermique comptent pour des virus qui infectent le cerveau
Les virus transportés par les tiques et les moustiques, comme le virus de l’encéphalite à tiques et le virus West Nile, peuvent envahir le cerveau et provoquer des maladies graves, et il n’existe toujours pas de médicaments spécifiques pour les arrêter. Cette étude examine comment ces virus détournent un ensemble d’« assistants » protéiques de l’hôte, appelés chaperons Hsp70, pour assembler et libérer de nouvelles particules virales. Comme les protéines Hsp70 sont déjà étudiées comme cibles thérapeutiques en cancérologie, mieux comprendre cette relation pourrait ouvrir de nouvelles voies pour traiter des infections virales dangereuses sans attaquer les virus directement.
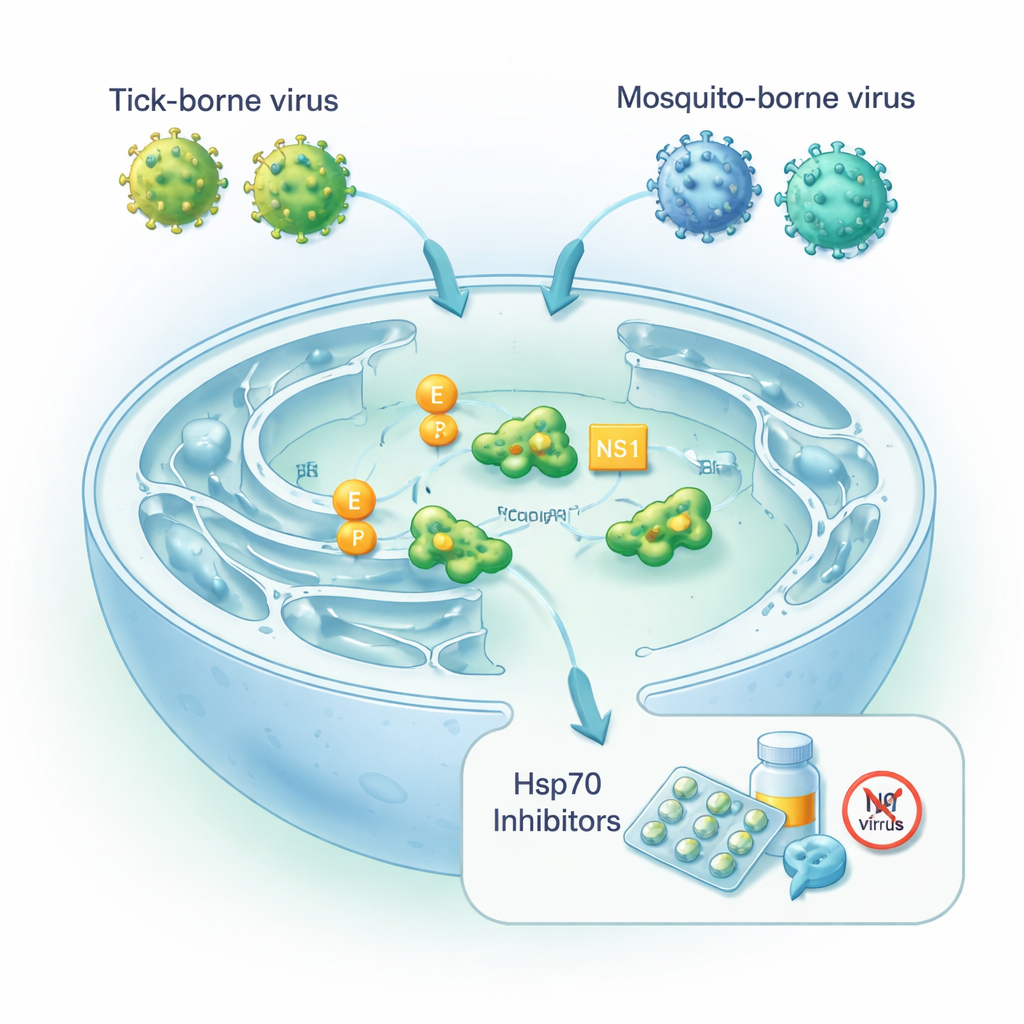
Des virus qui s’appuient sur la machinerie de repliement de la cellule
Les orthoflavivirus sont de petits virus à ARN dont le génome code pour une longue polyprotéine qui doit être clivée et repliée en plusieurs éléments fonctionnels. Deux composants viraux clés sont la protéine d’enveloppe E, qui recouvre la particule virale et lui permet d’entrer dans de nouvelles cellules, et la protéine non structurale NS1, qui aide le virus à copier son génome et peut être sécrétée pour manipuler le système immunitaire. Tout cela se déroule dans le réticulum endoplasmique, la partie de la cellule où de nombreuses protéines sont repliées et préparées pour l’export. Là, la cellule s’appuie sur les chaperons Hsp70, y compris une forme résidente appelée BiP, pour empêcher les nouvelles protéines de se désordonner sous stress. Les auteurs ont cherché à savoir dans quelle mesure les orthoflavivirus neurotropes transmis par les tiques et les moustiques dépendent de ces chaperons pour assembler des particules infectieuses.
Des interactions directes entre protéines virales et Hsp70
En utilisant des cellules modifiées pour surexprimer certaines protéines virales, ainsi que des cellules infectées par des virus authentiques, les chercheurs ont précipité BiP ou Hsp70 et vérifié quels partenaires viraux les accompagnaient. Ils ont constaté que BiP et Hsp70 formaient systématiquement des complexes avec la protéine d’enveloppe E de plusieurs orthoflavivirus, qu’ils soient transmis par les tiques ou les moustiques. Cela suggère que le repliement de E dans le réticulum endoplasmique est guidé par ces chaperons. Le tableau était plus sélectif pour NS1 : BiP et Hsp70 se liaient fortement à NS1 des virus transmis par les tiques, comme le virus de l’encéphalite à tiques et le virus Langat, mais pas à NS1 des virus transmis par les moustiques, comme West Nile et Usutu. Ces différences reflètent probablement des variations dans la glycosylation et le repliement de NS1, indiquant que des virus apparentés n’utilisent pas forcément les mêmes voies de l’hôte.
Bloquer les chaperons réduit fortement la production virale
Comme les protéines Hsp70 sont ciblables par des médicaments, l’équipe a testé deux petites molécules qui interfèrent avec différentes parties de la machinerie des chaperons. YM‑1 cible le domaine de liaison au nucléotide, bloquant les Hsp70 dans un état inactif, tandis que PES‑Cl bloque la poche de liaison au substrat qui saisit normalement les protéines clientes. À des doses qui laissaient la plupart des cellules en vie, YM‑1 a réduit drastiquement la quantité de virus infectieux libérée pour les quatre orthoflavivirus testés et a diminué la quantité de protéine d’enveloppe retrouvée dans les milieux de culture, ce qui indique un blocage général de la formation ou de la libération des particules. PES‑Cl, en revanche, a eu peu d’effet sur les titres infectieux ou les niveaux de protéine d’enveloppe, même s’il affaiblissait l’interaction physique entre Hsp70/BiP et la protéine d’enveloppe dans les tests de liaison. Cela suggère qu’une interférence brève avec le site de saisie n’est pas suffisante pour paralyser l’assemblage viral, tandis que l’arrêt du cycle énergétique du chaperon l’est.
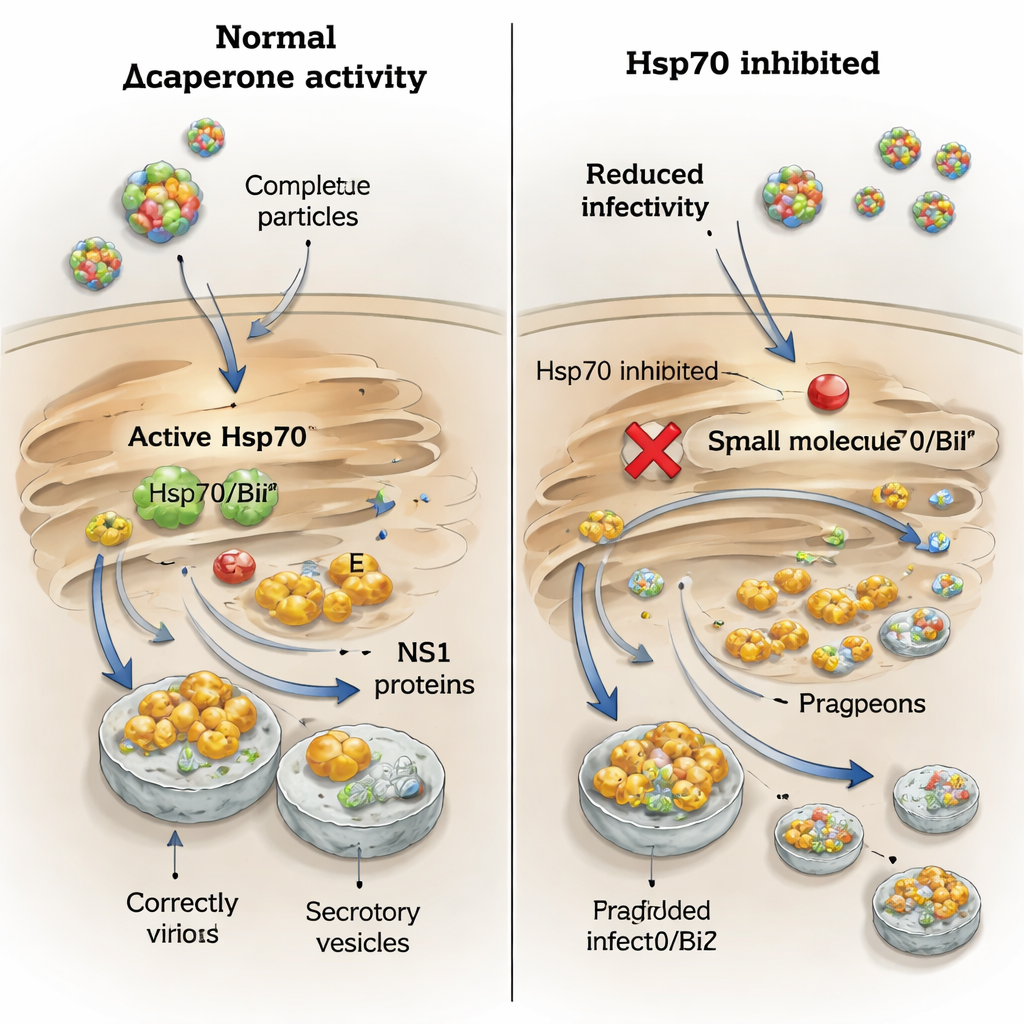
Une dépendance particulière des virus transmis par les tiques à BiP pour NS1
L’histoire pour NS1 est plus nuancée. Lorsque les cellules infectées ont été traitées par PES‑Cl, la sécrétion de NS1 des virus de l’encéphalite à tiques et Langat a chuté fortement, tandis que NS1 des virus West Nile et Usutu n’a pas été affectée. Cela reflète la découverte précédente selon laquelle seules les NS1 d’origine tique se lient fortement à BiP et Hsp70. Pour zoomer sur le rôle de BiP, les auteurs ont utilisé des petits ARN interférents pour diminuer spécifiquement les niveaux de BiP. Cela a réduit les quantités des protéines d’enveloppe et de NS1 à l’intérieur des cellules et dans le milieu pour les virus de l’encéphalite à tiques et West Nile, cependant les titres de virus infectieux ont diminué seulement modestement. Lorsque les cellules appauvries en BiP ont été traitées par des médicaments bloquant la dégradation des protéines, les niveaux intracellulaires de NS1 ont rebondi mais sa sécrétion ne l’a pas fait, montrant que BiP est nécessaire non seulement pour protéger NS1 de la dégradation mais aussi pour la guider sur la voie sécrétoire.
Ce que cela implique pour les stratégies antivirales futures
Pour un non‑spécialiste, le message principal est que ces virus qui infectent le cerveau dépendent fortement des assistants de repliement protéique de la cellule pour construire leur enveloppe externe et, pour certaines espèces, pour sécréter NS1 comme arme. Un inhibiteur large des chaperons comme YM‑1 peut donc réduire fortement la production de particules infectieuses de plusieurs virus apparentés à la fois, bien que ses effets puissants dépassent probablement un seul chaperon et puissent aussi mettre en tension les cellules saines. Des approches plus ciblées, axées peut‑être sur la façon dont BiP et Hsp70 traitent des clients viraux spécifiques comme NS1, pourraient un jour permettre de concevoir des traitements moins susceptibles d’engendrer des résistances virales tout en préservant la plupart du repliement protéique normal de l’hôte.
Citation: Blank, L., Lorenz, C. & Steffen, I. Divergent roles of Hsp70 chaperones in orthoflavivirus protein secretion and virion formation. npj Viruses 4, 8 (2026). https://doi.org/10.1038/s44298-026-00175-8
Mots-clés: orthoflavivirus, chaperon Hsp70, virus de l’encéphalite à tiques, virus West Nile, cibles médicamenteuses antivirales