Clear Sky Science · fr
La protéine G soluble du virus respiratoire syncytial favorise la dissémination virale via l’amorçage du NLRP3 médié par TLR2 et la pyroptose
Pourquoi ce virus pulmonaire concerne tout le monde
Le virus respiratoire syncytial, ou VRS, est surtout connu comme une menace hivernale pour les nourrissons, mais il envoie aussi de nombreux personnes âgées et sujets immunodéprimés à l’hôpital. Même avec de nouveaux vaccins et des anticorps protecteurs, le VRS réinfecte encore les gens de façon répétée et peut provoquer de graves lésions pulmonaires. Cette étude examine une protéine virale peu connue, une forme soluble de la protéine G du VRS, et met au jour comment elle pourrait préparer discrètement les cellules pulmonaires à une inflammation explosive et aider le virus à se propager plus efficacement dans les voies respiratoires.
Une protéine virale sécrétée qui voyage en amont de l’infection
Le VRS porte à sa surface une protéine d’attachement appelée G qui l’aide à se fixer aux cellules des voies aériennes. Fait inhabituel, les cellules infectées libèrent aussi de grandes quantités d’une version libre de cette protéine, connue sous le nom de G soluble. Les chercheurs ont montré que des cellules pulmonaires infectées en laboratoire peuvent libérer des niveaux très élevés de G soluble dans leur environnement. Parce que cette forme peut diffuser loin du foyer d’infection initial, elle peut atteindre des cellules voisines pas encore infectées, préparant ainsi un remaniement plus vaste de la muqueuse pulmonaire que ce que provoquerait le virus seul.
Le G soluble, clé polyvalente des surfaces cellulaires
En combinant microscopie, tests biochimiques d’extraction et traitements enzymatiques, l’équipe a cartographié la manière dont le G soluble s’attache aux cellules. Ils ont constaté qu’il peut se lier à des chaînes sucrées appelées glycosaminoglycanes, ainsi qu’à un récepteur connu du VRS nommé CX3CR1. Surtout, le G soluble se lie aussi à une molécule détectrice de motifs présente sur les cellules immunitaires et des voies aériennes, TLR2. Un petit motif de la protéine G, connu sous le nom de CX3C, s’est avéré important pour une forte liaison à CX3CR1 et pour un recrutement efficace de TLR2. Cela signifie que le G soluble peut d’abord être capté de manière lâche à la surface cellulaire, puis engager des récepteurs plus spécifiques qui contrôlent la réponse des cellules aux menaces.
Amorcer les cellules pulmonaires à un type de mort cellulaire inflammatoire
L’engagement de TLR2 par le G soluble s’est révélé loin d’être anodin. Dans des cellules immunitaires rapporteurs et des lignées cellulaires pulmonaires humaines, le G soluble a activé la voie de signalisation MyD88–NF-κB en aval de TLR2, entraînant la libération de messagers inflammatoires tels que l’IL-6 et l’IL-8. Parallèlement, il a augmenté la production de composants d’un « système d’alarme » moléculaire appelé inflammasome NLRP3 et d’enzymes qui génèrent des molécules réactives comme le monoxyde d’azote et des radicaux oxygénés. Pris isolément, ces changements causaient seulement des dommages modestes. Mais lorsque les cellules amorcées étaient ensuite infectées par le VRS, le second coup déclenchait l’assemblage complet de l’inflammasome, l’activation de l’enzyme caspase‑1, la formation de pores dans la membrane cellulaire et une forme incendiaire de mort cellulaire connue sous le nom de pyroptose. Ce processus perforait les cellules, déversait des contenus inflammatoires et coïncidait avec des quantités plus élevées de virus infectieux libérées dans le milieu de culture.
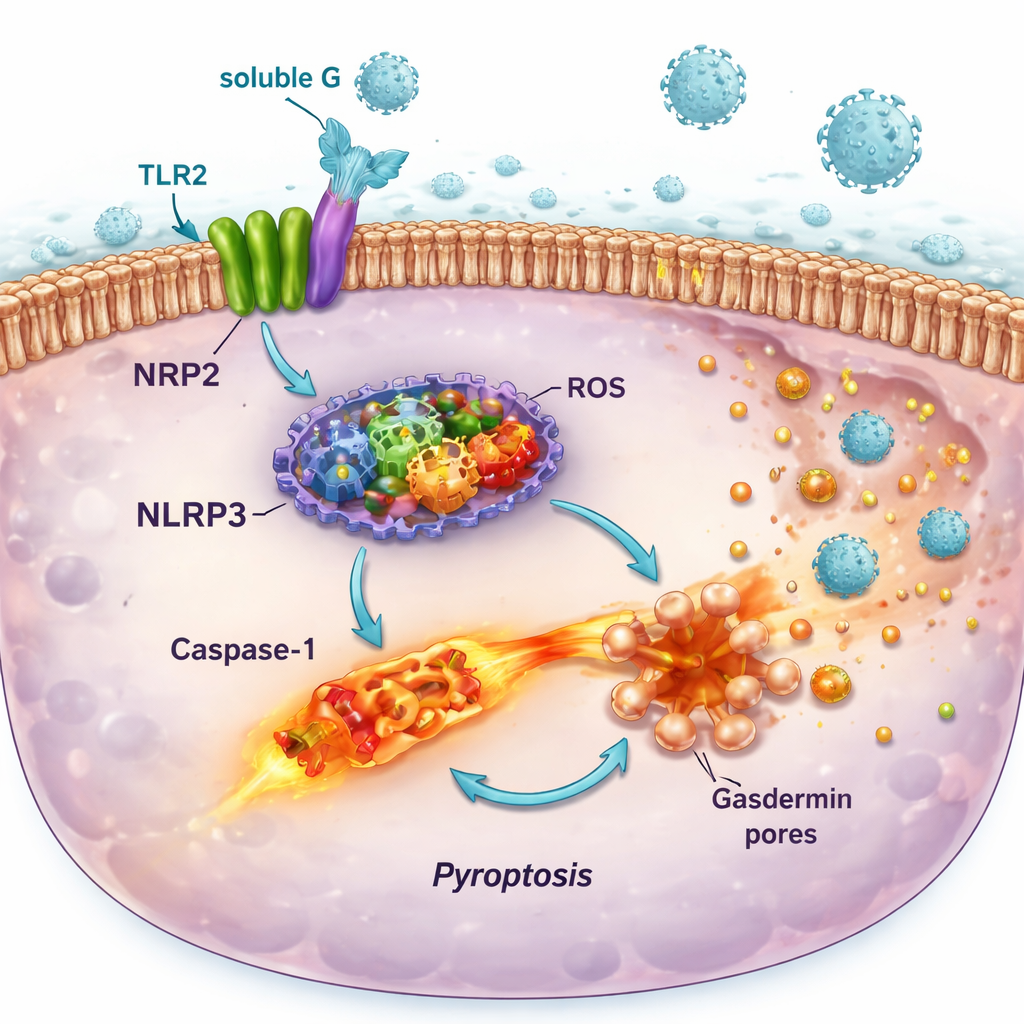
Comment cette réaction en chaîne peut aggraver la maladie pulmonaire
L’effet pro‑nécrotique du G soluble était le plus marqué dans les cellules épithéliales des voies aériennes—les mêmes cellules que le VRS préfère infecter—et dépendait de l’inflammasome NLRP3, car un inhibiteur spécifique de NLRP3 préservait en grande partie la viabilité cellulaire. En revanche, certaines cellules immunitaires riches en TLR2 mais pauvres en récepteur CX3CR1 n’ont pas subi de mort lytique importante dans les mêmes conditions. Ce schéma suggère que le VRS utilise le G soluble pour affaiblir et détruire sélectivement la couche protectrice des voies respiratoires tout en préservant certaines cellules immunitaires capables de continuer à produire des signaux. Le résultat est un environnement pulmonaire avec plus d’inflammation, plus de débris cellulaires et plus d’occasions pour de nouvelles particules virales de s’échapper et d’infecter les cellules voisines.
Ce que cela implique pour les traitements futurs
Pour un non‑spécialiste, le message clé est que le VRS ne mise pas uniquement sur les dommages directs de l’invasion virale. En libérant de grandes quantités de protéine G soluble, il peut « ramollir » les cellules voisines via TLR2, les rendant plus susceptibles de mourir de façon inflammatoire et de libérer le virus. Ce travail identifie plusieurs étapes de cette chaîne—le G soluble lui‑même, son motif CX3C, TLR2 et l’inflammasome NLRP3—comme des cibles médicamenteuses potentielles. En principe, des thérapies bloquant l’interaction entre le G soluble et TLR2, ou atténuant l’activité de NLRP3, pourraient réduire à la fois les lésions pulmonaires et la dissémination virale. De telles approches pourraient un jour compléter les vaccins et anticorps existants contre le VRS, offrant une meilleure protection aux patients les plus jeunes et les plus vulnérables.
Citation: Meineke, R., Agac, A., Knittler, MC. et al. The soluble G protein of respiratory syncytial virus promotes viral dissemination via TLR2-mediated NLRP3 priming and pyroptosis. npj Viruses 4, 6 (2026). https://doi.org/10.1038/s44298-026-00172-x
Mots-clés: virus respiratoire syncytial, protéine G soluble, inflammasome TLR2, pyroptose, inflammation pulmonaire