Clear Sky Science · fr
Thérapie hormonale ménopausique et risque de maladies neuropsychiatriques : une étude de randomisation mendélienne ciblant des médicaments
Pourquoi cette recherche est importante
Beaucoup de femmes se demandent si la prise d’hormones autour de la ménopause protégera leur cerveau ou, au contraire, l’exposera à des troubles comme la perte de mémoire, la dépression ou l’anxiété. Les médecins sont eux aussi partagés, car les études antérieures ont donné des résultats contradictoires. Cet article utilise une approche génétique, similaire dans son esprit à un essai randomisé à long terme, pour poser une question simple : lorsque les récepteurs aux œstrogènes du cerveau sont modulés de la manière dont pourrait le faire la thérapie hormonale ménopausique, cela modifie‑t‑il le risque de maladie d’Alzheimer ou de troubles mentaux courants ?
Le casse‑tête autour des hormones et du cerveau
Les femmes sont plus susceptibles que les hommes de souffrir de dépression, d’anxiété et de maladie d’Alzheimer. Une idée dominante est que l’œstrogène, une hormone sexuelle féminine majeure, contribue à façonner le cerveau au cours de la vie et peut le protéger — jusqu’à ce que ses niveaux fluctuent ou diminuent à la cinquantaine. Pendant la transition ménopausique, de nombreuses femmes utilisent la thérapie hormonale ménopausique (THM) pour soulager des symptômes tels que les bouffées de chaleur et les troubles du sommeil. Pourtant, les études sur l’impact de la THM sur la santé cérébrale sont discordantes : certaines ont relevé un risque accru de démence, d’autres une protection, et beaucoup n’ont montré aucun effet net. Ces incohérences peuvent provenir de la brièveté des essais, de différences dans les formulations médicamenteuses, et du fait que les femmes présentant des symptômes plus sévères sont plus susceptibles de se voir prescrire des hormones.
Utiliser les gènes comme expérience naturelle
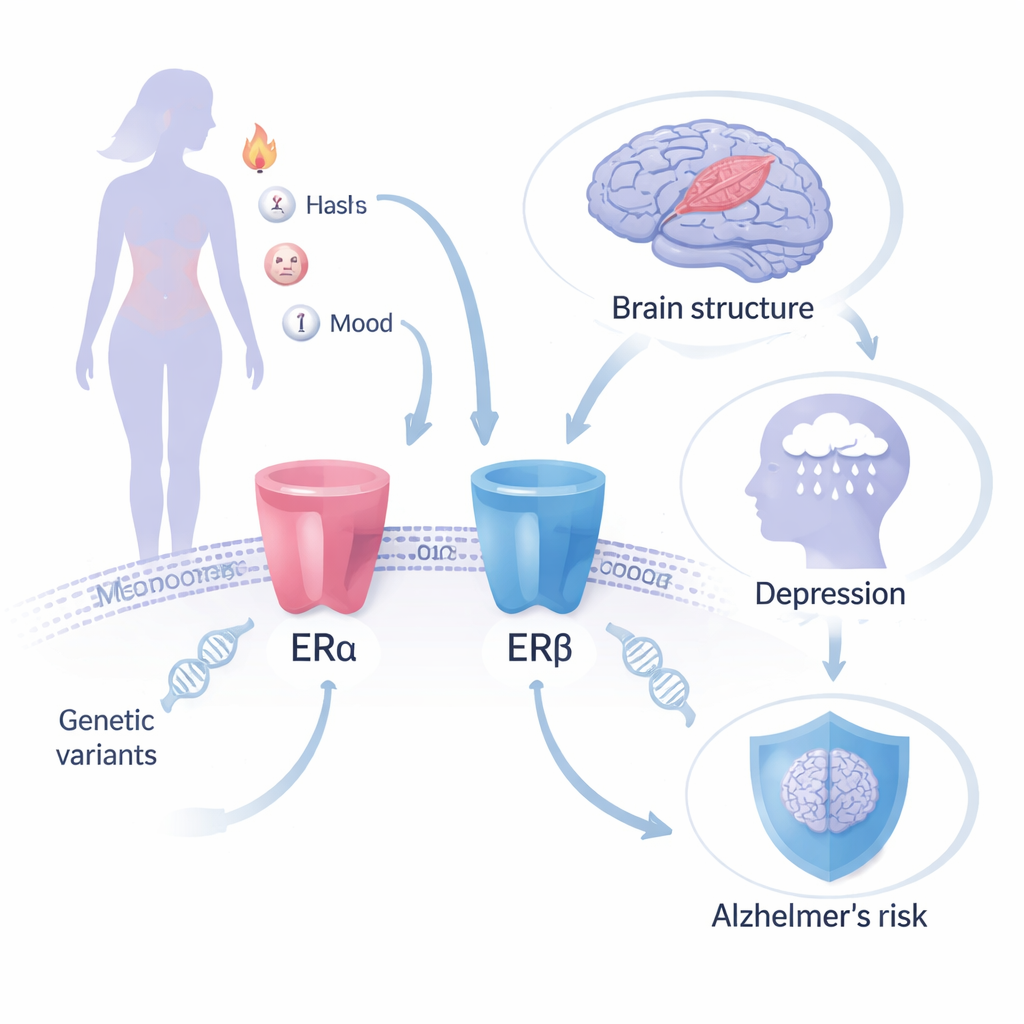
Plutôt que de suivre des femmes prenant des pilules hormonales, les chercheurs ont eu recours à la randomisation mendélienne, une méthode qui utilise des variations génétiques naturellement présentes comme substitut d’un « traitement » attribué aléatoirement sur toute la vie. Ils se sont concentrés sur deux protéines appelées récepteurs aux œstrogènes — ERα et ERβ — que la THM vise à activer. Des variants génétiques spécifiques des gènes codant ces récepteurs (ESR1 et ESR2) ont des effets connus sur des traits « en aval » modifiés par l’action des œstrogènes, comme la densité minérale osseuse, une protéine sanguine qui transporte les hormones sexuelles, et le taux d’hémoglobine. En suivant le lien entre ces variants associés aux récepteurs et de larges jeux de données génomiques sur la maladie d’Alzheimer, la structure cérébrale, la dépression et l’anxiété, l’équipe a pu estimer comment la modulation de chaque récepteur pourrait influencer les risques à long terme pour le cerveau et la santé mentale.
Ce que montraient les preuves génétiques
Les auteurs ont construit trois instruments génétiques : deux capturant l’activité de ERα (via des variants liés à la densité osseuse et à la globuline de liaison aux hormones sexuelles) et un capturant l’activité de ERβ (via un variant lié à l’hémoglobine). Ils ont ensuite combiné ces instruments avec certaines des plus grandes études d’association à l’échelle du génome disponibles sur la maladie d’Alzheimer, des mesures IRM cérébrales (matière grise globale, volume de l’hippocampe et « taches » de la substance blanche liées au vieillissement), la dépression et l’anxiété. Globalement, ils n’ont trouvé aucune preuve convaincante que des variations génétiques simulant des changements dans l’un ou l’autre récepteur aux œstrogènes modifient de façon significative le risque de maladie d’Alzheimer ou affectent ces mesures de la structure cérébrale. Quelques signaux faibles pour des modifications de la matière grise ou du volume hippocampique n’ont pas résisté à la correction statistique, ce qui suggère qu’ils peuvent être dus au hasard plutôt qu’à un effet biologique réel.
Un signal d’alerte pour le risque de dépression
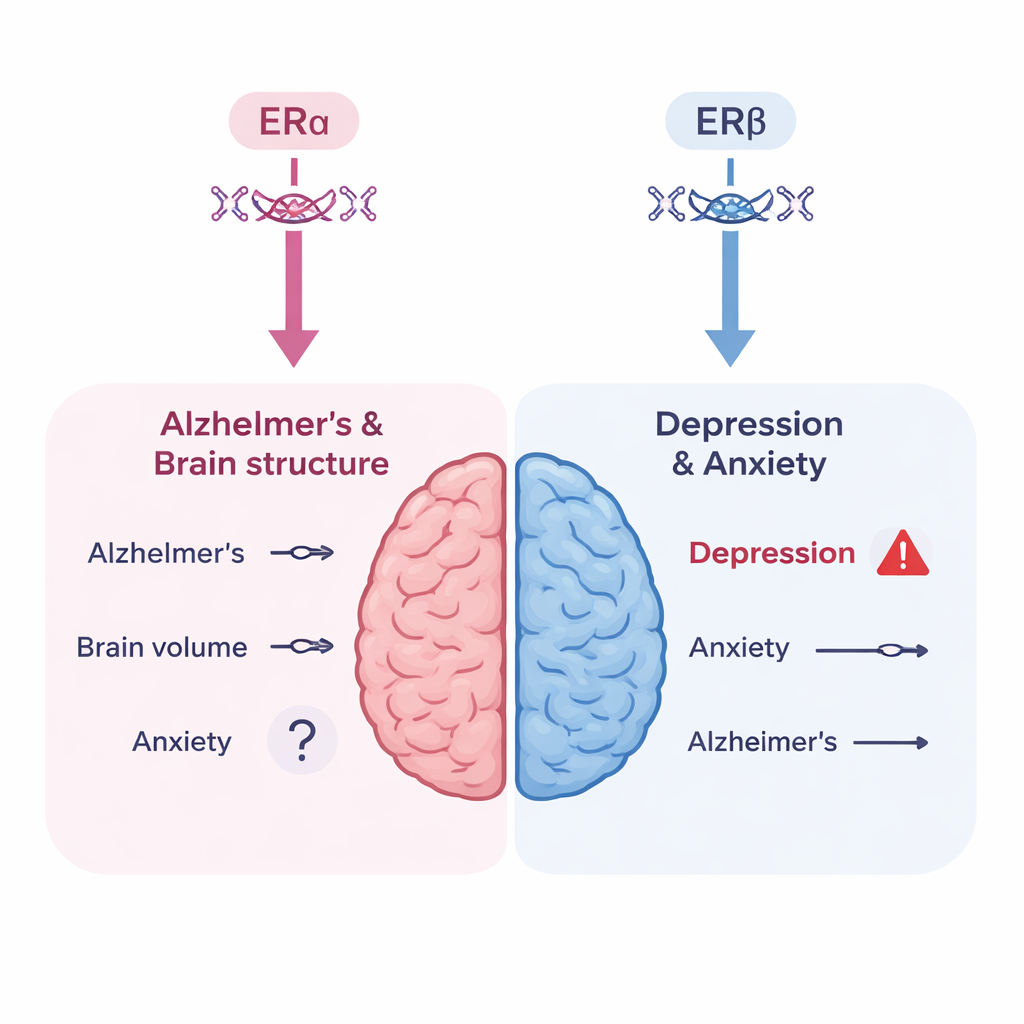
L’histoire était différente pour l’humeur. Lorsque les chercheurs ont examiné l’activité de ERβ, capturée par le proxy génétique basé sur l’hémoglobine, ils ont observé un lien statistiquement robuste avec un risque plus élevé de dépression. Ce résultat concorde avec ce que l’on sait des régions où ERβ est le plus actif dans le cerveau — des zones comme l’hippocampe et le thalamus fortement impliquées dans la régulation de l’humeur. Cependant, les auteurs mettent en garde que le proxy basé sur l’hémoglobine est imparfait : une hémoglobine basse peut elle‑même contribuer à la fatigue et à une humeur dépressive, ce qui peut brouiller l’interprétation. Ils n’ont trouvé aucune preuve génétique solide que l’activité de ERα à elle seule augmente le risque de dépression, et seulement une indication suggestive et non définitive que ERα pourrait être liée à l’anxiété. Il est important de noter que des effets génétiques opérant de façon continue depuis la naissance ne sont pas identiques au fait de commencer une THM à la cinquantaine, si bien que ces résultats ne doivent pas être interprétés comme une prédiction directe d’un schéma thérapeutique particulier.
Ce que cela signifie pour les femmes et leurs médecins
Pour des décisions du quotidien, cette étude suggère que cibler les récepteurs aux œstrogènes de manière similaire à la THM n’augmente ni ne diminue de façon nette le risque à vie de maladie d’Alzheimer, ni ne provoque de changements majeurs dans la structure cérébrale, du moins chez les personnes d’ascendance européenne. En parallèle, le résultat liant ERβ à la dépression souligne que les circuits cérébraux sensibles aux hormones sont associés à l’humeur, et que différents récepteurs aux œstrogènes peuvent avoir des implications distinctes pour la santé mentale. Ce travail ne remplace pas les essais cliniques, mais il offre une « vérification de réalité » génétique puissante qui peut aider à affiner les futures thérapies hormonales et orienter la recherche vers des traitements plus sûrs et mieux adaptés pour les femmes traversant la ménopause.
Citation: Schindler, L.S., Gill, D., Oppenheimer, H. et al. Menopausal hormone therapy and risk of neuropsychiatric disease: a drug target Mendelian randomisation study. npj Womens Health 4, 10 (2026). https://doi.org/10.1038/s44294-026-00130-1
Mots-clés: thérapie hormonale ménopausique, récepteurs aux œstrogènes, maladie d’Alzheimer, risque de dépression, randomisation mendélienne