Clear Sky Science · fr
L'expression d'IL10RB dans les cellules cancéreuses est associée à des changements évolutifs qui solidifient la résistance au traitement
Pourquoi certains cancers refusent de rester vaincus
Les traitements contre le cancer ont fait d'énormes progrès, et pourtant de nombreuses tumeurs réapparaissent, se propagent ou cessent de répondre aux médicaments. Cette étude explore pourquoi certaines cellules cancéreuses deviennent particulièrement difficiles à éliminer et comment une molécule de surface peu connue, appelée IL10RB, pourrait agir comme un commutateur caché aidant les tumeurs à résister à la fois à la chimiothérapie et aux immunothérapies modernes — et comment le bloquer pourrait rétablir l'avantage au profit du système immunitaire.
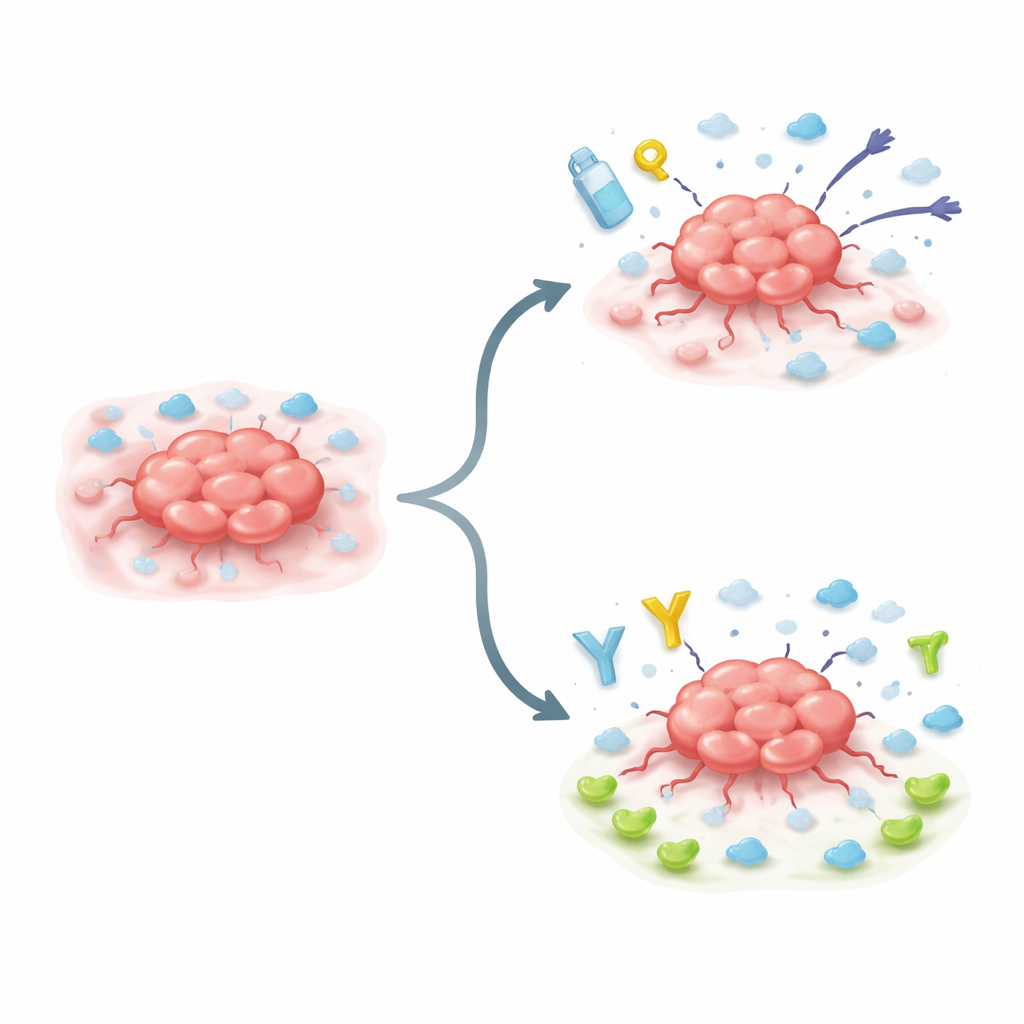
Une étape morphologique dans l'évolution tumorale
Beaucoup de cancers agressifs traversent un processus de transformation appelé transition épithélio-mésenchymateuse. En termes simples, des cellules auparavant bien ordonnées relâchent leurs attaches, deviennent plus mobiles et adoptent des caractéristiques associées aux cellules souches, qui sont plus robustes et adaptatives. Les chercheurs se sont concentrés sur des cellules cancéreuses poussées dans cet état par une protéine de contrôle maîtresse appelée Snail. Ils ont découvert qu'une fois Snail active, elle augmente fortement la production d'IL10RB à la surface de ces cellules, marquant une étape évolutive vers une tumeur plus tenace et résistante aux traitements.
Un commutateur qui rend le cancer plus coriace
Pour comprendre ce que fait réellement IL10RB, l'équipe a modulé son niveau dans des lignées cellulaires cancéreuses de souris et humaines. En diminuant IL10RB, les cellules tumorales à croissance rapide et contrôlées par Snail perdaient une partie de leur capacité à se multiplier, à adhérer aux surfaces et à envahir les tissus environnants. En forçant d'autres cellules cancéreuses à produire davantage d'IL10RB, les cellules changeaient de forme, développant des prolongements en forme de tentacules utilisés pour creuser dans les tissus voisins. Ces cellules riches en IL10RB devenaient plus invasives, adhéraient plus fermement à leur environnement et étaient plus difficiles à tuer avec des chimiothérapies courantes, même si elles se divisaient parfois plus lentement. Au niveau génétique, la surexpression d'IL10RB activait un vaste programme de changements liés à la dissémination, à la survie et à la résistance médicamenteuse.
Quand le traitement se retourne contre l'organisme
L'histoire devient encore plus inquiétante dans des expériences vivantes chez la souris. Les tumeurs chargées en IL10RB ne croissaient pas toujours le plus rapidement, mais elles étaient nettement plus dangereuses pour l'hôte. Une chimiothérapie standard qui réduisait les tumeurs ordinaires pouvait en réalité aggraver les tumeurs riches en IL10RB, accélérant leur propagation vers des organes distants. Ces tumeurs déformaient aussi le système immunitaire des animaux. À l'intérieur et autour des tumeurs, des cellules immunitaires tueuses clés s'épuisaient et étaient surchargées, tandis que dans la rate — le réservoir immunitaire de l'organisme — le nombre et la fonction des cellules T et des cellules NK bénéfiques chutaient fortement. Le cancer ne se contentait pas d'éviter les médicaments ; il désarmait silencieusement les défenses de l'organisme.
Renverser la situation avec des anticorps ciblés
Comme IL10RB fait également partie de la signalisation immunitaire normale, il y avait une inquiétude selon laquelle le cibler pourrait faire plus de mal que de bien. Pour tester cela, les chercheurs ont mis au point des anticorps qui bloquent spécifiquement IL10RB. Dans plusieurs modèles murins de cancer, y compris des cancers des os et du côlon avec tumeurs locales et métastases disséminées, ces anticorps ont réduit la taille des tumeurs et prolongé la survie, souvent après une ou deux doses seulement. Le bénéfice dépendait fortement d'un type particulier de cellule immunitaire : les cellules T CD8 positives, spécialisées dans l'élimination des cellules anormales. Lorsque ces cellules T tueuses étaient supprimées expérimentalement, le bénéfice disparaissait. Fait important, le blocage d'IL10RB n'a pas anéanti les cellules immunitaires normales, mais a restauré leur capacité à attaquer le cancer, et cela a fonctionné sur plusieurs types tumoraux différents.
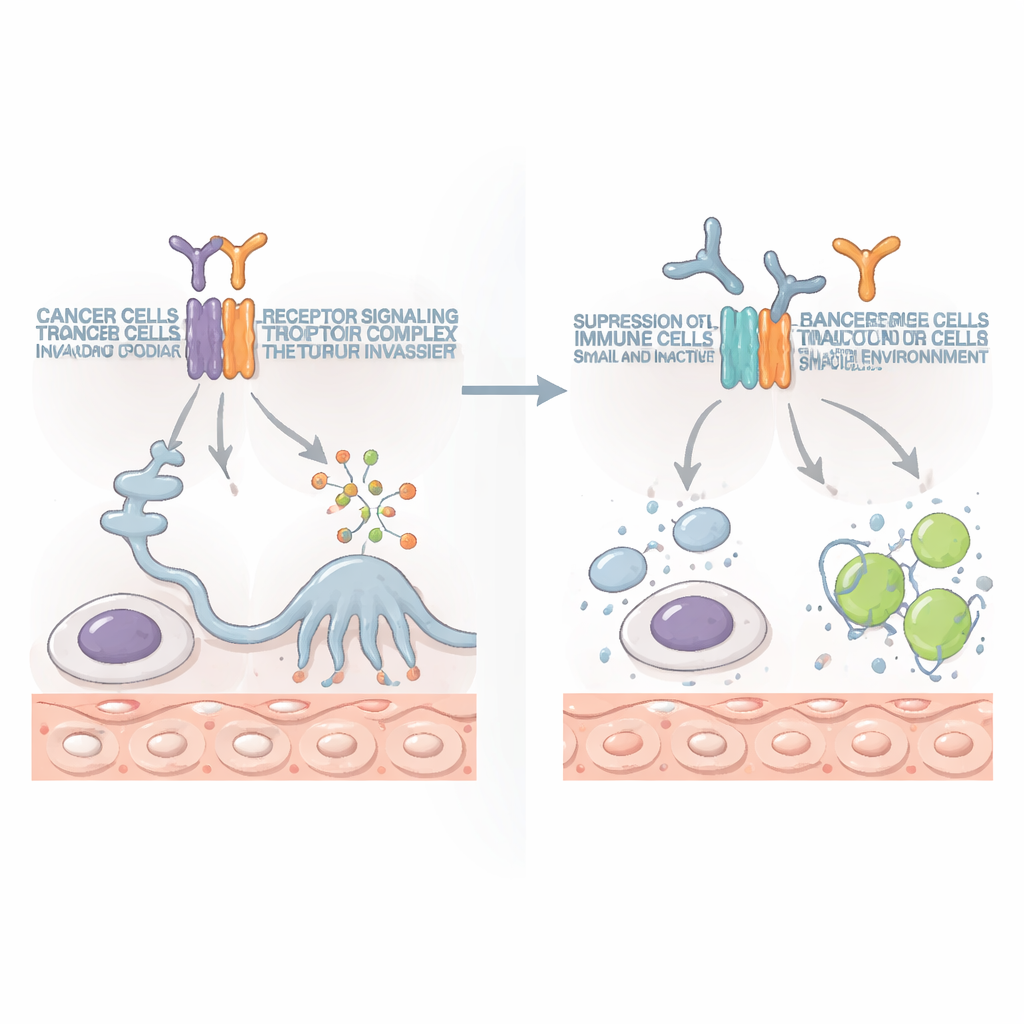
Un nouvel allié pour l'immunothérapie moderne
Aujourd'hui, les médicaments qui relâchent les « freins » immunitaires, comme les bloqueurs de PD-1, ont transformé le traitement de certains cancers mais ne bénéficient qu'à une minorité de patients. Dans cette étude, les anticorps bloquant IL10RB, pris seuls, ont surpassé le blocage de PD-1 dans certains modèles. Lorsqu'ils étaient combinés, les deux se renforçaient mutuellement : les tumeurs diminuaient davantage, se propageaient moins et, chez certains animaux, disparaissaient complètement. La combinaison augmentait le nombre et la vigueur des cellules T tueuses et des cellules NK, qui produisaient davantage de molécules anti-cancer et menaient des attaques plus puissantes contre les cellules tumorales.
Ce que cela signifie pour les soins oncologiques futurs
Pris ensemble, ces résultats suggèrent qu'IL10RB marque et soutient un stade évolutif tardif et durci du cancer — un stade moins axé sur la croissance rapide et davantage sur la survie, la dissémination et l'évasion immunitaire. En bloquant IL10RB, il pourrait être possible de retirer ces protections, d'empêcher la chimiothérapie de se retourner contre l'organisme et de rendre les immunothérapies existantes plus efficaces. Bien que des travaux supplémentaires sur des échantillons humains et des études de sécurité rigoureuses soient encore nécessaires, IL10RB émerge ici comme une nouvelle cible prometteuse pour lutter contre certains des cancers les plus résistants aux traitements.
Citation: Kudo-Saito, C., Ozawa, H., Imazeki, H. et al. IL10RB expression in cancer cells is associated with evolutionary changes to solidify treatment resistance. BJC Rep 4, 11 (2026). https://doi.org/10.1038/s44276-026-00211-3
Mots-clés: résistance au traitement, évolution du cancer, immunothérapie, microenvironnement tumoral, IL10RB