Clear Sky Science · fr
Une enquête génomique révèle l’émergence d’une lignée dominante multirésistante dans les populations de Proteus mirabilis
Pourquoi ce germe hospitalier vous concerne
Pour beaucoup, les infections urinaires sont une gêne douloureuse et occasionnelle. Mais dans les hôpitaux et les maisons de retraite, certaines infections sont provoquées par des bactéries robustes qui adhèrent aux sondes, résistent à plusieurs antibiotiques et se propagent silencieusement entre les personnes et les animaux. Cette étude suit l’un de ces coupables, Proteus mirabilis, à l’échelle mondiale, en utilisant son ADN comme carnet de voyage pour révéler comment une seule lignée difficile à traiter est silencieusement devenue dominante au cours du dernier siècle.
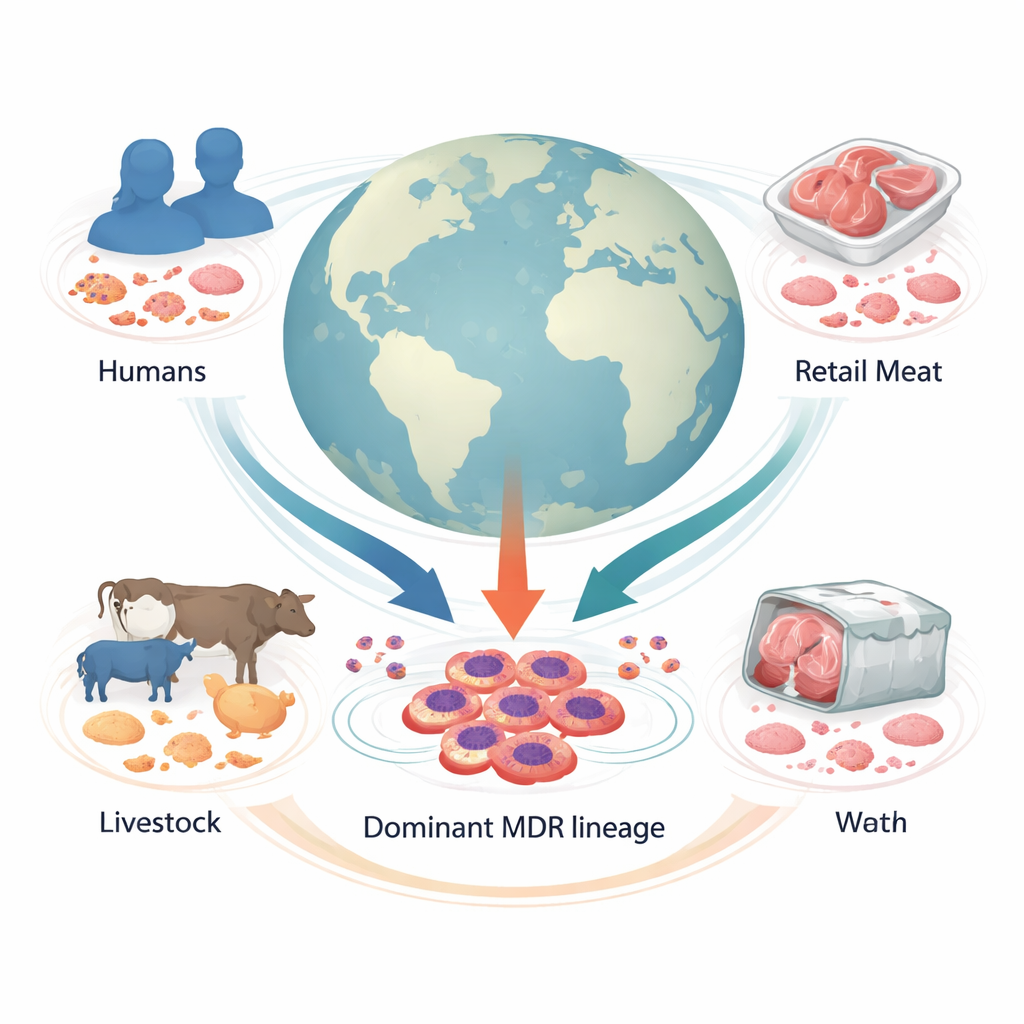
Un aperçu mondial d’une menace cachée
Les chercheurs ont assemblé les génomes de 1 142 échantillons de Proteus mirabilis recueillis dans 34 pays, provenant d’humains, d’animaux d’élevage, de viandes vendues au détail et d’autres environnements. En comparant les génomes complets, ils ont réparti les bactéries en 178 familles génétiques. Une se détachait : le « Cluster-1 », une lignée majeure qui représentait un échantillon sur cinq et comprenait des souches issues d’hôpitaux sur plusieurs continents. La plupart de ces souches provenaient d’humains, mais une part substantielle provenait aussi d’animaux d’élevage et de viande, indiquant que cette lignée circule entre espèces et le long de la chaîne alimentaire.
Une lignée équipée de nombreux remparts antibiotiques
Lorsque l’équipe a recherché les gènes de résistance aux antibiotiques dans les génomes, le Cluster-1 affichait une charge nettement plus élevée. En moyenne, ses membres hébergeaient près de 18 gènes de résistance chacun, bien plus que les autres lignées. Parmi eux figuraient des gènes qui neutralisent certains de nos antibiotiques les plus puissants, comme les carbapénèmes, souvent réservés en dernier recours. De nombreux gènes de résistance se trouvent au sein d’une grande « île » d’ADN appelée PmGRI1, qui peut sauter d’une bactérie à une autre. Certaines versions de cette île portent plus de 20 gènes de résistance simultanément, transformant efficacement Proteus en une pharmacie ambulante de défenses et laissant peu d’options thérapeutiques aux médecins.
Caractères adhésifs qui aident la bactérie à tenir
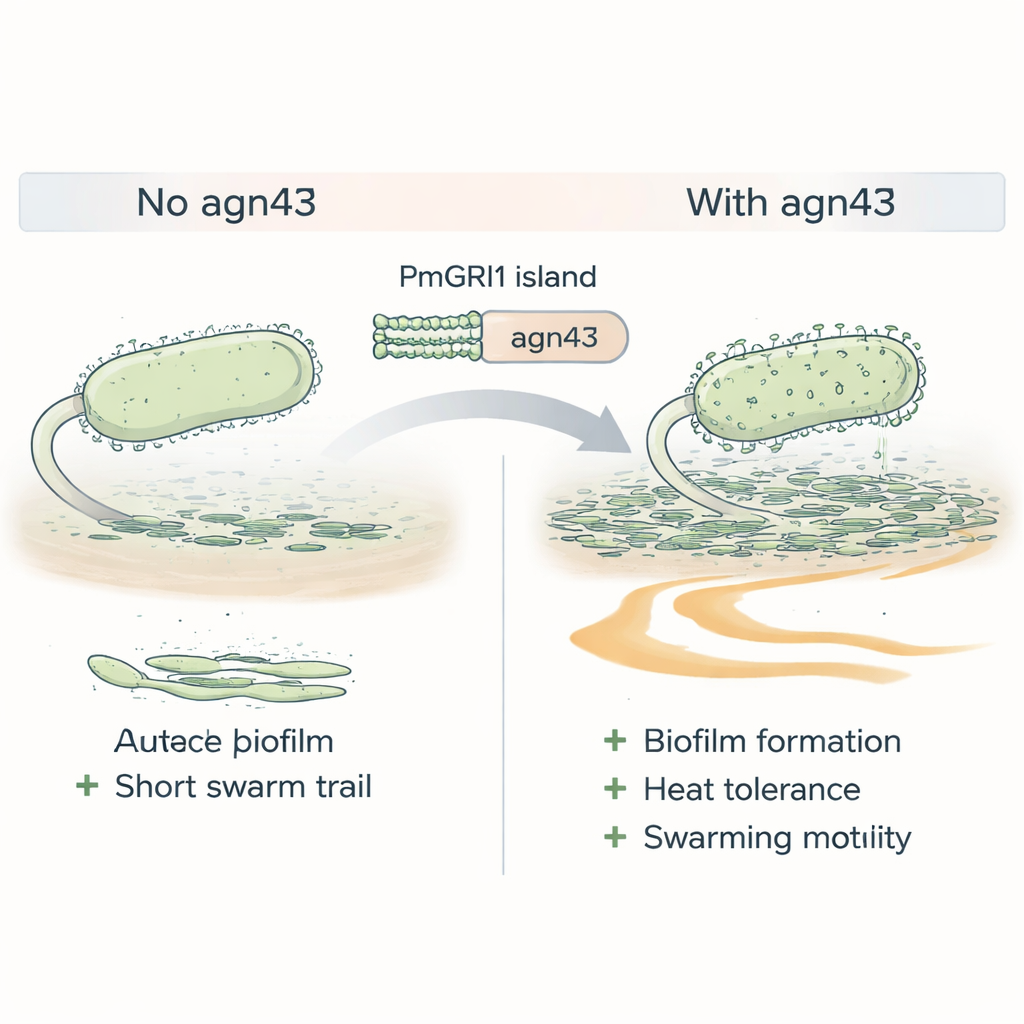
La résistance seule ne garantit pas le succès ; les bactéries doivent aussi survivre dans l’organisme et dans l’environnement hospitalier. Les souches du Cluster-1 étaient enrichies en gènes associés à l’adhérence aux cellules et à la formation de biofilms — des communautés visqueuses qui protègent les bactéries des médicaments et du système immunitaire. Un gène remarquable sur l’île PmGRI1, appelé agn43, code une protéine de surface qui agit comme du Velcro moléculaire, aidant les cellules à s’agglomérer. Lorsque les scientifiques ont supprimé agn43 dans une souche du Cluster-1, le mutant formait des biofilms plus faibles, supportait moins bien le stress thermique et se déplaçait moins efficacement à la surface, autant de caractères qui aident normalement Proteus à coloniser les sondes urinaires et à se propager dans les voies urinaires.
Comment et où cette super-lignée s’est propagée
En combinant les différences génétiques avec les dates d’isolement, les chercheurs ont reconstruit une chronologie pour le Cluster-1. Ils ont estimé que son ancêtre commun le plus récent est apparu vers 1910, des décennies avant l’usage généralisé des antibiotiques modernes. La lignée s’est ensuite scindée en deux branches d’intérêt médical : l’une, principalement observée en Chine, porte un gène détruisant les carbapénèmes appelé blaKPC-2, et l’autre, surtout aux États-Unis, porte un gène apparenté, blaIMP-27. Depuis la fin des années 1980, le Cluster-1 s’est rapidement étendu et a été détecté à plusieurs reprises en déplacement entre pays et entre humains, animaux d’élevage et viande, soulignant son potentiel épidémique.
Ce que cela signifie pour les patients et la santé publique
Pour le grand public, le message est le suivant : une famille particulière de Proteus mirabilis a évolué en un germe hospitalier très performant en combinant deux avantages : une armure épaisse de gènes de résistance aux antibiotiques et une « adhérence » accrue qui favorise la formation de films protecteurs et la persistance sur les sondes et les tissus. Cette combinaison rend les infections plus difficiles à traiter et plus faciles à diffuser. Ce travail met en évidence la nécessité d’une surveillance génétique étroite de cette lignée dans les hôpitaux et l’agriculture, d’un renforcement des mesures de contrôle des infections liées aux sondes, et d’un usage prudent des antibiotiques pour ralentir l’essor et la circulation mondiale de telles souches multirésistantes.
Citation: Zhang, T., Wei, H., Ju, Z. et al. Genomic survey uncovers the emergence of a multidrug-resistant dominant lineage in Proteus mirabilis populations. npj Antimicrob Resist 4, 17 (2026). https://doi.org/10.1038/s44259-026-00189-5
Mots-clés: résistance aux antibiotiques, infection urinaire, infections nosocomiales, génomique bactérienne, biofilm