Clear Sky Science · fr
Expansion mondiale sur cinq décennies de Staphylococcus argenteus ST2250 modèle des dynamiques de résistance aux antimicrobiens
Pourquoi un germe peu connu a de l’importance
La plupart des gens ont entendu parler du « MRSA », le Staphylococcus aureus résistant aux antibiotiques qui hante les hôpitaux et les titres de presse. Bien moins connaissent son proche cousin, Staphylococcus argenteus. Cette étude montre qu’une famille particulière de S. argenteus, appelée ST2250, s’est discrètement répandue dans le monde au cours des 50 dernières années tout en accumulant un ensemble de gènes de résistance aux antibiotiques. Comprendre comment cela s’est produit aide les médecins et les responsables de santé publique à se préparer à la prochaine vague d’infections difficiles à traiter.
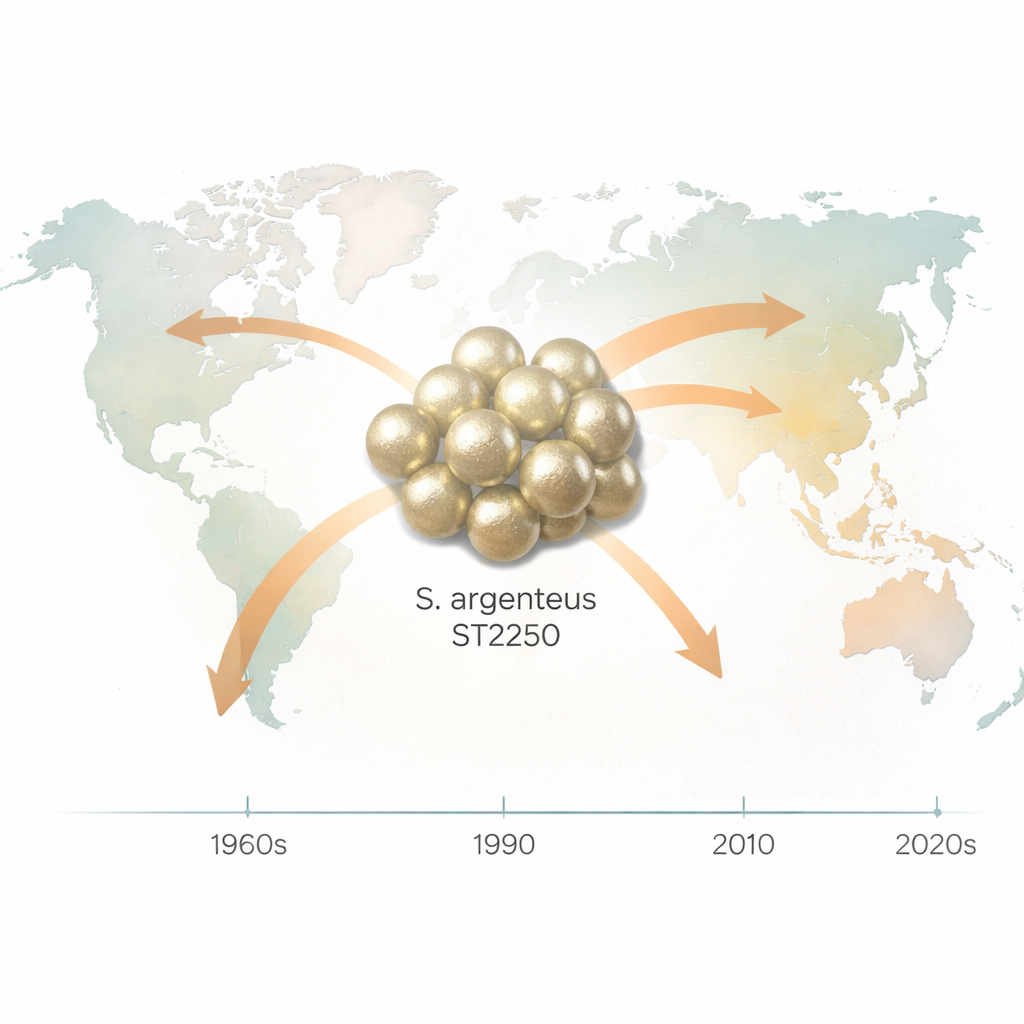
Un nouveau fauteur de trouble dans la famille des staphylocoques
S. argenteus n’a été reconnue comme espèce à part entière qu’en 2015, après des années où elle avait été prise pour S. aureus au laboratoire. Pourtant, elle peut provoquer bon nombre des mêmes problèmes : intoxinations alimentaires, infections cutanées et des tissus mous, infections du sang, maladies des os et des articulations, ainsi que des infections chez les animaux et dans les produits alimentaires. Comme les tests de routine la confondent souvent avec S. aureus, son impact réel a probablement été sous-estimé. Les auteurs ont rassemblé 379 génomes de haute qualité de S. argenteus provenant de 28 pays sur six continents, majoritairement d’humains malades mais aussi d’aliments, d’animaux et de l’environnement, pour dresser un panorama mondial de l’évolution de cette espèce.
Un clone dominant fait le tour du monde
Quand l’équipe a comparé l’ADN de tous ces isolats, elle a constaté que S. argenteus se compose de plusieurs lignées distinctes, chacune correspondant à un « type de séquence » génétique spécifique. L’une d’elles, ST2250, dominait l’ensemble des données, représentant plus de la moitié des génomes. ST2250 a été trouvée sur plusieurs continents et dans de nombreux types d’échantillons, des patients hospitalisés aux aliments. À partir d’un arbre évolutif calibré dans le temps, les chercheurs estiment que l’ancêtre commun des souches ST2250 actuelles est apparu vers 1967. Depuis lors, sa taille de population effective — un indicateur du nombre d’infections et de transmissions réussies — a fortement augmenté pendant des décennies, culminant autour de 2012 avant de montrer des signes de déclin récent.
Chargée d’outils de résistance et de virulence
L’étude a répertorié les gènes qui aident S. argenteus à provoquer des maladies (gènes de virulence) et à résister aux antibiotiques (gènes de résistance aux antimicrobiens, ou RAM). Chaque génome portait des dizaines de gènes de virulence, et les souches ST2250 n’en présentaient que légèrement moins que les autres lignées, suggérant un potentiel de pathogénicité similaire. La différence la plus nette portait sur la résistance. Sur l’ensemble des génomes, les auteurs ont trouvé 29 gènes de RAM distincts couvrant 12 classes d’antibiotiques et de désinfectants. Les souches ST2250 portaient typiquement plus de gènes de résistance que les autres types et présentaient souvent les mêmes combinaisons. De nombreuses souches ST2250 portaient aussi fosB, un gène qui protège contre la fosfomycine, un ancien antibiotique dont l’utilisation a repris face aux infections staphylococciques difficiles. Le proche parent ST1850 portait également fosB, ce qui suggère que ce gène aurait pu être présent chez leur ancêtre commun.
Comment les traits de résistance voyagent ensemble
Les chercheurs ont recherché des gènes de résistance qui ont tendance à apparaître ensemble dans une même souche plus souvent que le hasard ne le voudrait. Ils ont trouvé des associations fortes, comme le gène de résistance aux tétracyclines (tetL) avec la résistance aux aminosides (aph(3')-IIIa), et la résistance au triméthoprime (dfrG) avec la résistance à la méthicilline (mecA). Ces grappes reflètent probablement des événements passés où plusieurs gènes ont été acquis simultanément sur des éléments d’ADN mobiles tels que des plasmides, puis transmis au fil de la propagation des lignées bactériennes. En effet, l’équipe a détecté des dizaines de types de « réplicons » plasmidiques et a montré que certains plasmides co-occurrent fortement avec des gènes de résistance spécifiques. Au sein de ST2250, deux sous-lignées majeures sont apparues : l’une en Asie et l’autre en Europe, chacune marquée par son propre paquet de résistances caractéristique et, en Europe, par la cassette de résistance à la méthicilline connue sous le nom de SCCmec.
Ce que cela signifie pour l’avenir
Pour les non-spécialistes, le message principal est que S. argenteus n’est pas une curiosité inoffensive mais un membre en expansion de la famille des staphylocoques résistants aux médicaments. En l’espace d’environ cinq décennies, une unique lignée réussie, ST2250, s’est répandue largement et a accumulé un mélange riche de gènes de résistance, créant les conditions propices à l’émergence de souches multirésistantes. Bien qu’il existe des indices précoces suggérant un ralentissement de la croissance de ST2250, d’autres lignées dotées de leurs propres traits de résistance attendent en coulisses. Les auteurs soutiennent qu’une détection plus précise de S. argenteus, un échantillonnage plus large au-delà des hôpitaux et une surveillance génétique étroite seront essentiels pour empêcher que ce pathogène discret ne devienne la prochaine grande menace staphylococcique.
Citation: Costa, L.R.M., Marmion, M., Buiatte, A.B.G. et al. Five-decade global expansion of Staphylococcus argenteus ST2250 shapes antimicrobial resistance dynamics. npj Antimicrob Resist 4, 14 (2026). https://doi.org/10.1038/s44259-026-00188-6
Mots-clés: Staphylococcus argenteus, résistance aux antimicrobiens, épidémiologie génomique, clone ST2250, bactéries résistantes aux médicaments