Clear Sky Science · fr
Synergie phage‑méropenem contre des isolats cliniques de Klebsiella pneumoniae producteurs d’OXA‑48
Pourquoi de minuscules virus pourraient sauver des antibiotiques défaillants
Les hôpitaux du monde entier sont confrontés à des infections qui ne répondent plus à nos antibiotiques les plus puissants. L’un des pires coupables est une bactérie nommée Klebsiella pneumoniae, capable de provoquer des pneumonies, des infections sanguines et des infections urinaires. Cette étude examine si des virus soigneusement choisis qui attaquent les bactéries — appelés phages — peuvent s’allier à un antibiotique puissant, le méropenem, pour éliminer des souches fortement résistantes qui menacent aujourd’hui la vie des patients.
Un germe hospitalier discret en progression
Klebsiella pneumoniae est devenu un super‑microbe majeur des hôpitaux parce que de nombreuses souches ont appris à résister aux carbapénèmes, une famille d’antibiotiques réservée en dernier recours. Ces bactéries portent souvent des gènes de résistance sur de petits cercles d’ADN appelés plasmides, qu’elles peuvent s’échanger comme des cartes à collectionner. Un de ces plasmides, connu sous le nom de pOXA‑48, code pour une enzyme qui dégrade les carbapénèmes, rendant des médicaments comme le méropenem largement inefficaces. À mesure que ces plasmides se propagent au sein de clones bactériens à haut risque à travers l’Europe et au‑delà, les traitements standard deviennent moins fiables, rendant même des interventions médicales de routine plus dangereuses.
Recruter des phages comme attaques de précision
Parce que l’arrivée de nouveaux antibiotiques est lente, les chercheurs se tournent vers la thérapie par phages — l’utilisation de virus qui infectent et tuent spécifiquement les bactéries. Dans cette étude, l’équipe s’est concentrée sur un phage lytique appelé vB_Kpn_2‑P4, capable d’infecter un large éventail d’isolats cliniques de Klebsiella collectés dans des hôpitaux espagnols. En tests de laboratoire, ce phage a pu attaquer des bactéries portant plusieurs mécanismes différents de résistance aux carbapénèmes. Cependant, comme cela arrive souvent avec les antibiotiques et les phages, certaines cellules bactériennes ont fini par survivre et repousser, soulignant la nécessité de stratégies combinées plutôt que de s’en remettre à une seule arme.
Quand le médicament et le virus agissent mieux ensemble
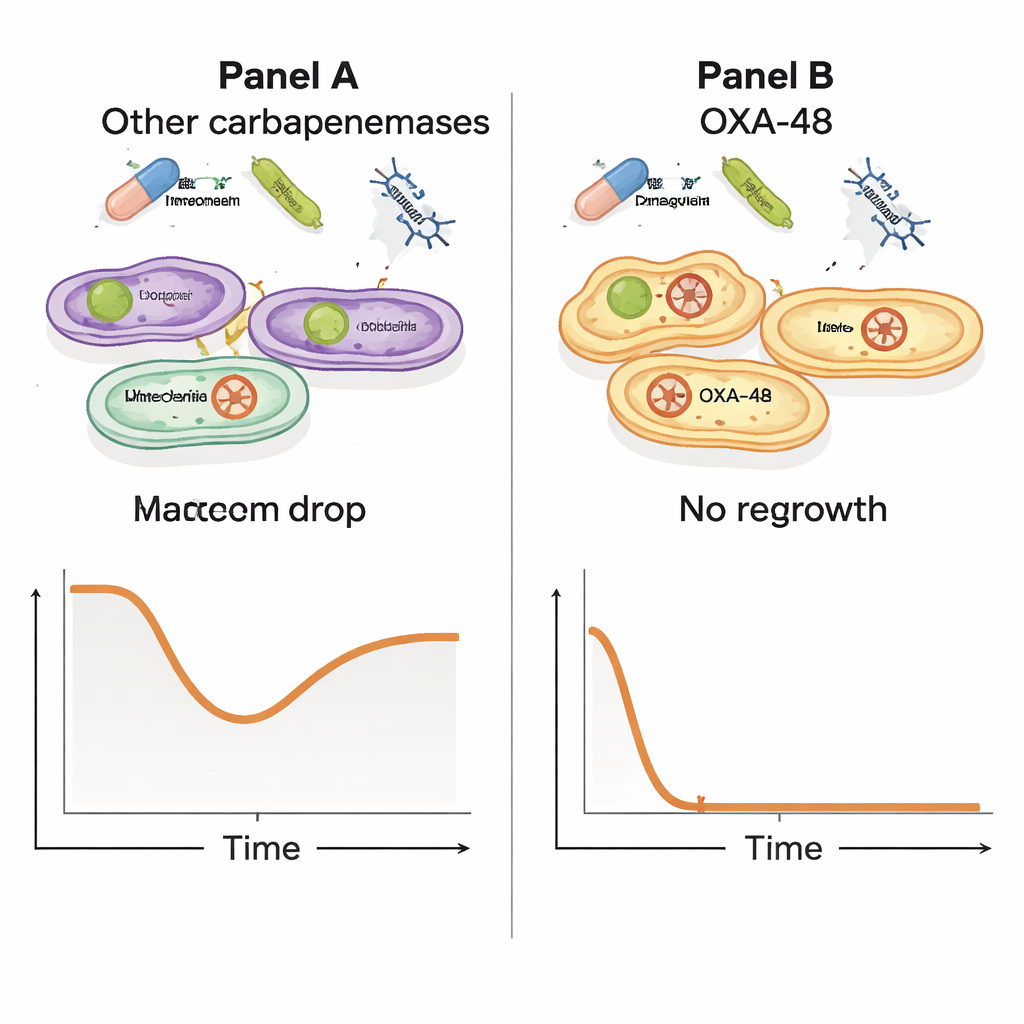
Les chercheurs ont ensuite testé le comportement du méropenem et du phage lorsqu’ils sont utilisés ensemble. Ils ont cultivé douze isolats résistants et les ont exposés au méropenem seul, au phage seul, ou aux deux simultanément, en suivant la croissance pendant de nombreuses heures. Si tous les isolats pouvaient tolérer le méropenem dans les conditions du test, un schéma frappant est apparu : chez les souches portant le plasmide OXA‑48, la combinaison phage plus méropenem à forte dose provoquait un effondrement spectaculaire du nombre de bactéries, suivi d’une absence de reprise détectable. À des niveaux plus faibles de méropenem, ces souches OXA‑48 montraient quand même une forte diminution de la charge bactérienne. En revanche, les souches dotées d’autres enzymes de résistance n’ont pas présenté cet effet synergique puissant, ce qui suggère qu’une caractéristique particulière du plasmide OXA‑48 rend les bactéries particulièrement vulnérables face à ces deux menaces simultanées.
Suivre l’adjuvant génétique caché
Pour comprendre pourquoi seuls les producteurs d’OXA‑48 affichaient cette synergie, l’équipe a comparé les génomes des différents isolats bactériens. Ils ont identifié des dizaines de gènes associés à la réponse synergique, presque tous regroupés sur le plasmide pOXA‑48. Fait important, lorsqu’ils ont isolé des bactéries ayant évolué vers une résistance au phage, ces survivantes portaient encore un gène OXA‑48 intact ; elles n’avaient pas simplement abandonné le plasmide pour échapper au phage. Cela indique une image plus subtile dans laquelle le plasmide qui confère la résistance aux médicaments impose aussi des coûts cachés à la biologie des bactéries — des coûts qui deviennent létaux lorsque le phage et l’antibiotique frappent ensemble, faisant pencher la balance contre le pathogène.
Ce que cela pourrait signifier pour les traitements futurs
Pour les non‑spécialistes, le message clé est que les astuces génétiques mêmes que les bactéries utilisent pour esquiver nos médicaments peuvent parfois se retourner contre elles. Dans ce cas, un plasmide de résistance spécifique semble rendre certaines souches de Klebsiella extrêmement sensibles à une attaque combinée par un phage adapté et le méropenem. Bien que ce travail ait été réalisé en conditions de laboratoire et que des recherches supplémentaires soient nécessaires chez l’animal et chez l’humain, il suggère que l’appariement du phage approprié au profil de résistance adéquat pourrait ranimer des antibiotiques qui paraissaient avoir perdu leur efficacité. Plutôt que de remplacer les antibiotiques, les phages pourraient devenir des alliés intelligents qui nous aident à déjouer des super‑microbes autrefois invincibles.
Citation: Cantallops, I., Ferriol-González, C., Barcos-Rodríguez, T. et al. Phage-meropenem synergy against OXA-48-producing Klebsiella pneumoniae clinical isolates. npj Antimicrob Resist 4, 12 (2026). https://doi.org/10.1038/s44259-026-00186-8
Mots-clés: thérapie par phages, résistance aux antibiotiques, Klebsiella pneumoniae, plasmide OXA‑48, synergie méropenem