Clear Sky Science · fr
Réponse globale à l’exposition aux antibiotiques révèle un rôle critique du métabolisme des nucléotides dans la tolérance élevée aux β‑lactamines
Pourquoi certaines bactéries résistent à nos meilleurs antibiotiques
Les antibiotiques sont censés éliminer les bactéries nuisibles, et pourtant de nombreuses infections persistent obstinément ou réapparaissent après le traitement. Cet article explore une raison insuffisamment prise en compte : certaines bactéries peuvent se mettre à l’abri et survivre temporairement même à des doses très élevées de médicaments puissants comme la pénicilline. En révélant comment ces microbes réorganisent leur chimie interne pour tenir le coup, les chercheurs indiquent de nouvelles pistes pour restaurer l’efficacité des antibiotiques existants.
Une ruse de survie furtive au sein des infections
Lorsqu’elles sont exposées à des antibiotiques β‑lactamines tels que la pénicilline, de nombreuses bactéries Gram‑négatives dangereuses ne meurent pas simplement. Elles peuvent au contraire perdre leur paroi rigide et se transformer en corps fragiles et arrondis appelés sphéroplastes. Ainsi transformées, elles cessent de se multiplier mais restent bien vivantes et métaboliquement actives. Une fois le médicament éliminé, elles reconstruisent leur paroi, retrouvent leur forme normale en bâtonnet et peuvent relancer l’infection. Parce que cette « tolérance » constitue une étape vers une résistance complète aux antibiotiques et l’échec du traitement, comprendre comment survivent les sphéroplastes est crucial pour la médecine future.
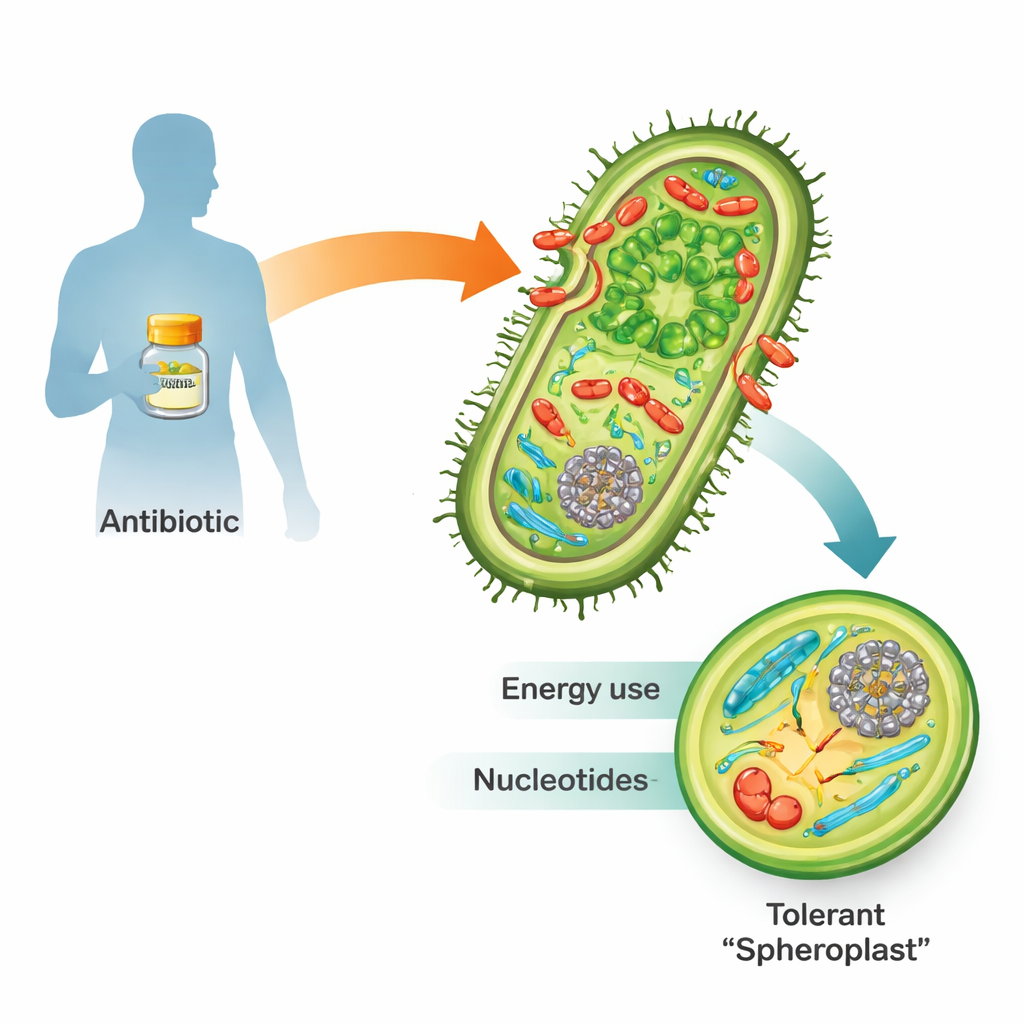
À l’écoute de l’alerte d’urgence cellulaire
L’équipe a utilisé Vibrio cholerae, la bactérie responsable du choléra, comme modèle parce qu’elle tolère exceptionnellement bien les β‑lactamines et se prête facilement à la manipulation génétique. Les chercheurs ont exposé les bactéries à dix fois la dose minimale létale de pénicilline et suivi la réponse au cours du temps avec deux outils puissants. La transcriptomique a suivi quels gènes étaient activés ou réprimés, tandis que la métabolomique a mesuré des centaines de petites molécules qui alimentent et construisent la cellule. Ensemble, ces techniques « multi‑omiques » ont produit une cartographie temporelle de la manière dont une cellule tolérante reconfigure son fonctionnement interne pendant l’assaut médicamenteux.
Redirections métaboliques et une faiblesse cachée
Les données ont révélé des changements profonds dans les voies centrales. Les gènes de synthèse de la paroi cellulaire se sont fortement activés, cohérents avec la tentative de la cellule de réparer les dégâts et de se préparer à la récupération. Les systèmes de réponse au choc thermique et au stress se sont également déclenchés, traitant probablement les protéines mal repliées ou oxydées créées par le stress induit par l’antibiotique. Parallèlement, le métabolisme carboné central a basculé : certaines étapes du cycle de l’acide citrique (TCA), le principal générateur d’énergie de la cellule, ont été stimulées, tandis que des intermédiaires clés de la glycolyse tels que le glucose‑6‑phosphate et le fructose‑6‑phosphate ont été fortement épuisés. Ces intermédiaires alimentent normalement à la fois la production d’énergie et la construction de la paroi, ce qui suggère qu’un « cycle futile » continu et gaspilleur du matériel de paroi épuisait les ressources.
Pression sur les nucléotides
Le changement le plus saisissant concernait les nucléotides, les briques de l’ADN, de l’ARN et de nombreuses molécules porteuses d’énergie. Les niveaux de nombreux nucléotides et de leurs précurseurs se sont effondrés dans les cellules traitées à la pénicilline, alors même que les gènes de leur synthèse de novo étaient fortement activés. Parallèlement, les gènes impliqués dans le « recyclage » des nucléotides étaient réprimés, comme si la cellule tentait de conserver ce qui restait. Ces schémas suggéraient que les sphéroplastes subissaient un stress sévère en nucléotides. Lorsque les chercheurs ont délibérément perturbé les voies fournissant des précurseurs de nucléotides — par exemple la voie des pentoses phosphates — ou bloqué la production de nucléotides avec un autre médicament, le triméthoprime, la combinaison avec les β‑lactamines a tué bien plus de bactéries que chaque médicament utilisé séparément. Cette forte synergie a été observée non seulement chez Vibrio cholerae mais aussi chez des souches cliniques hautement tolérantes de Klebsiella pneumoniae et d’Escherichia coli.
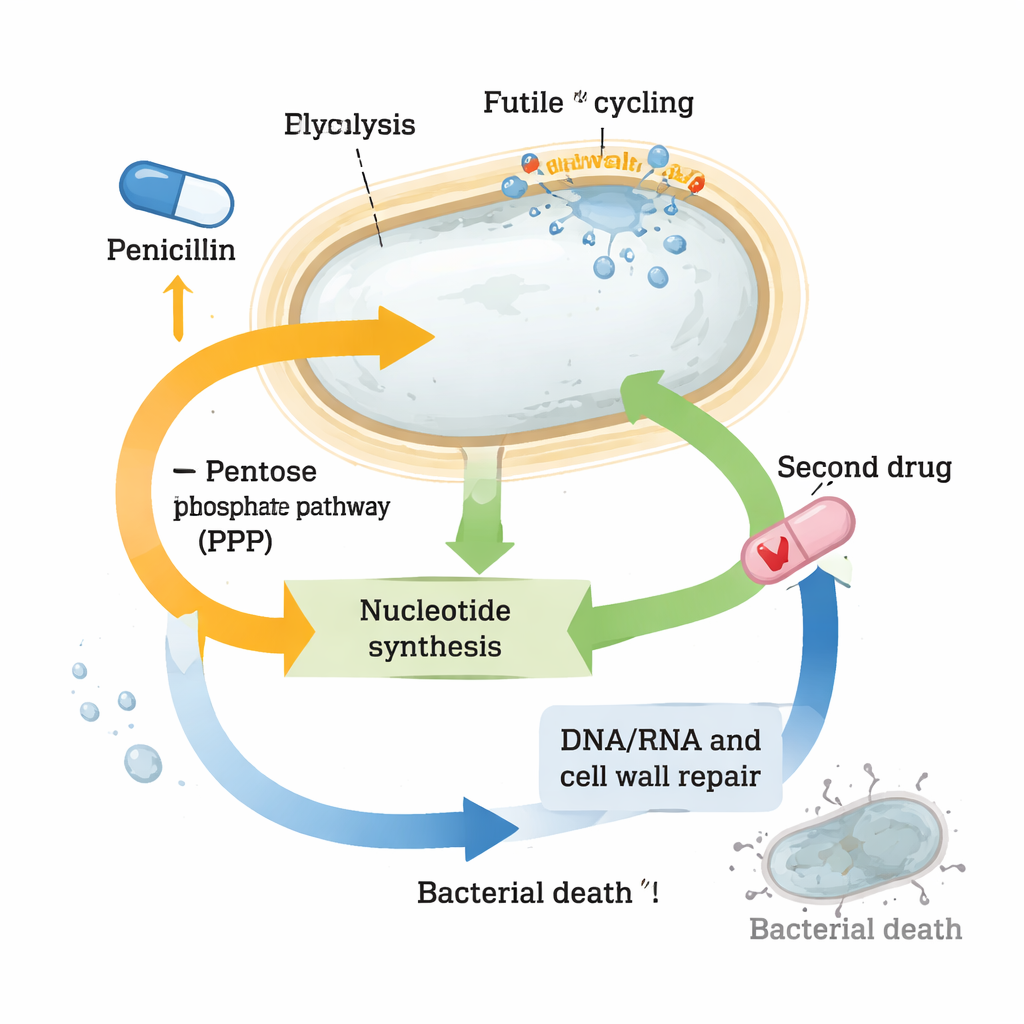
Transformer la chimie de survie en avantage thérapeutique
Malgré une importante réorganisation de leur métabolisme, les sphéroplastes tolérants parviennent à maintenir relativement stable leur monnaie énergétique, l’ATP, et à éviter des dégâts catastrophiques, ce qui les aide à survivre à de longues expositions aux antibiotiques. Mais l’étude montre qu’en procédant ainsi, ils poussent leurs réservoirs de nucléotides au bord du précipice. Cet équilibre précaire crée une vulnérabilité : perturber légèrement le métabolisme des nucléotides avec un second médicament fait s’effondrer leurs défenses et restaure une activité bactéricide puissante. Pour les lecteurs non spécialistes, la conclusion est que certaines bactéries survivent aux antibiotiques non pas parce que les médicaments ne ciblent pas leurs cibles, mais parce que les cellules réorientent rapidement leur chimie pour encaisser le coup. En trouvant et en exploitant les maillons faibles de cette réorganisation de survie — ici, le métabolisme des nucléotides — les chercheurs pourraient transformer d’anciens antibiotiques en thérapies combinées puissantes capables de déjouer des agents pathogènes très tolérants.
Citation: Keller, M.R., Kazi, M.I., Saleh, A. et al. Global response to antibiotic exposure reveals a critical role for nucleotide metabolism in high-level β-lactam tolerance. npj Antimicrob Resist 4, 11 (2026). https://doi.org/10.1038/s44259-026-00183-x
Mots-clés: tolérance aux antibiotiques, antibiotiques β‑lactamines, métabolisme des nucléotides, persistance bactérienne, combinaisons médicamenteuses