Clear Sky Science · fr
Diriger le transfert de charge dans des composites CuInS2/BiOCl pour permettre la rupture de liaisons C–F de PFAS dans l’eau sous l’action du soleil
Pourquoi il est important de briser les « produits chimiques éternels »
Pendant des décennies, une famille de composés synthétiques connus sous le nom de « produits chimiques éternels » s’est infiltrée dans l’eau potable, les emballages alimentaires, les mousses anti‑incendie et nos organismes. Ces substances, appelées techniquement PFAS, sont recherchées pour leur résistance à la chaleur et aux taches — mais cette même robustesse les rend extrêmement difficiles à éliminer de l’environnement. Cet article présente une technologie activée par la lumière du soleil capable de rompre effectivement les liaisons les plus fortes d’un substitut clé des PFAS en solution aqueuse, ouvrant la voie à des moyens pratiques de dépolluer rivières, eau du robinet et effluents industriels.
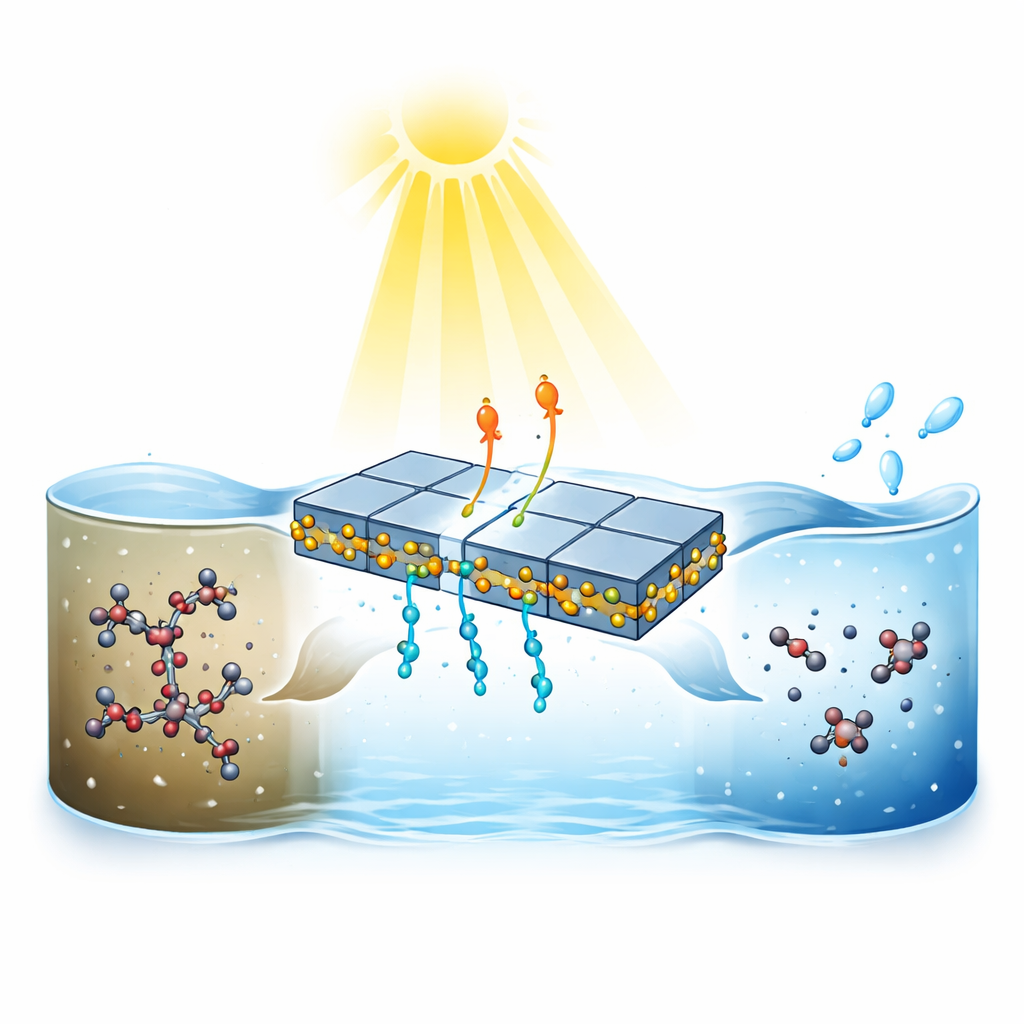
Une nouvelle manière d’exploiter la lumière solaire
Les chercheurs se sont concentrés sur le p‑perfluoré nonénoxybenzènesulfonate de sodium (OBS), un remplacement des anciens PFAS qui apparaît désormais dans les eaux de surface et suscite des inquiétudes pour la santé. Les traitements conventionnels peinent avec les PFAS car leurs liaisons carbone–fluor sont parmi les plus fortes de la chimie, nécessitant souvent des températures, des pressions ou des réactifs agressifs pour être rompues. Inspiré par la façon dont les plantes séparent les charges électriques pendant la photosynthèse, l’équipe a conçu un matériau en couches activé par la lumière capable d’utiliser la lumière solaire ordinaire pour attaquer l’OBS en milieu aqueux dans des conditions douces.
Conception d’un catalyseur en deux parties
Le cœur du système est un partenariat soigneusement conçu entre deux semi‑conducteurs : des cristaux minces en forme de plaquettes d’oxychlorure de bismuth (BiOCl) et de minuscules points quantiques de sulfure de cuivre‑indium (CuInS2). Une fois combinés, ces matériaux forment ce qu’on appelle une hétérojonction en Z, une structure qui canalise les charges négatives (électrons) générées par la lumière vers les particules de CuInS2 et les charges positives (trous) vers les plaques de BiOCl. La microscopie et des mesures avancées en rayons X montrent que les points quantiques adhèrent fermement aux bords des plaques via des liaisons soufre–bismuth, créant un contact intime qui accélère le flux de charge et empêche les électrons et les trous de se recombiner et de gaspiller la lumière absorbée.
Rompre les liaisons les plus solides
Lorsque la lumière atteint le composite, les charges séparées deviennent de puissants agents chimiques. Des calculs et la spectroscopie révèlent que les électrons concentrés sur les points quantiques de CuInS2 sont fortement réducteurs : ils se dirigent vers la branche riche en fluor de la molécule d’OBS, affaiblissent puis rompent les liaisons carbone–fluor de sorte que des ions fluorure sont libérés. Simultanément, les trous positifs sur les plaques de BiOCl attaquent le groupement sulfonaté et l’anneau benzénique attaché, morcelant le squelette carboné. Ces deux processus conjoints raccourcissent la chaîne carbonée et arrachent les atomes de fluor bien plus efficacement que chacun des matériaux utilisés séparément. Sous lumière ultraviolette, le composite optimisé élimine environ trois quarts du fluor total et de la matière organique totale provenant de l’OBS en seulement huit heures — parmi les performances les plus élevées rapportées à ce jour.
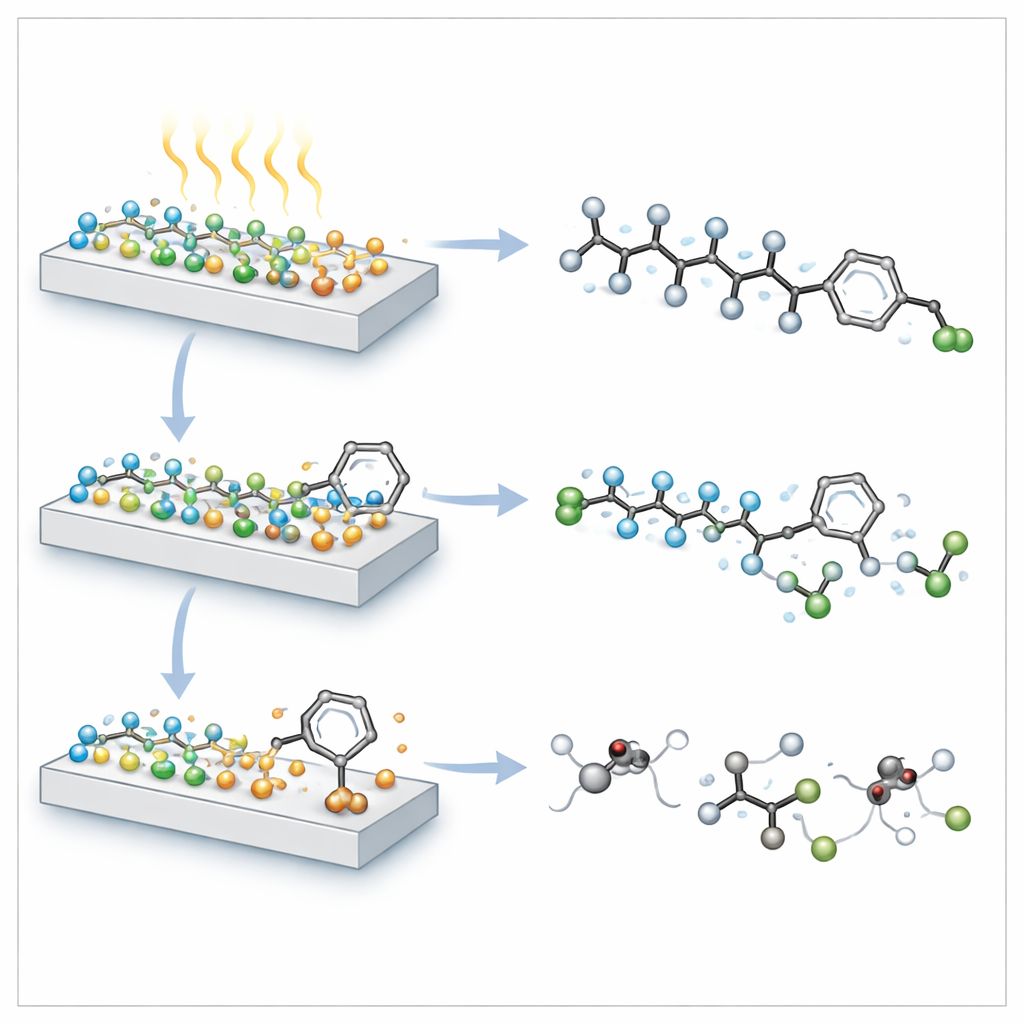
Du laboratoire à l’eau qui coule
Pour vérifier si cette approche pouvait fonctionner en dehors du laboratoire, l’équipe a enrobé des feuilles de polyester flexibles avec le catalyseur et construit un simple réacteur en panneau dans lequel l’eau contaminée pouvait s’écouler tout en étant exposée à la lumière solaire naturelle. Lors d’essais en extérieur, le système a éliminé plus de 96 % de l’OBS de l’eau en dix heures, avec une perte de catalyseur presque négligeable. Le composite a également dégradé des mélanges de 17 PFAS différents, incluant des versions à chaîne longue et courte, et l’a fait dans de l’eau de rivière réelle contenant des minéraux et de la matière organique naturelle. Des tests de toxicité sur de petits vers et des embryons de poissons zèbre ont montré que l’eau traitée présentait des effets biologiques nettement réduits par rapport aux solutions non traitées.
Ce que cela signifie pour une eau plus propre
En termes simples, cette étude démontre un filtre alimenté par le soleil qui fait plus que piéger les PFAS : il contribue à les détruire. En dirigeant les charges générées par la lumière vers les zones appropriées à l’intérieur d’un matériau en deux parties, les chercheurs ont pu rompre certaines des liaisons les plus fortes de la chimie moderne et démanteler des molécules PFAS complexes en fragments beaucoup moins nocifs. Bien que des travaux supplémentaires soient nécessaires avant un déploiement à grande échelle, les résultats suggèrent une voie réaliste vers des systèmes de traitement en flux continu et économe en énergie capables de s’attaquer aux « produits chimiques éternels » dans l’eau potable et les cours d’eau pollués.
Citation: Liu, F., Li, H., Gao, Z. et al. Steering charge transfer in CuInS2/BiOCl composites to enable sunlight-driven C–F bond cleavage of PFAS in water. Nat Water 4, 334–347 (2026). https://doi.org/10.1038/s44221-026-00590-4
Mots-clés: PFAS, traitement de l’eau, photocatalyse, remédiation solaire, chimie environnementale