Clear Sky Science · fr
Atténuation de l’activation épicardique et de l’abondance de myofibroblastes via l’axe Fbln2–Nupr1b stimule la régénération cardiaque chez le poisson zèbre
Pourquoi certains cœurs peuvent se réparer seuls
Lorsqu’une personne fait une crise cardiaque, le muscle endommagé est généralement comblé par une cicatrice rigide qui ne guérit jamais vraiment. Le poisson zèbre, petit poisson rayé d’aquarium, réalise quelque chose de remarquable : il régénère son tissu cardiaque et élimine progressivement la majeure partie de la cicatrice. Cette étude pose une question apparemment simple mais aux grandes implications médicales : comment un cœur en cours de réparation sait‑il quand construire une cicatrice et quand l’éliminer pour permettre la croissance de nouveau muscle ? En décodant cet équilibre chez le poisson zèbre, le travail ouvre la voie à des stratégies qui pourraient un jour aider les cœurs humains blessés à se réparer plutôt qu’à défaillir.
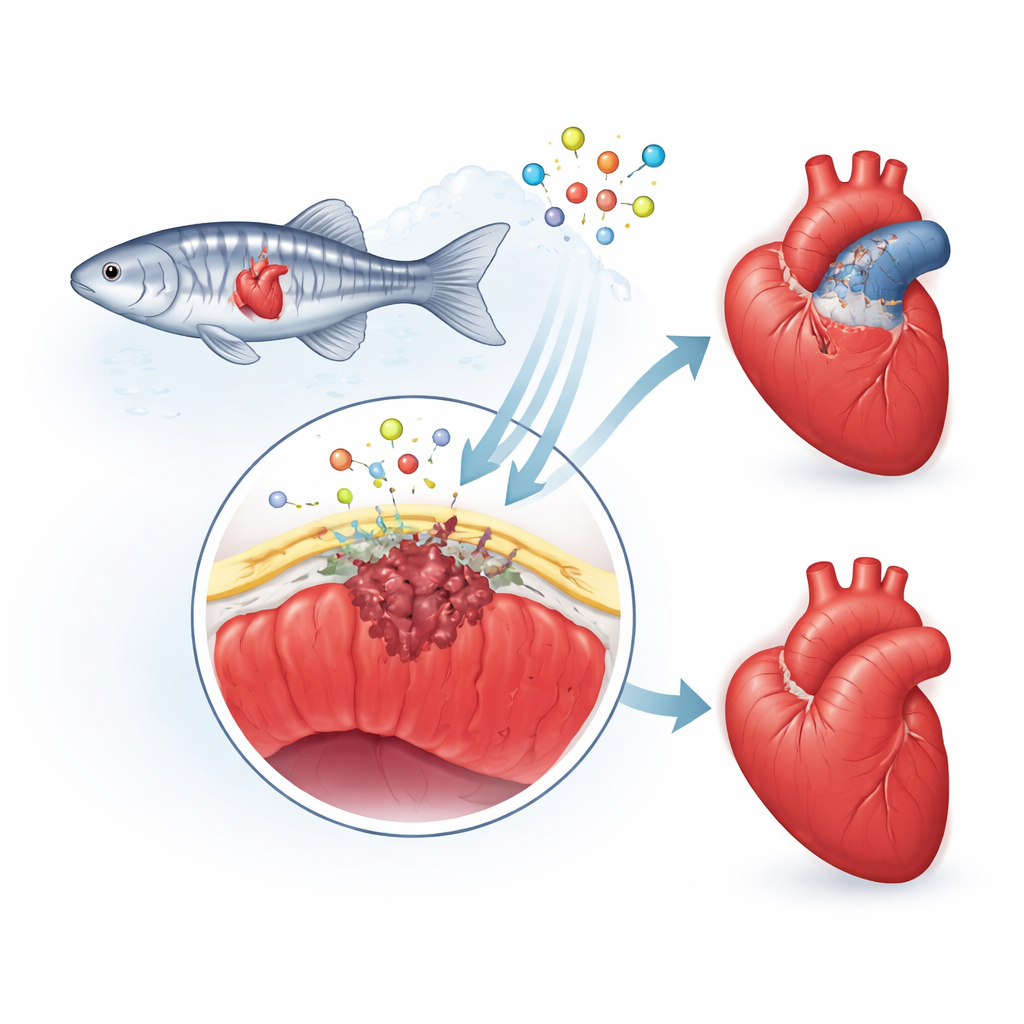
La peau protectrice du cœur
Les chercheurs se concentrent sur l’épicarde, une fine « peau » qui recouvre le cœur. Après une blessure, cette couche s’active : ses cellules changent d’identité et certaines pénètrent dans la zone endommagée. Là, elles deviennent des cellules de soutien et des cellules productrices de cicatrice, et elles libèrent des signaux chimiques qui guident la formation de nouveaux vaisseaux sanguins et de muscle cardiaque. Chez l’humain, cette réponse de réparation a tendance à déborder, laissant une cicatrice épaisse et permanente. Chez le poisson zèbre, en revanche, la cicatrice est temporaire et est progressivement démontée au fur et à mesure du retour d’un tissu sain. L’équipe a émis l’hypothèse qu’une protéine appelée fibuline‑2 (Fbln2), présente dans l’échafaudage entourant le cœur, contribue à régler la vitesse et l’intensité de cette réponse épicardique.
Un variateur moléculaire de la cicatrisation
En utilisant l’édition génétique chez le poisson zèbre, les scientifiques ont créé deux types de poissons présentant des niveaux différents de Fbln2 : une lignée avec Fbln2 réduit et une autre sans la protéine. Ils ont endommagé les cœurs des poissons avec une sonde de congélation, imitant une crise cardiaque, et ont suivi la guérison sur plusieurs semaines à mois. Lorsque les niveaux de Fbln2 étaient abaissés, la division cellulaire précoce du muscle cardiaque et de l’endothélium vasculaire diminuait, mais la cicatrice fibreuse formée était plus petite et plus facilement remodelée. Au bout de trois mois, ces cœurs s’étaient bien régénérés et contenaient peu de collagène, principal composant de la cicatrice. En revanche, les poissons totalement dépourvus de Fbln2 montraient une inhibition plus marquée d’une voie clé de croissance et de cicatrisation impliquant la famille de signaux TGFβ, et présentaient beaucoup moins de cellules formatrices de cicatrice juste sous l’épicarde. Leurs cicatrices initiales étaient également plus petites — mais plus tard, ces cœurs n’ont pas réussi à éliminer le collagène et ont fini par conserver des cicatrices volumineuses et durables avec une régénération déficiente.
Approche détaillée des changements d’état épicardiques
Pour observer le comportement des cellules épicardiques à résolution unicellulaire, l’équipe a utilisé le séquençage ARN unicellulaire peu après la blessure. Ils ont identifié plusieurs « états » cellulaires épicardiques, incluant des cellules silencieuses, des cellules nouvellement activées, des cellules stressées s’adaptant au faible apport en oxygène et des cellules en division active. Chez les poissons avec des niveaux normaux de Fbln2, les cellules épicardiques progressaient de manière fluide d’un état silencieux à activé puis mûr. Chez les poissons avec Fbln2 réduit ou absent, cette progression était bloquée : les cellules stagnaient aux stades précoces et les groupes activés plus matures étaient sous‑représentés, surtout chez les animaux sans Fbln2. De nombreux gènes qui s’expriment normalement lors de l’activation épicardique et en réponse à la signalisation TGFβ étaient affaiblis, ce qui désigne Fbln2 comme un régulateur de cette voie qui détermine à quel degré l’épicarde s’engage dans la formation et le remodelage de la cicatrice.
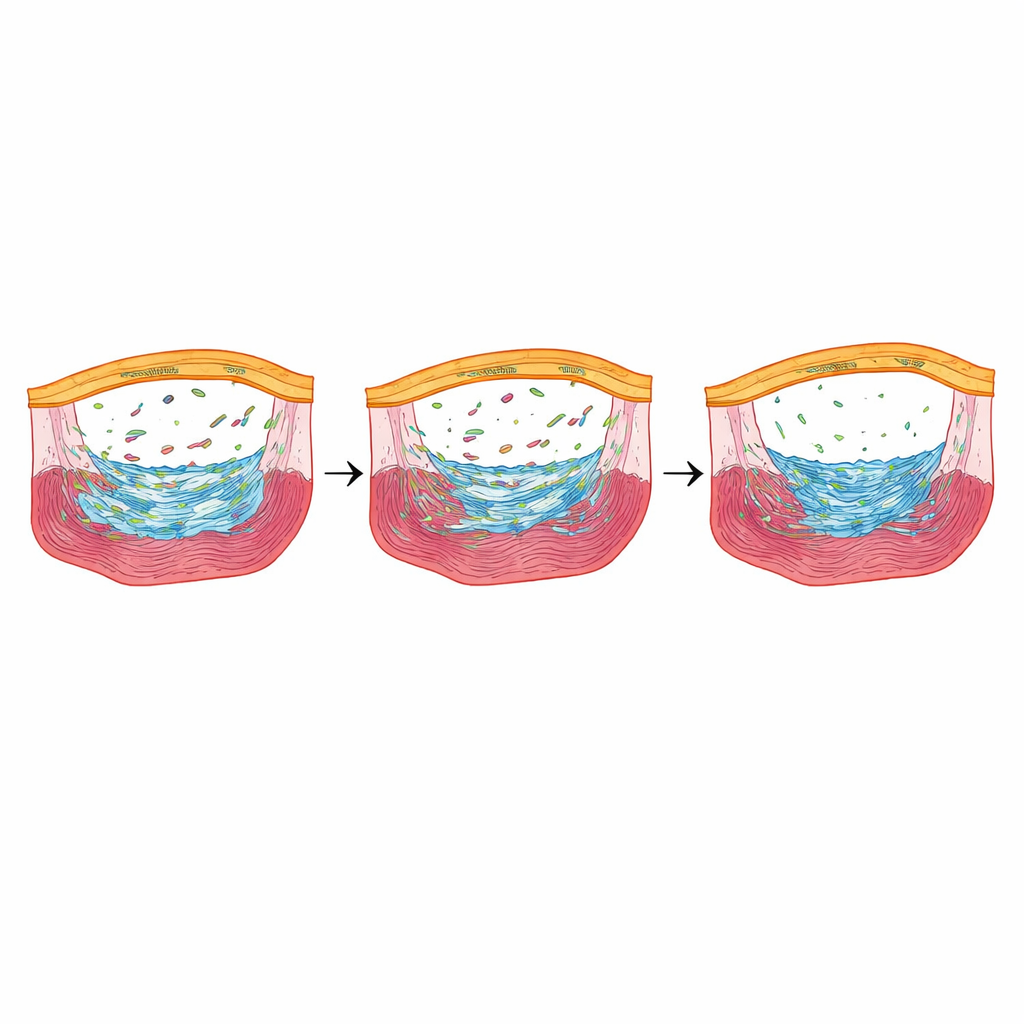
Un répondeur au stress qui ajuste finement la réparation
Parmi les gènes les plus fortement réduits lorsque Fbln2 était abaissé, un se distinguait : nupr1b, un régulateur sensible au stress actif dans les cellules épicardiques au début de la réparation. Lorsque les chercheurs ont supprimé nupr1b, les poissons zèbres présentaient moins de cellules épicardiques formatrices de cicatrice et une division réduite des cellules du muscle cardiaque, et ils conservaient d’importants dépôts de collagène des mois après la blessure — très similaire aux poissons totalement dépourvus de Fbln2. Fait remarquable, lorsque les auteurs ont brièvement réactivé nupr1b uniquement dans les cellules épicardiques des poissons avec Fbln2 réduit, le nombre de cellules formatrices de cicatrice et la prolifération des cellules musculaires cardiaques sont revenus, et la cicatrisation tardive a augmenté. Le blocage chimique des récepteurs TGFβ a réduit les niveaux de nupr1b, positionnant nupr1b en aval d’un axe de signalisation Fbln2–TGFβ.
Ce que cela signifie pour la guérison du cœur humain
Ensemble, ces résultats révèlent un « axe épicardique Fbln2–Nupr1b » qui aide les cœurs de poisson zèbre à tenir un équilibre délicat entre trop peu et trop de fibrose. Atténuer légèrement cet axe tempère le pic précoce de cicatrisation et favorise l’élimination efficace de la cicatrice, tandis que l’éteindre complètement compromet la régénération et laisse une cicatrice rigide. Pour la médecine humaine, la leçon est que l’objectif n’est pas de bloquer la cicatrisation à tout prix, mais de l’ajuster — conserver suffisamment de structure pour prévenir la rupture tout en garantissant que le tissu cicatriciel reste temporaire et peut être remplacé par du muscle sain. Comprendre et, éventuellement, exploiter ce système de contrôle du poisson zèbre pourrait éclairer de futures thérapies visant à encourager le cœur humain blessé vers une régénération réelle plutôt que vers une cicatrisation chronique.
Citation: Kayman Kürekçi, G., Kaur Bajwa, G., Zhang, S. et al. Attenuation of epicardial activation and myofibroblast abundance via the Fbln2–Nupr1b axis stimulates cardiac regeneration in zebrafish. Nat Cardiovasc Res 5, 218–233 (2026). https://doi.org/10.1038/s44161-026-00785-8
Mots-clés: régénération cardiaque, fibrose, poisson zèbre, épicarde, signalisation TGF-bêta