Clear Sky Science · fr
Blocage sélectif de l’activation latente de la TGF-β1 supprime la fibrose tissulaire avec une bonne sécurité
Pourquoi la cicatrisation cachée importe
De nombreuses maladies chroniques endommagent silencieusement nos organes en déposant du tissu cicatriciel rigide, un processus appelé fibrose. Cette cicatrisation peut progressivement étouffer la fonction normale du foie, des reins, des poumons et même autour des tumeurs, où elle peut aussi atténuer les effets des immunothérapies modernes contre le cancer. La protéine TGF-β1 se trouve au cœur de ce processus de cicatrisation, mais l’inactiver partout dans le corps s’est avéré dangereux. Cette étude décrit un nouvel anticorps, appelé SOF10, conçu pour bloquer uniquement l’activation nocive de la TGF-β1 tout en préservant ses rôles essentiels, montrant des bénéfices prometteurs dans des modèles animaux de maladies hépatiques, d’insuffisance rénale et de cancer.
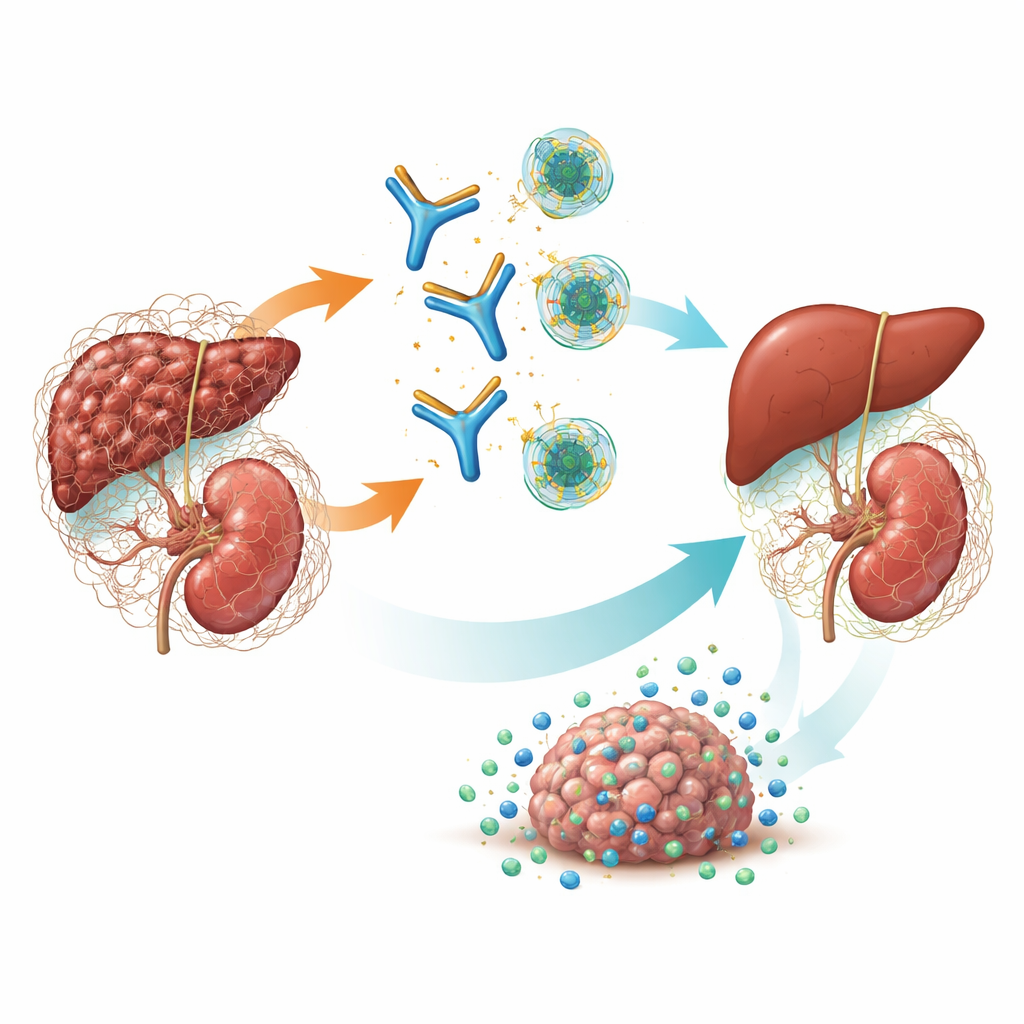
Un commutateur maître pour la cicatrisation et le cancer
La TGF-β est une puissante molécule de signalisation qui aide à contrôler la croissance cellulaire, la réparation et les interactions avec le système immunitaire. Dans les maladies chroniques, une forme—la TGF-β1—pousse les fibroblastes à produire un excès de tissu conjonctif, entraînant le raidissement et la défaillance des organes. Elle façonne aussi une coque fibreuse et immunosuppressive autour des tumeurs qui empêche les cellules immunitaires et les médicaments d’atteindre les cellules cancéreuses. Des médicaments antérieurs ont tenté d’inhiber simultanément les trois formes de la TGF-β, mais ce « blocage pan‑TGF-β » a provoqué des effets secondaires graves tels que des lésions des valvules cardiaques, des hémorragies et des tumeurs cutanées. Des études génétiques et des modèles antérieurs ont suggéré que la TGF-β1 est le principal responsable de la fibrose rénale et de nombreux tumeurs solides, ouvrant la possibilité qu’un ciblage soigneux de cette isoforme soit à la fois efficace et plus sûr.
Verrouiller la TGF-β1 dans sa forme inactive
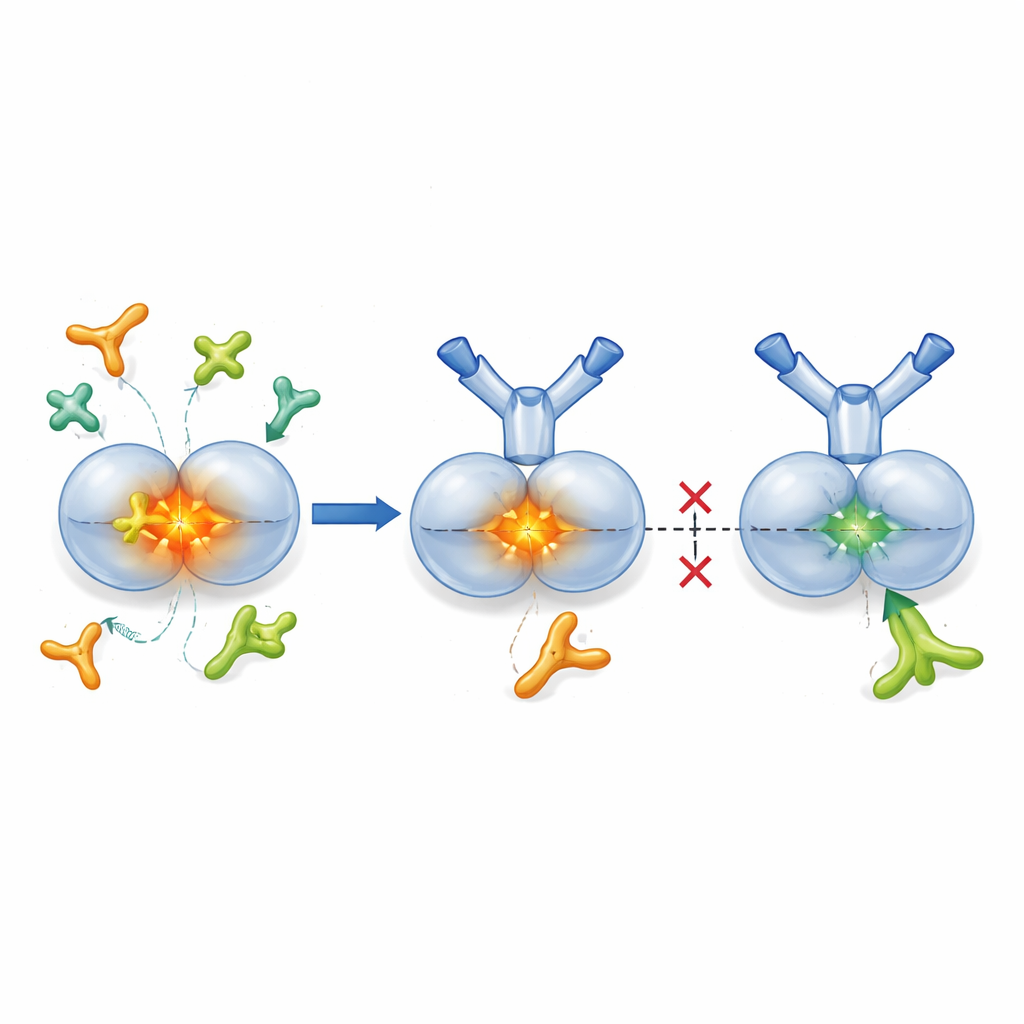
La TGF-β1 est généralement produite dans un « paquet latent », où le cœur actif est enveloppé par une protéine partenaire qui le maintient inactif jusqu’au moment opportun. Des enzymes appelées protéases et certaines protéines d’adhésion à la surface cellulaire connues sous le nom d’intégrines peuvent ouvrir ce paquet, libérant la TGF-β1 active dans le tissu environnant. Les chercheurs ont conçu SOF10, un anticorps humanisé qui se lie uniquement à la forme latente de la TGF-β1, et non à l’hormone active ni aux autres isoformes. Des études structurales par cristallographie aux rayons X ont montré que SOF10 se glisse à l’interface entre deux moitiés du complexe latent, le stabilisant comme une pince. Dans des tests en laboratoire, cela a empêché les protéases et une intégrine (αvβ8) de libérer la TGF-β1 active, tout en laissant une autre intégrine (αvβ6)—importante pour le maintien de l’équilibre immunitaire dans les tissus sains—largement intacte. En pratique, SOF10 silencie sélectivement les voies d’activation dommageables tout en épargnant une voie homéostatique clé.
Protéger le foie et les reins des dommages lents
Pour vérifier si ce verrou sélectif sur la TGF-β1 pouvait réellement limiter la fibrose, l’équipe a testé SOF10 dans plusieurs modèles murins. Dans un modèle rapide de stéatose hépatique induite par l’alimentation évoluant vers une fibrose du foie, le traitement par SOF10 a réduit l’expression hépatique des gènes répondant à la TGF-β et des gènes de synthèse du collagène, et a diminué l’hydroxyproline, un marqueur chimique du tissu cicatriciel accumulé. Dans deux modèles rénaux différents—un modèle d’obstruction chirurgicale qui induit une fibrose interstitielle et un modèle génétique du syndrome d’Alport qui développe à la fois une cicatrisation glomérulaire et une insuffisance rénale—SOF10 a réduit l’activité des gènes fibrosants, diminué la teneur en collagène et réduit visiblement les zones cicatricielles au microscope. Dans le modèle chronique d’Alport, des analyses sanguines ont montré une amélioration de la fonction rénale, et ces bénéfices étaient comparables à ceux d’un anticorps bloquant plus largement la TGF-β, mais sans inhiber les autres isoformes de TGF-β.
Libérer le système immunitaire à l’intérieur des tumeurs
Parce que le tissu fibreux autour des tumeurs peut agir à la fois comme une barrière physique et comme un frein immunitaire, les chercheurs ont évalué si SOF10 pouvait améliorer les réponses aux inhibiteurs de points de contrôle. Dans des modèles murins de cancer du sein et du côlon qui répondent mal à l’anti–PD-L1, l’ajout de SOF10 a significativement ralenti la croissance tumorale, alors que SOF10 ou l’anti–PD-L1 seuls avaient peu d’effet. Les tumeurs des animaux traités en combinaison contenaient plus de cellules T CD8 tueuses et davantage des enzymes toxiques qu’elles utilisent pour détruire les cellules cancéreuses. Les fibroblastes prélevés dans ces tumeurs présentaient une activité réduite des voies de synthèse du collagène et de la matrice mais une activité accrue des voies de l’interféron et de présentation d’antigène, une bascule vers un stroma plus favorable à l’immunité. Ces changements reflétaient étroitement ce qui avait été observé avec un blocage large de la TGF-β, suggérant que cibler uniquement la TGF-β1 latente peut reprogrammer l’environnement tumoral de manière similaire.
Signaux de sécurité chez les animaux
Étant donné que des tentatives antérieures de bloquer la TGF-β de façon étendue ont rencontré des problèmes de sécurité, l’équipe a réalisé des études de toxicité de 13 semaines chez la souris et chez le singe cynomolgus, administrant à répétition des doses élevées de SOF10. Le médicament s’est comporté comme un anticorps typique dans le plasma, et sur une large plage de doses il n’y a eu aucun signe de lésions des organes majeurs, d’altération des numérations de cellules sanguines ou de dysfonction cardiorespiratoire. Les doses les plus élevées testées—jusqu’à 200 mg/kg toutes les deux semaines chez la souris et 100 mg/kg chez le singe—ont été désignées comme des niveaux sans effets nocifs observés. Ce profil de sécurité soutient l’idée que l’épargne de la TGF-β2, de la TGF-β3 et de l’activation médiée par αvβ6 réduit les risques observés avec des approches antérieures moins sélectives.
Ce que cela pourrait signifier pour les patients
Dans l’ensemble, les résultats suggèrent que verrouiller la TGF-β1 dans sa coquille inactive—plutôt que d’éliminer toute la signalisation TGF-β—peut atténuer la fibrose dans plusieurs organes, améliorer la fonction rénale et rendre les tumeurs récalcitrantes plus vulnérables à l’immunothérapie, le tout avec des signaux de sécurité encourageants chez l’animal. Bien que des essais chez l’humain soient nécessaires pour confirmer ces bénéfices et surveiller les effets à long terme, SOF10 et des stratégies similaires pourraient ouvrir une nouvelle voie pour traiter les maladies fibrosantes chroniques et certains cancers, en réduisant la cicatrisation nocive tout en préservant les rôles de réparation et d’équilibre immunitaire que nos tissus nécessitent encore.
Citation: Kanamori, M., Sato, I., Koo, C.X. et al. Selective blockade of latent TGF-β1 activation suppresses tissue fibrosis with good safety. Commun Med 6, 131 (2026). https://doi.org/10.1038/s43856-026-01408-w
Mots-clés: fibrose, TGF-beta1, anticorps monoclonal, maladies du rein et du foie, immunothérapie du cancer