Clear Sky Science · fr
Caractérisation génomique et sous-clustering du complexe clonale Escherichia coli 38 révèlent des marqueurs génétiques associés à l’hôte
Pourquoi cela importe dans la vie quotidienne
Les infections résistantes aux antibiotiques ne sont plus un problème confiné aux hôpitaux : elles touchent de plus en plus l’alimentation, les animaux, les voyages et la vie communautaire. Cette étude porte sur un groupe particulier de bactéries Escherichia coli, nommé complexe clonale 38 (CC38), qui peut provoquer des infections graves du sang et des voies urinaires et résister souvent à nos antibiotiques les plus importants. En retraçant l’origine de ces bactéries et leurs déplacements entre humains, animaux et environnement, les chercheurs mettent au jour des indices susceptibles d’aider les autorités sanitaires à arrêter des souches dangereuses avant qu’elles ne se propagent largement.
Un examen plus attentif d’une famille bactérienne problématique
Tous les E. coli ne sont pas nuisibles, mais certaines lignées sont des récidivistes dans les maladies sévères. Le CC38 a récemment émergé comme l’un de ces groupes problématiques, se classant juste derrière une lignée à haut risque bien connue (ST131) dans les infections sanguines au Danemark. L’équipe a examiné 242 E. coli CC38 résistants provenant de patients danois, 83 provenant d’aliments et d’animaux d’élevage, et plus de 2 300 génomes apparentés collectés dans le monde. Ils ont utilisé le séquençage du génome entier — lire essentiellement l’ADN de chaque bactérie — pour cartographier les relations entre les différentes branches de cette famille, les gènes de résistance qu’elles portent et les hôtes auxquels elles sont associées.
Suivre la piste des hôpitaux aux fermes et aux aliments
Lorsque les chercheurs ont comparé les E. coli CC38 de patients danois à ceux provenant de volailles, d’animaux d’élevage et de produits alimentaires, ils ont identifié deux principaux groupes danois. Un groupe était principalement composé d’infections humaines, tandis que l’autre contenait des bactéries issues de volailles, d’autres animaux d’élevage et de produits alimentaires. Fait important : il n’y avait pas de correspondances d’ADN quasi identiques entre isolats humains et animaux, ce qui suggère l’absence de flambées alimentaires nettes et évidentes au Danemark pendant la période étudiée. Cependant, des modèles statistiques examinant des segments d’ADN accessoires indiquaient que certains sous-groupes associés aux humains ont probablement des origines avicoles, laissant supposer des transferts passés ou indirects de poulets vers l’homme.
Un arbre généalogique mondial avec deux grandes branches
En élargissant l’analyse à un jeu de données mondial de 2 638 génomes, l’équipe a construit un « arbre familial » global pour le CC38. Deux branches majeures se sont distinguées. L’une était fortement liée aux volailles et présentait des niveaux modérés de résistance aux médicaments ainsi que de nombreux traits associés à des maladies graves. L’autre était dominée par des sous-groupes associés aux humains, qui différaient par la résistance, le potentiel pathogène et les hôtes préférentiels. Certains sous-groupes étaient clairement centrés sur l’homme et fortement résistants, tandis que d’autres montraient des profils mixtes, apparaissant chez l’homme, les volailles, la faune, l’eau et les animaux de compagnie. Ce patchwork reflète la capacité du CC38 à s’adapter à différents environnements et espèces hôtes, compliquant les efforts de contrôle.
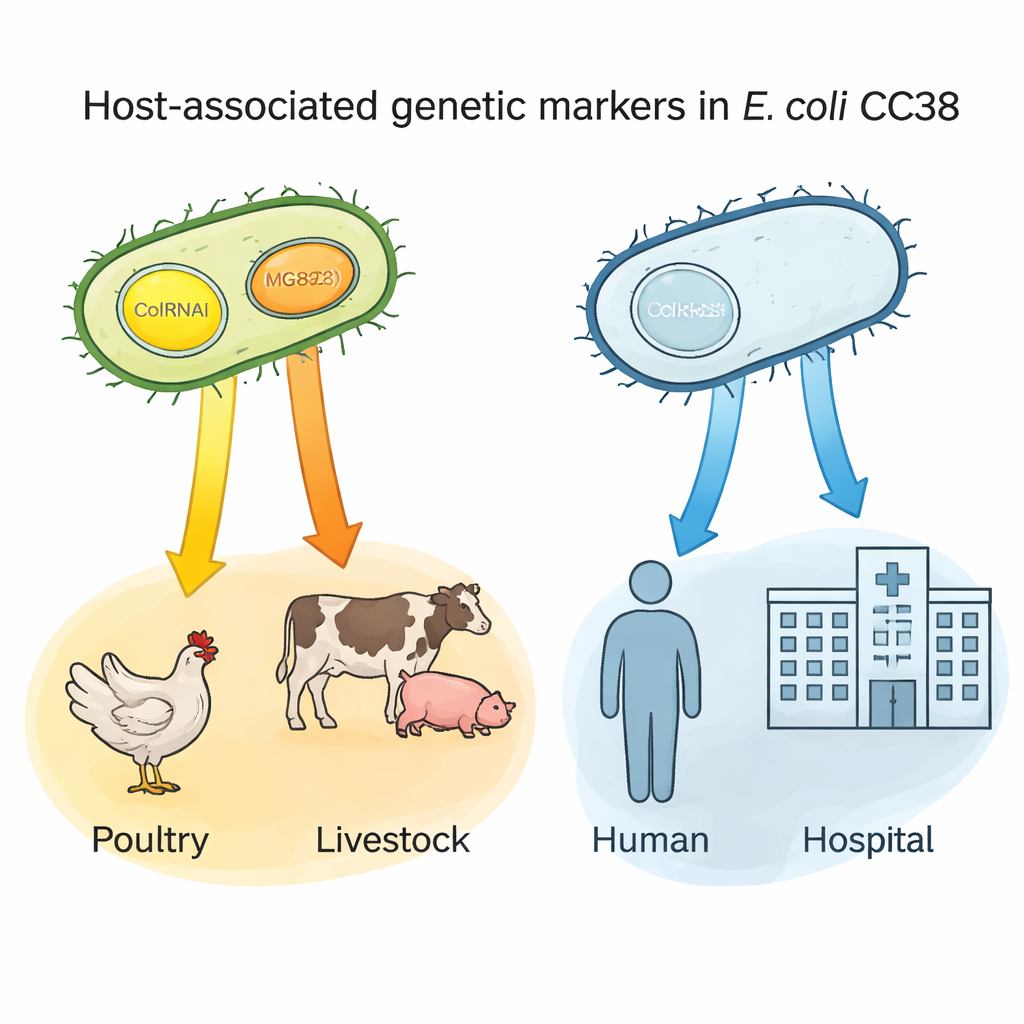
De petits cercles d’ADN comme « étiquettes » d’hôte
Une découverte clé porte sur deux petits morceaux d’ADN — des plasmides appelés ColRNAI et Col(MG828) — capables de se déplacer entre bactéries. Ces plasmides étaient fréquents dans le CC38 issu des volailles et d’autres animaux d’élevage, mais rares dans les sous-groupes centrés sur l’humain. À l’aide d’analyses statistiques, les auteurs ont montré que la présence de l’un ou l’autre plasmide prédisait fortement une origine avicole ; la présence des deux simultanément était particulièrement caractéristique des lignées liées à l’élevage et à certaines sources alimentaires. Comme ces plasmides transportent souvent des gènes de résistance, ils peuvent agir comme des « étiquettes » génétiques signalant des bactéries susceptibles de provenir de réservoirs animaux et aider à retracer la manière dont des souches résistantes entrent dans la chaîne alimentaire et atteignent les humains.
Ce que cela signifie pour la protection de la santé
Pour un non-spécialiste, le message principal est que les E. coli nuisibles et résistants aux médicaments ne sont pas confinés aux hôpitaux ou aux patients : ils forment des populations interconnectées couvrant les humains, les volailles, le bétail, la faune, les aliments et l’environnement. Cette étude montre que, au sein d’une lignée importante, le CC38, certaines branches sont fortement liées aux animaux et d’autres aux humains, et que des éléments d’ADN mobiles spécifiques peuvent aider à révéler l’origine probable d’une souche. Utiliser ces marqueurs génétiques dans la surveillance de routine pourrait fournir un avertissement précoce lorsque des bactéries résistantes associées aux animaux commencent à apparaître chez l’homme. Cela soutient en retour une approche « One Health » — considérer la santé humaine, animale et environnementale comme un même système — pour concevoir des stratégies plus intelligentes et ciblées afin de prévenir les infections et ralentir la propagation de la résistance aux antibiotiques.
Citation: Roer, L., Rasmussen, A., Hansen, F. et al. Genomic characterization and sub-clustering of Escherichia coli clonal complex 38 reveal host associated genetic markers. Commun Med 6, 126 (2026). https://doi.org/10.1038/s43856-026-01402-2
Mots-clés: résistance aux antimicrobiens, Escherichia coli, transmission zoonotique, volailles et élevage, surveillance génomique