Clear Sky Science · fr
Prédiction du pronostic à partir du profilage spatial des protéines dans les cancers du sein triple négatifs
Pourquoi l’agencement des cellules cancéreuses compte
Lorsque les médecins examinent un cancer du sein agressif au microscope, ils observent un paysage dense de cellules tumorales, de cellules immunitaires et de tissus de soutien. Mais jusqu’à récemment, la plupart des tests se sont concentrés sur la quantité d’une molécule donnée, et non sur son emplacement. Cette étude montre que l’arrangement physique des protéines et des cellules dans les cancers du sein triple négatifs peut prédire l’issue pour les patients, et présente une nouvelle méthode pour lire directement ces motifs spatiaux à partir d’images très détaillées.
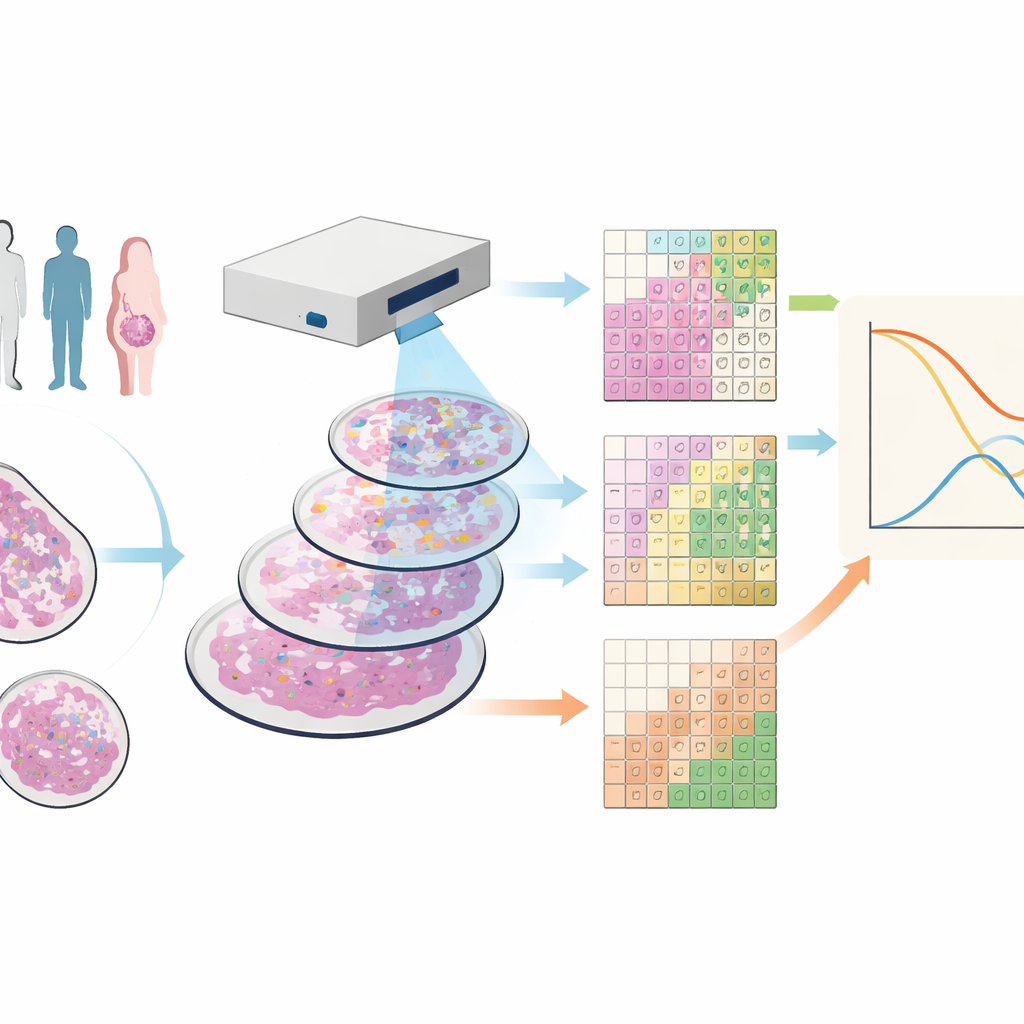
Voir le tissu tumoral en de nombreuses couleurs
Les chercheurs ont travaillé sur des échantillons tissulaires provenant de 88 personnes atteintes d’un cancer du sein triple négatif, une forme de la maladie qui ne présente pas les cibles médicamenteuses courantes et qui a souvent un pronostic défavorable. Ils ont utilisé une technique appelée cytométrie de masse par imagerie, qui colore chaque échantillon avec des dizaines d’anticorps marqués par des métaux. Sous un scanner spécialisé, cela produit des images où chaque point du tissu porte une empreinte détaillée de nombreuses protéines différentes, révélant simultanément les cellules tumorales, divers types de cellules immunitaires, les vaisseaux sanguins et les fibres structurelles.
Découper l’image en tuiles plutôt qu’en cellules
La plupart des outils actuels tentent de tracer des contours autour de chaque cellule puis de les classer par type, un processus qui peut être source d’erreurs et lent, surtout sur des coupes tissulaires fines où les cellules ne sont capturées que partiellement. L’équipe a plutôt créé SparTile, une méthode qui évite de dessiner les contours individuels des cellules. SparTile découpe chaque image en nombreux petits carrés qui se chevauchent, ou tuiles, et utilise des techniques mathématiques pour apprendre les motifs récurrents de combinaisons de protéines à l’intérieur de ces tuiles. Elle regroupe d’abord les tuiles en régions larges — tumeur, tissu de soutien (stroma) ou zones riches en cellules immunitaires — puis subdivise chaque région en « microenvironnements » plus spécifiques, chacun avec son propre mélange de protéines et de types cellulaires voisins.
Quartiers cachés liés au pronostic des patients
Une fois ces microenvironnements cartographiés, les scientifiques ont mesuré la fréquence de chaque motif dans l’échantillon de chaque patient et ont comparé ces données à la survie à long terme. Plusieurs corrélations marquantes sont apparues. Un microenvironnement centré sur la tumeur, riche en une protéine appelée MX1 et en marqueurs de cellules myéloïdes, était associé à un risque de décès nettement plus élevé. Un autre motif tumoral marqué par la vimentine — indice queles cellules tumorales ont basculé vers un état plus mobile et invasif — était également fortement corrélé à une survie défavorable. En revanche, les zones dominées par certains lymphocytes T étaient liées à de meilleurs résultats, tandis que les régions riches en cellules B montraient des effets plus faibles, peut-être parce qu’elles étaient rares dans les petits carottes tissulaires analysées.
La distance entre tumeur et cellules immunitaires comme signal d’alerte
Au-delà de la présence de microenvironnements particuliers, leurs relations spatiales importaient aussi. L’équipe a évalué la proximité entre les régions tumorales et les régions riches en cellules myéloïdes en calculant une mesure statistique du chevauchement spatial de leurs signaux protéiques. Les patients dont les tumeurs présentaient des zones riches en myéloïdes nichées au sein des cellules tumorales avaient tendance à évoluer moins bien que ceux où les deux populations étaient plus séparées. Cette mesure de « distance » est demeurée un puissant prédicteur de risque même après prise en compte des facteurs cliniques standard, et son importance a été confirmée lorsqu’elle a été testée sur deux jeux de données d’images de cancers du sein indépendants provenant d’autres équipes de recherche.
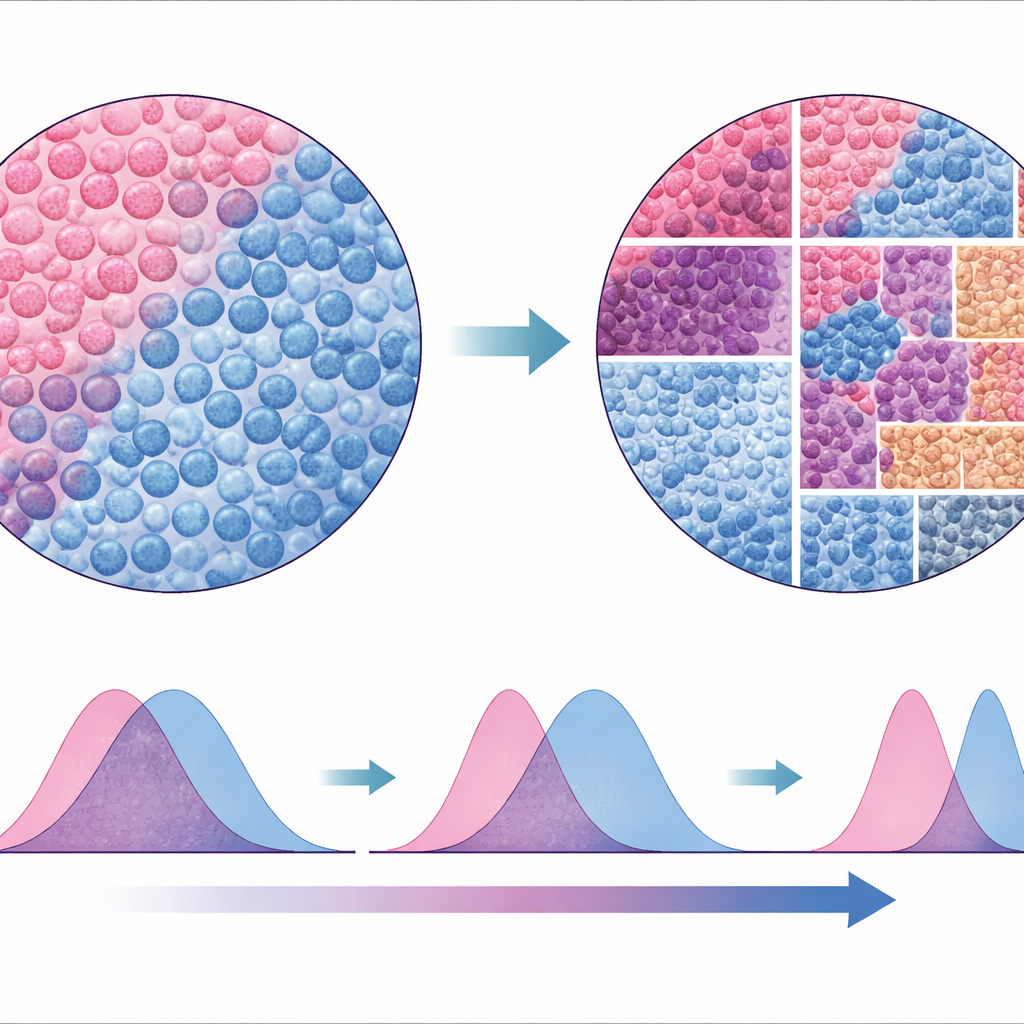
Une nouvelle manière de lire le paysage tumoral
Pour tester la robustesse de leur approche, les auteurs ont comparé SparTile aux méthodes traditionnelles qui reposent sur la segmentation et la classification des cellules individuelles puis sur la construction de voisinages autour d’elles. Si les analyses basées sur les cellules ont retrouvé certains des mêmes motifs, elles étaient moins cohérentes entre les jeux de données et moins fiables pour signaler certains microenvironnements à risque, comme ceux impliquant MX1 et les cellules myéloïdes. Parce que SparTile fonctionne directement sur les images protéiques brutes, elle évite nombre d’hypothèses et d’écueils techniques des approches cellule par cellule, tout en pouvant être combinée ensuite avec elles lorsque des types cellulaires détaillés sont nécessaires pour planifier des expériences ou des thérapies.
Ce que cela signifie pour les patients et les soins futurs
Ce travail montre que non seulement les ingrédients, mais aussi l’agencement d’une tumeur importe pour prédire l’évolution d’un patient atteint d’un cancer du sein triple négatif. En convertissant des images multi-protéines complexes en motifs spatiaux interprétables et en mesures de distance simples, SparTile offre un moyen d’identifier les patients à haut risque à partir de petits échantillons tissulaires et de révéler des agencements biologiques qui pourraient être ciblés par des traitements futurs. Bien que des validations supplémentaires soient nécessaires avant d’en faire un outil de la pratique courante, l’approche ouvre la voie à un avenir où la « carte » d’une tumeur devient aussi importante que sa liste de composants moléculaires.
Citation: Foroughi pour, A., Wu, TC., Noorbakhsh, J. et al. Prediction of outcome from spatial Protein profiling of triple-negative breast cancers. Commun Med 6, 133 (2026). https://doi.org/10.1038/s43856-026-01400-4
Mots-clés: cancer du sein triple négatif, microenvironnement tumoral, protéomique spatiale, cytométrie de masse par imagerie, biomarqueurs pronostiques