Clear Sky Science · fr
IdentifiHR prédit l’insuffisance de recombinaison homologue dans le carcinome ovarien séreux de haut grade en utilisant l’expression génique
Pourquoi cette recherche compte pour les patientes atteintes du cancer de l’ovaire
Pour les personnes atteintes d’un carcinome ovarien séreux de haut grade, l’une des formes les plus mortelles du cancer de l’ovaire, le choix du traitement peut être une question de vie ou de mort. Environ la moitié de ces tumeurs présentent une faiblesse dans leurs mécanismes de réparation de l’ADN, ce qui les rend particulièrement sensibles à certains médicaments appelés inhibiteurs de PARP. Le défi consiste à déterminer, pour chaque patiente, si sa tumeur présente cette vulnérabilité. Cette étude présente IdentifiHR, un nouvel outil qui lit des motifs d’activité génique, plutôt que de se baser uniquement sur les mutations de l’ADN, pour prédire quelles tumeurs ont une réparation de l’ADN défaillante et pourraient tirer le plus grand bénéfice de ces traitements ciblés.
Des cicatrices de l’ADN aux motifs d’activité génique
Quand une cellule perd une voie majeure de réparation appelée recombinaison homologue, elle commence à recoller son ADN en utilisant des mécanismes plus sujets aux erreurs. Avec le temps, cela laisse un profil caractéristique de « cicatrices » à l’échelle du génome — régions manquantes, copies supplémentaires et segments de chromosomes brisés. Les tests cliniques existants recherchent ces cicatrices directement dans l’ADN ou des mutations spécifiques dans des gènes clés tels que BRCA1 et BRCA2. Ces tests sont puissants mais exigent un séquençage ADN étendu et ne reflètent pas toujours l’état de réparation actuel de la tumeur. Les auteurs se sont demandé si une autre couche biologique — le profil des gènes activés ou réprimés dans la tumeur — pouvait servir de lecture en temps réel de ces dommages et être utilisée pour classer les tumeurs comme déficientes ou compétentes en réparation.
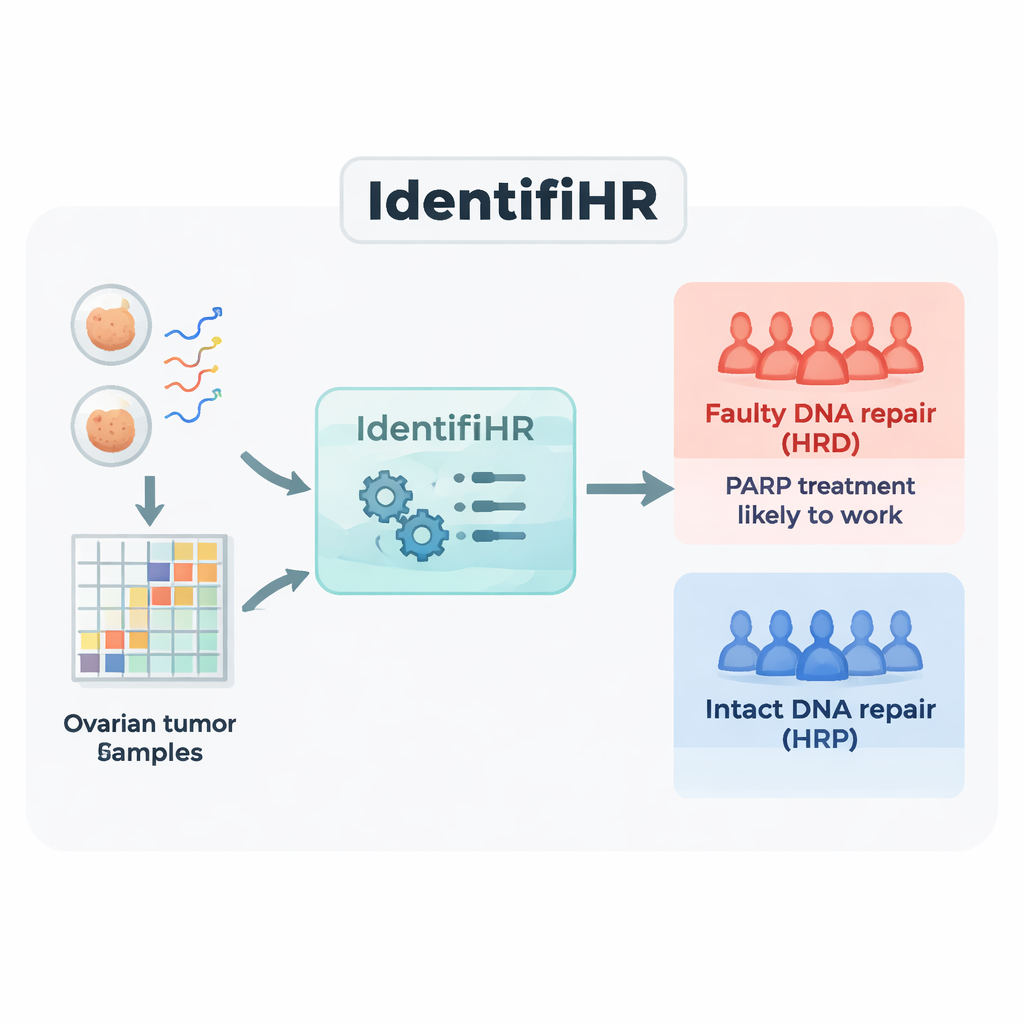
Construction d’un prédicteur basé sur les gènes, IdentifiHR
L’équipe a commencé avec des données de séquençage ARN de 361 tumeurs ovariennes provenant d’une grande ressource publique, The Cancer Genome Atlas. Le séquençage ARN mesure quels gènes sont actifs, et à quel degré, dans chaque échantillon. Ils ont divisé les tumeurs en un groupe d’entraînement et un groupe de test, étiquetant chaque cas comme déficient en réparation (HRD) ou compétent en réparation (HRP) en utilisant la norme actuelle basée sur l’ADN qui combine plusieurs mesures des cicatrices génomiques. Dans les tumeurs d’entraînement, ils ont identifié 2 604 gènes dont l’activité différait de façon constante entre les cancers HRD et HRP. Nombre de ces gènes se situaient dans des régions du génome déjà connues pour être fréquemment gagnées ou perdues dans les tumeurs déficientes en réparation, montrant que le signal d’expression génique reflétait les dommages ADN sous-jacents.
Un signature de 209 gènes qui suit l’état de réparation
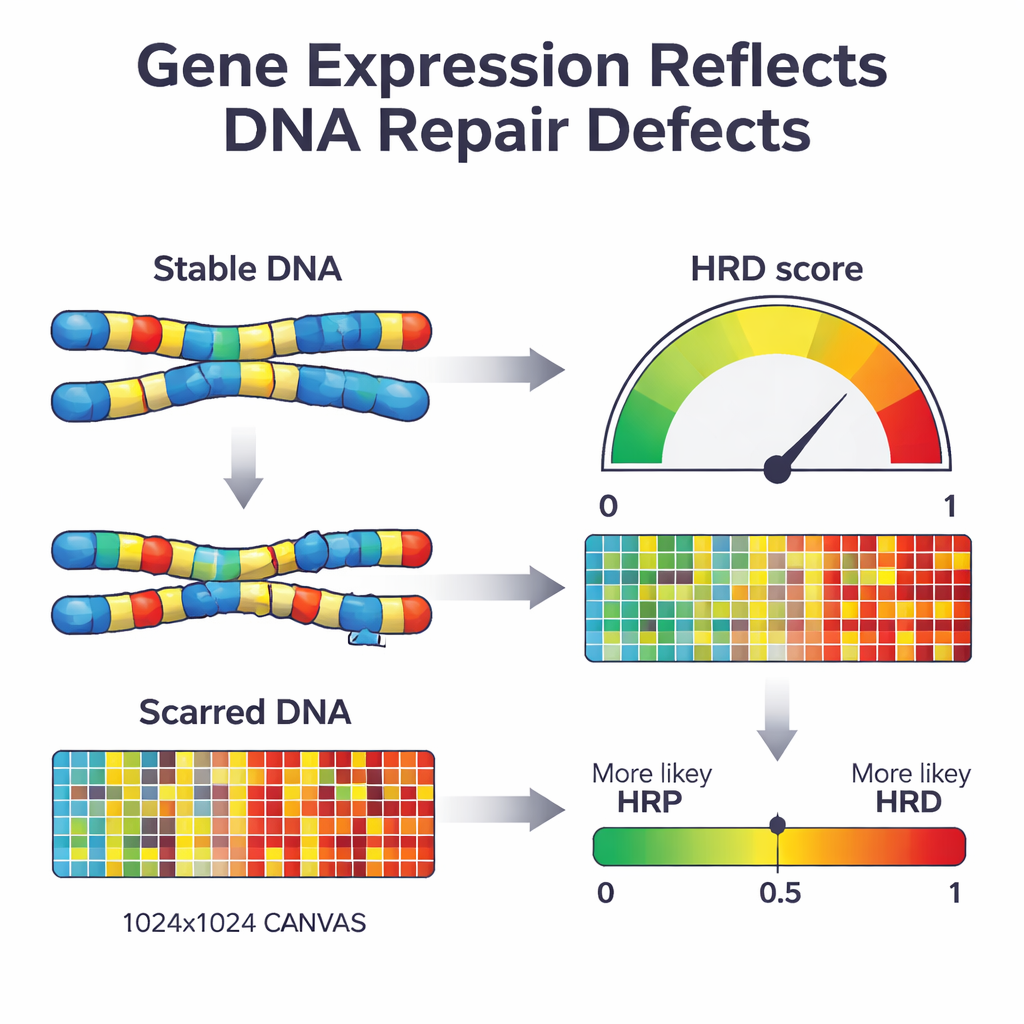
Ensuite, les chercheurs ont utilisé une approche d’apprentissage automatique connue sous le nom de régression logistique pénalisée pour réduire cette liste de 2 604 gènes au jeu d’information le plus pertinent. Le modèle obtenu, nommé IdentifiHR, s’appuie sur l’activité de seulement 209 gènes pour estimer la probabilité qu’une tumeur soit déficiente en réparation. Fait intéressant, un seul de ces gènes est un gène de réparation de l’ADN classique ; la plupart sont des gènes ordinaires dont l’activité est modifiée en raison de changements plus larges de la structure chromosomique. IdentifiHR ne fournit pas simplement une étiquette oui/non — il produit un score de probabilité qui suit de manière continue le score de dommages basé sur l’ADN, reflétant l’idée que l’insuffisance de réparation se situe sur un spectre plutôt que comme un état binaire.
Test de l’outil sur plusieurs cohortes de patientes
Les auteurs ont rigoureusement testé IdentifiHR sur trois jeux de données indépendants qui n’avaient jamais été utilisés lors de l’entraînement. Dans le sous-ensemble mis de côté de The Cancer Genome Atlas, le modèle a correctement distingué les tumeurs HRD des tumeurs HRP dans environ 85 % des cas. Il a obtenu des performances similaires — environ 86 % de précision — dans une étude australienne distincte qui incluait non seulement des tumeurs primaires mais aussi des échantillons prélevés à l’autopsie, du liquide abdominal (ascite) et des trompes de Fallope normales, le site probable d’origine de beaucoup de ces cancers. Dans chaque échantillon de trompe de Fallope normale, IdentifiHR a correctement prédit une réparation de l’ADN intacte. L’outil a également fonctionné sur des données monocellulaires « pseudo-agrégées », où des milliers de cellules cancéreuses individuelles ont été combinées informatiquement pour imiter un échantillon en masse, atteignant à nouveau environ 84 % de précision. Dans ces différents tests, IdentifiHR a égalé ou dépassé les performances de plusieurs méthodes basées sur l’expression génique existantes, développées à l’origine pour d’autres cancers ou pour prédire des scores de dommages apparentés.
Comment cela pourrait changer la recherche et les soins
Parce qu’IdentifiHR s’exécute sur des données d’ARN, souvent moins coûteuses et plus faciles à obtenir que des profils ADN à l’échelle du génome, il offre une voie pratique pour que les chercheurs — et potentiellement, à l’avenir, les cliniciens — estiment l’état de réparation de l’ADN lorsque seules des données d’expression génique sont disponibles. Le modèle est publié sous forme de package R open-source, de sorte que tout groupe disposant de données de séquençage appropriées peut l’appliquer. Bien qu’il ne remplace pas encore les tests ADN considérés comme étalon-or, et que sa capacité à détecter des changements plus subtils tels que la restauration de la réparation doive encore être étudiée, IdentifiHR fournit une nouvelle lentille puissante pour identifier quelles tumeurs ovariennes sont les plus susceptibles de répondre aux inhibiteurs de PARP et à des médicaments similaires. Pour les patientes, cette voie rapproche le domaine de décisions thérapeutiques plus précises et guidées par la biologie réelle du comportement de leurs cellules cancéreuses.
Citation: Weir, A.L., Lee, S.C., Li, M. et al. IdentifiHR predicts homologous recombination deficiency in high-grade serous ovarian carcinoma using gene expression. Commun Med 6, 119 (2026). https://doi.org/10.1038/s43856-026-01387-y
Mots-clés: cancer de l’ovaire, réparation de l’ADN, insuffisance de recombinaison homologue, expression génique, apprentissage automatique