Clear Sky Science · fr
Déficit de recombinaison homologue dans les cancers du sein primaires ER‑positifs et HER2‑négatifs
Pourquoi c’est important pour les patientes atteintes de cancer du sein
La plupart des cancers du sein appartiennent à un large groupe dit récepteur d’œstrogène positif et HER2‑négatif. Ces tumeurs sont généralement traitées par des médicaments bloquant les hormones, parfois en association avec une chimiothérapie. Pourtant, de nombreuses patientes rechutent et les cliniciens manquent d’outils précis pour décider qui a réellement besoin d’un traitement intensif ou pourrait bénéficier de nouvelles thérapies ciblées. Cette étude examine une faiblesse spécifique de certaines tumeurs — appelée déficit de recombinaison homologue, ou HRD — qui rend les cellules cancéreuses moins aptes à réparer les cassures de l’ADN, ouvrant potentiellement la voie à des traitements plus personnalisés.
Une faiblesse cachée présente seulement dans certaines tumeurs
La recombinaison homologue est l’un des principaux mécanismes cellulaires pour réparer des cassures d’ADN dangereuses. Quand ce système échoue — souvent à cause d’altérations de gènes bien connus comme BRCA1, BRCA2, PALB2 ou RAD51C — les cellules accumulent des mutations et peuvent devenir particulièrement sensibles à certains médicaments, y compris les chimiothérapies à base de platine et les inhibiteurs de PARP. L’HRD est fréquent dans une forme agressive de cancer du sein appelée triple‑négatif, mais son rôle dans le groupe plus courant récepteur d’œstrogène positif, HER2‑négatif, était incertain. Pour clarifier cela, les chercheurs ont analysé 502 tumeurs de ce type issues de l’étude suédoise SCAN‑B par séquençage du génome entier, en croisant ces données avec l’activité génique, la méthylation de l’ADN, les traitements reçus et le suivi à long terme.
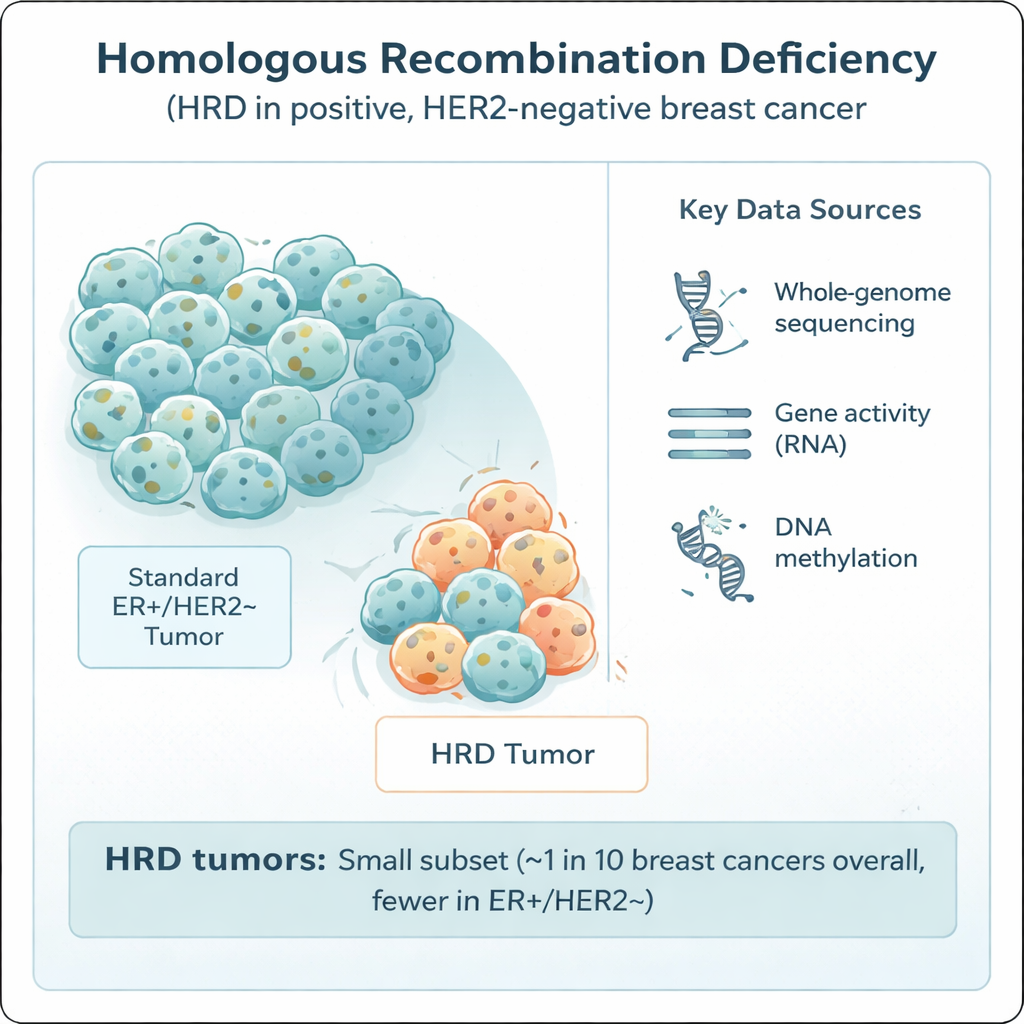
Comment l’étude a été réalisée
Toutes les tumeurs ont été prélevées au moment de la chirurgie, avant tout traitement médicamenteux, offrant un instantané clair de leur biologie d’origine. L’équipe a utilisé un outil sophistiqué de reconnaissance de motifs, HRDetect, pour lire les « signatures mutationnelles » laissées dans l’ADN tumoral lorsque la recombinaison homologue est défaillante. Les tumeurs ont été classées comme HRD si elles dépassaient un seuil strict de probabilité. Les scientifiques ont également comparé différentes méthodes de détection de l’HRD — des scores basés sur l’ADN à un test d’expression génique basé sur l’ARN — afin d’évaluer la concordance entre approches. De plus, ils ont examiné des caractéristiques plus larges comme la charge mutatoire globale, les schémas de gains et pertes chromosomiques, l’activité des gènes liés au système immunitaire et les marques chimiques sur l’ADN (méthylation) qui peuvent activer ou réprimer des gènes.
Quelle est la fréquence de l’HRD, et qu’en est‑il des causes ?
Les chercheurs ont constaté que seulement 8,4 % des tumeurs récepteur d’œstrogène positif, HER2‑négatif dans leur cohorte séquencée présentaient des preuves nettes d’HRD — bien moins que les ~60 % observés dans le cancer triple‑négatif. En combinant ces données avec des registres nationaux et d’autres études, ils estiment qu’environ 1 tumeur sur 20 dans ce sous‑groupe clinique, et environ 1 cas sur 9 des cancers du sein au total dans les populations d’Europe de l’Ouest/Nordiques, sont HRD. Dans les tumeurs HRD, ils ont souvent pu identifier une cause probable : environ 70 % présentaient des atteintes claires de BRCA1, BRCA2, RAD51C ou PALB2, par des mutations héréditaires, des mutations ou délétions spécifiques à la tumeur, ou par le silencement épigénétique des promoteurs géniques. Fait marquant, environ un tiers des cas HRD étaient dus à une hyperméthylation du promoteur — un enrobage chimique qui éteint les gènes de réparation de l’ADN sans en modifier la séquence. Cependant, près de 30 % des tumeurs HRD n’affichaient pas de coupable unique évident, suggérant des mécanismes supplémentaires, encore inconnus, menant à cette défaillance de réparation.
À quoi ressemblent les tumeurs HRD au microscope et en clinique
Les tumeurs HRD au sein de ce groupe fréquent avaient tendance à présenter des caractéristiques d’une maladie plus agressive : elles avaient souvent des taux de division cellulaire plus élevés, des niveaux d’intensité de récepteurs hormonaux plus faibles et des génomes plus complexes et riches en mutations que les tumeurs compétentes en recombinaison homologue. Elles apparaissaient dans presque tous les grands sous‑types moléculaires, mais étaient rares dans la classe plus indolente Luminal A et relativement surreprésentées dans un sous‑ensemble plus petit de type basal‑like. Pourtant, lorsqu’ils ont examiné l’activité génique globale et les profils de méthylation, les tumeurs HRD ne formaient pas un profil unique et facilement reconnaissable. Leurs profils d’expression étaient variés et les différences au sein de sous‑types spécifiques restaient modestes. Certaines tumeurs HRD, en particulier dans les groupes Luminal B et basal‑like, présentaient des signaux immunitaires plus élevés et une expression accrue de PD‑L1, laissant penser qu’elles pourraient être davantage visibles par le système immunitaire et potentiellement plus réceptives à l’immunothérapie.
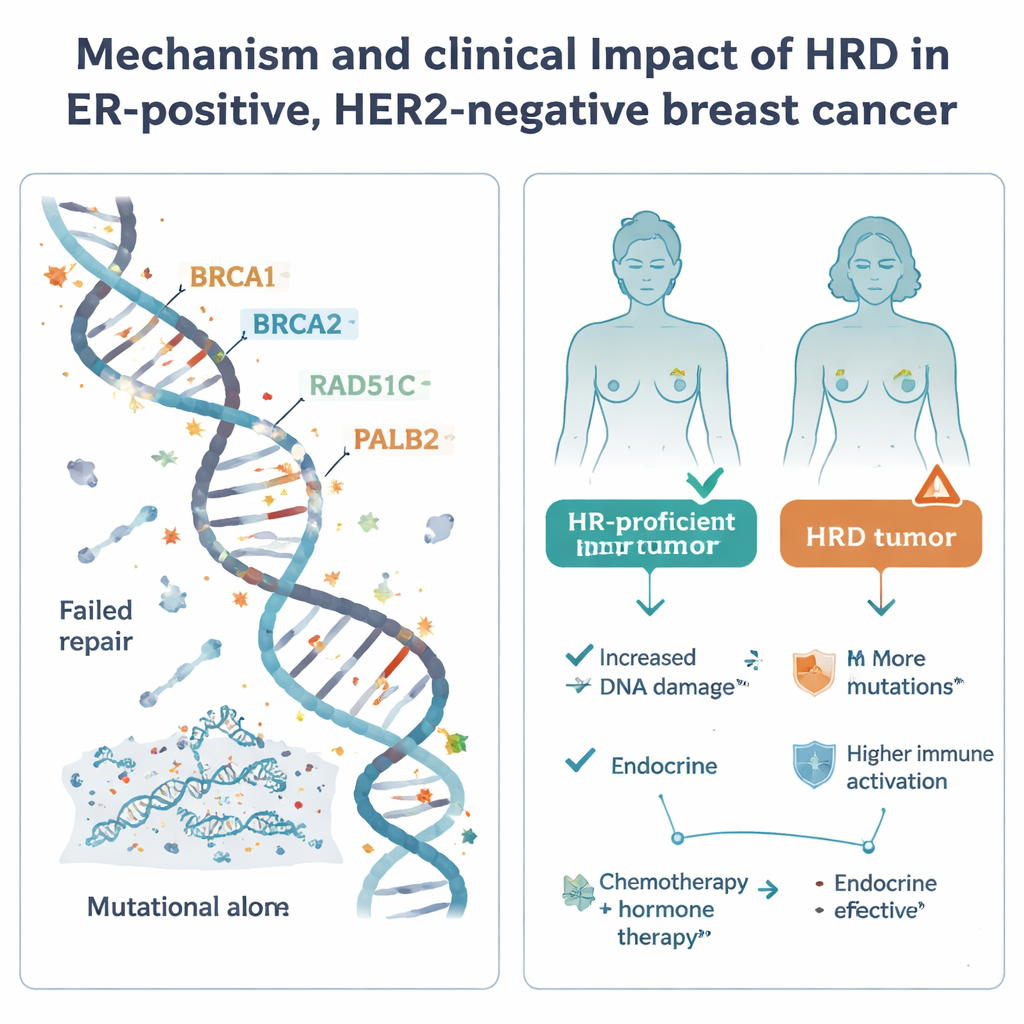
L’HRD modifie‑t‑il le pronostic des patientes ?
L’étude a ensuite examiné comment le statut HRD se corrélait aux résultats réels sous soins standards. Chez les patientes traitées uniquement par hormonothérapie après chirurgie, les tumeurs HRD montraient une tendance vers une survie sans récidive à distance plus faible, bien que le nombre de cas HRD fût limité et que le résultat n’atteigne pas la significativité statistique formelle. Ce schéma, associé à leurs caractéristiques moléculaires agressives, suggère que se fier uniquement à l’hormonothérapie peut être risqué pour les patientes porteuses de tumeurs HRD. En revanche, chez les patientes ayant reçu à la fois chimiothérapie et hormonothérapie, le statut HRD n’était pas clairement lié à de meilleurs ou pires résultats ; tous les groupes présentaient des taux de rechute globalement similaires, et la chimiothérapie pourrait atténuer en partie le risque supplémentaire lié à l’HRD.
Que signifie cela pour les choix thérapeutiques futurs
Pour le lecteur non spécialiste, le message principal est que seule une minorité des cancers du sein récepteur d’œstrogène positif, HER2‑négatif présente cette faiblesse particulière de réparation de l’ADN, mais lorsque l’HRD est présente elle indique souvent une maladie plus agressive qui peut ne pas être bien contrôlée par l’hormonothérapie seule. Les résultats soutiennent l’idée que le séquençage du génome entier peut identifier de manière fiable l’HRD et en clarifier les causes sous‑jacentes, au‑delà du simple dépistage des mutations héréditaires BRCA1 ou BRCA2. Bien que l’étude ne prouve pas encore que modifier le traitement en fonction du statut HRD améliore la survie, elle fournit des preuves préliminaires que les patientes ayant des tumeurs HRD pourraient tirer avantage de la chimiothérapie et, dans de futurs essais, des inhibiteurs de PARP ou des immunothérapies. En bref, le test HRD pourrait devenir un élément d’un arsenal plus fin pour adapter l’intensité du traitement — et les nouvelles options ciblées — à la biologie de chaque cancer du sein.
Citation: Davies, H.R., Black, D., Kvist, A. et al. Homologous recombination deficiency in primary ER-positive and HER2-negative breast cancer. Commun Med 6, 118 (2026). https://doi.org/10.1038/s43856-026-01385-0
Mots-clés: cancer du sein, réparation de l’ADN, gènes BRCA, Séquençage du génome, thérapie ciblée