Clear Sky Science · fr
Signature structurale des protéines plasmatiques classifie le statut de la maladie d’Alzheimer
Pourquoi un test sanguin pour la perte de mémoire compte
La maladie d’Alzheimer est souvent bien installée longtemps avant que des problèmes de mémoire ne deviennent évidents, mais les tests actuels pour la repérer tôt peuvent être invasifs, coûteux ou difficiles d’accès. Cette étude explore une idée différente : savoir si de minuscules modifications des formes tridimensionnelles des protéines circulant dans le sang peuvent révéler la position d’une personne sur le continuum du vieillissement sain à un léger oubli jusqu’à la maladie d’Alzheimer complète. Si cela fonctionne, un tel test sanguin pourrait simplifier le dépistage, favoriser un traitement plus précoce et aider les chercheurs à suivre qui bénéficie des nouvelles thérapies.
Regarder la forme des protéines, pas seulement la quantité
La plupart des analyses sanguines mesurent la quantité d’une molécule donnée. Ici, les chercheurs se sont plutôt focalisés sur la forme des protéines. À l’intérieur de nos cellules, un système de contrôle qualité maintient les protéines correctement repliées ; quand ce système flanche avec l’âge, des protéines mal repliées peuvent s’accumuler et endommager les cellules cérébrales. L’équipe s’est demandé si cette défaillance de « l’entretien » des protéines laissait une empreinte structurale dans les protéines sanguines. À partir de 520 volontaires, soit cognitivement sains, soit atteints d’un trouble cognitif léger (TCL) ou de la maladie d’Alzheimer, ils ont prélevé du sang et utilisé une technique chimique appelée profilage covalent des protéines pour marquer les parties exposées des protéines. Plus un site est exposé, plus il est facilement marqué, fournissant une lecture numérique de la structure protéique en grande partie indépendante de la quantité de protéine présente.
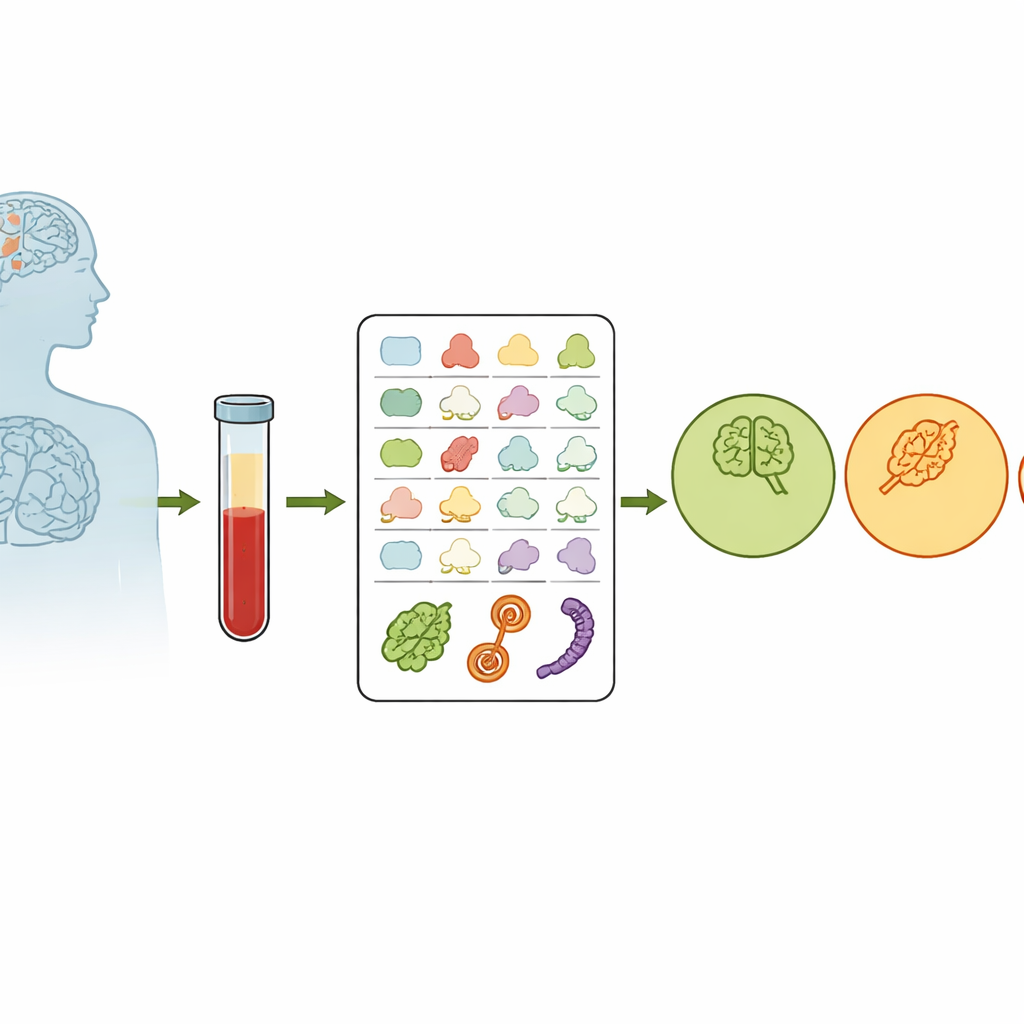
Détecter des empreintes structurelles dans le sang
Sur près de 900 fragments protéiques marqués, les chercheurs ont observé une tendance subtile mais cohérente : à mesure que les personnes passaient de l’état sain au TCL puis à l’Alzheimer, certaines surfaces protéiques devenaient moins exposées et plus variables d’un individu à l’autre. Ce schéma est compatible avec l’idée que le contrôle du repliement des protéines se détériore à mesure que la maladie progresse. L’équipe a également examiné comment un facteur génétique majeur de risque pour l’Alzheimer, la variante APOE ε4, influençait la structure des protéines. Ils ont constaté que les porteurs de deux copies de ε4 présentaient des modifications structurelles distinctes dans plusieurs protéines interagissant avec la protéine APOE, ce qui suggère que ce gène à risque modifie non seulement quelles protéines sont présentes, mais aussi comment elles sont repliées et organisées.
Relier les protéines sanguines à l’humeur et au comportement
L’Alzheimer affecte bien plus que la mémoire ; des symptômes tels que l’agitation, la dépression et les hallucinations sont fréquents et diffèrent souvent entre hommes et femmes. Les chercheurs ont combiné des évaluations cliniques de 12 types de symptômes neuropsychiatriques avec leurs mesures de forme protéique. Dans les deux sexes, des symptômes plus sévères étaient généralement associés à des protéines devenant plus structurellement « fermées ». Certaines protéines, dont la clusterine et plusieurs autres liées à l’accumulation d’amyloïde, suivaient la sévérité des symptômes de façon similaire chez les hommes et les femmes, tandis que d’autres présentaient des schémas spécifiques au sexe. Ces résultats laissent entrevoir que la structure des protéines sanguines pourrait refléter non seulement la présence de la maladie, mais aussi la manière dont elle se manifeste dans le comportement et l’humeur.
Un panel de trois protéines pour classifier le stade de la maladie
Pour transformer ces mesures complexes en outil cliniquement utile, l’équipe a injecté les données structurelles dans 18 approches d’apprentissage automatique différentes. Le modèle le plus performant, basé sur l’apprentissage profond, s’appuyait sur seulement trois fragments protéiques issus de C1QA, de la clusterine (aussi appelée CLUS) et de l’apolipoprotéine B (ApoB). En n’utilisant que les relevés structuraux de ces trois fragments, le modèle a correctement classé les personnes en groupes sain, TCL ou Alzheimer dans environ 83 % des cas sur un jeu de test indépendant. Lorsqu’on lui posait des questions plus simples à deux voies — par exemple distinguer sain de TCL, ou TCL d’Alzheimer — les performances du panel étaient encore meilleures, avec des mesures de précision comparables ou supérieures à de nombreuses approches sanguines actuelles qui se concentrent sur les quantités de protéines plutôt que sur leur structure.
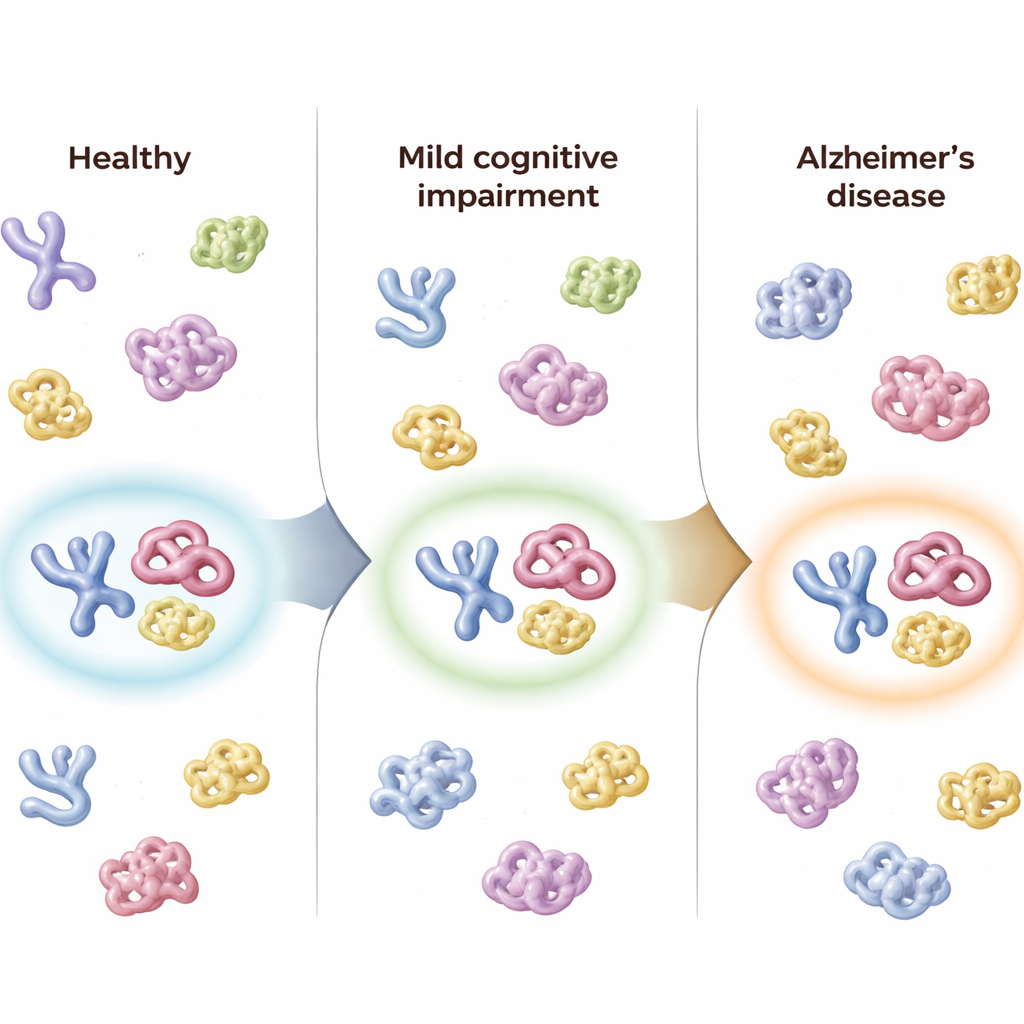
Suivi des personnes dans le temps
Les chercheurs disposaient aussi d’échantillons de suivi de 50 participants prélevés jusqu’à environ huit mois plus tard. Chez les personnes dont le diagnostic s’est aggravé — par exemple de sain à TCL, ou de TCL à Alzheimer — le score combiné du panel à trois protéines a évolué dans le même sens, reflétant la progression de la maladie. En revanche, les individus dont l’état clinique est resté stable ont montré peu de variation de leur score de panel. Le score global de « confiance Alzheimer » du panel suivait de près les tests cognitifs standards, les mesures du fonctionnement quotidien, l’atrophie cérébrale visible en IRM et les marqueurs établis d’amyloïde et de tau dans le liquide céphalorachidien, suggérant que le signal structurel sanguin reflète les changements cérébraux sous-jacents.
Ce que cela pourrait signifier pour les patients
Dans l’ensemble, le travail montre que de petits changements coordonnés dans les formes d’un petit nombre de protéines plasmatiques abondantes peuvent indiquer de façon fiable si une personne est cognitivement saine, légèrement déficiente ou atteinte de la maladie d’Alzheimer. Parce que le test utilise le sang plutôt que le liquide céphalorachidien ou l’imagerie cérébrale, il pourrait, en principe, être étendu au dépistage de routine ou pour sélectionner et suivre les participants dans les essais cliniques. Les auteurs soulignent néanmoins que des études plus vastes et plus longues sont nécessaires, et que la chimie impliquée reste spécialisée. Néanmoins, leurs résultats mettent en avant la structure des protéines — pas seulement leur concentration — comme une nouvelle source d’information prometteuse pour détecter et suivre la maladie d’Alzheimer plus tôt et avec plus de précision.
Citation: Son, A., Kim, H., Diedrich, J.K. et al. Structural signature of plasma proteins classifies the status of Alzheimer’s disease. Nat Aging 6, 597–611 (2026). https://doi.org/10.1038/s43587-026-01078-2
Mots-clés: Biomarqueurs de la maladie d’Alzheimer, test sanguin pour la démence, modifications du repliement des protéines, diagnostic par apprentissage automatique, clusterine et C1QA