Clear Sky Science · fr
La résistance au traitement par chimiothérapie à base de platine dans les cancers du poumon et de l’ovaire est provoquée par un secretome sénescent cibleable par TGFβ
Quand le traitement du cancer se retourne contre lui
La chimiothérapie à base de platine est l’un des piliers du traitement moderne du cancer, en particulier pour les cancers du poumon et de l’ovaire. Elle vise à endommager l’ADN tumoral au point que les cellules cancéreuses ne puissent plus se diviser. Pourtant, de nombreux patients voient leur tumeur régresser au départ, pour ensuite voir la maladie réapparaître, plus résistante. Cette étude pose une question simple mais troublante : ces mêmes médicaments qui sauvent des vies peuvent-ils aussi aider les cellules cancéreuses survivantes à se rétablir ? Les auteurs montrent que la réponse se trouve dans un groupe particulier de cellules endommagées, semblables à des cellules vieillissantes, et dans les messages chimiques puissants qu’elles délivrent.
La double vie des cellules cancéreuses vieillissantes
La chimiothérapie ne traite pas toutes les cellules tumorales de la même manière. Certaines sont détruites net, d’autres entrent dans un état appelé sénescence cellulaire — arrêt définitif de la division tout en restant vivantes. Ces cellules sénescentes prennent du volume et commencent à sécréter un mélange de protéines et de signaux connu sous le nom de phénotype sécrétoire associé à la sénescence, ou SASP. En utilisant des cellules humaines de cancers du poumon et de l’ovaire en culture, ainsi que des modèles murins, les chercheurs ont montré que des agents à base de platine comme le cisplatine et le carboplatine génèrent des cellules sénescentes particulièrement puissantes. Quand des cellules cancéreuses fraîches ont été exposées au fluide prélevé sur ces cultures sénescentes, elles ont proliféré plus rapidement, migré davantage et formé des amas et sphères plus grands et plus agressifs que les cellules témoins.
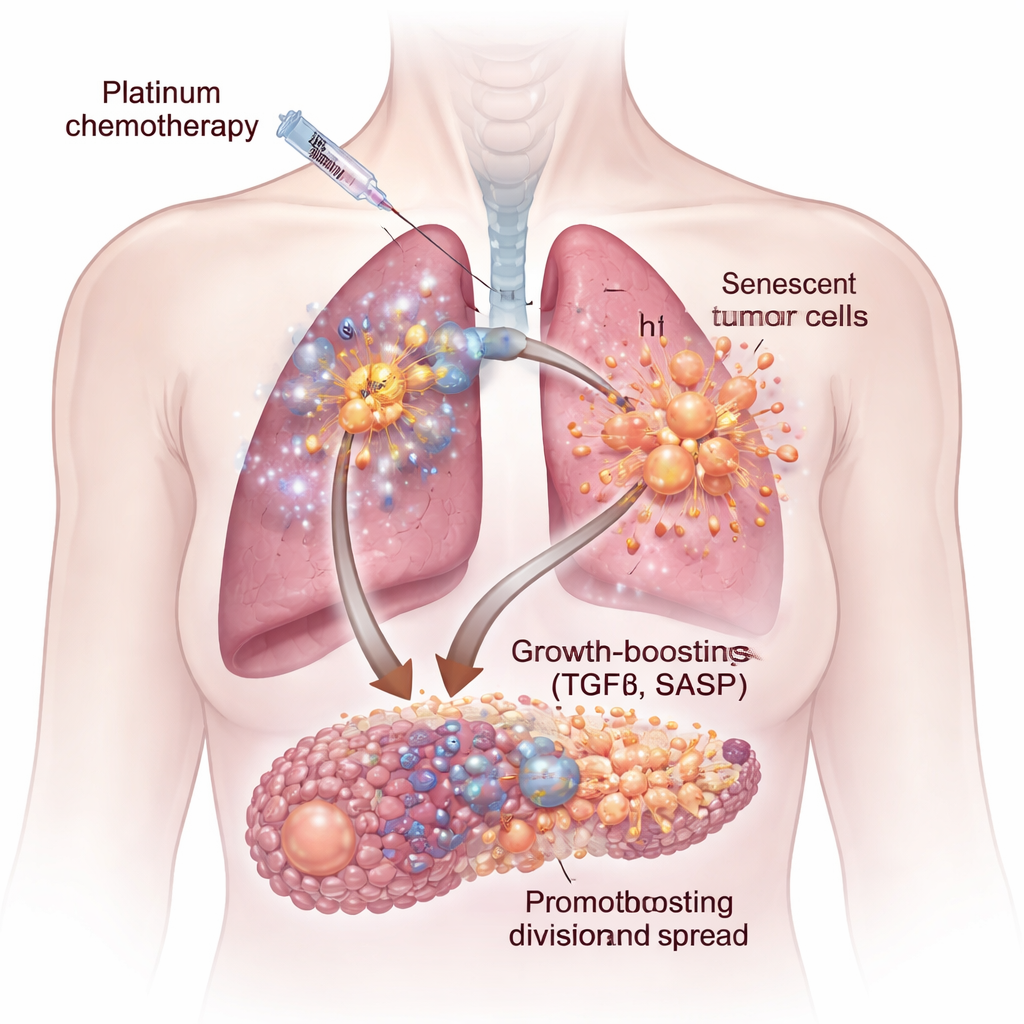
Un signal de croissance caché : le TGFβ
Toutes les chimiothérapies ne déclenchent pas les mêmes sécrétions délétères. Lorsque l’équipe a comparé les agents à base de platine à deux autres traitements courants, le docétaxel et le palbociclib, seules les cellules traitées par platine ont produit un SASP qui stimulait fortement la croissance tumorale. En combinant des études d’expression génique, des mesures protéiques et une microarray de microenvironnements à haut débit, ils ont identifié un coupable principal : la molécule de signalisation transforming growth factor-beta, ou TGFβ. Les cellules sénescentes induites par le cisplatine étaient enrichies en formes multiples de TGFβ et en voies associées. L’ajout de TGFβ purifié aux cellules cancéreuses reproduisait l’effet de stimulation observé avec le fluide sénescent, soulignant cette famille de cytokines comme un moteur central du secretome pro-tumoral.
Comment le signal reprogramme les cellules cancéreuses
L’étude a ensuite retracé comment ces signaux riches en TGFβ modifient le comportement des cellules tumorales voisines. À la surface des cellules réceptrices, le TGFβ se lie à un récepteur appelé TGFBR1. Cela active ensuite une chaîne interne de protéines — en particulier les voies AKT et mTOR — connues pour contrôler la croissance, le métabolisme et la survie cellulaires. Tant dans des cellules de cancer du poumon humaines que murines, l’exposition aux sécrétions dérivées du cisplatine augmentait rapidement les formes activées (phosphorylées) d’AKT et de sa cible en aval p70S6K, et augmentait l’expression de gènes du cycle cellulaire. Bloquer TGFBR1 avec un médicament appelé galunisertib, ou inhiber directement mTOR, réduisait largement cette flambée de signalisation et diminuait la prolifération supplémentaire, la formation de colonies et la croissance invasive en sphères déclenchées par le secretome sénescent.
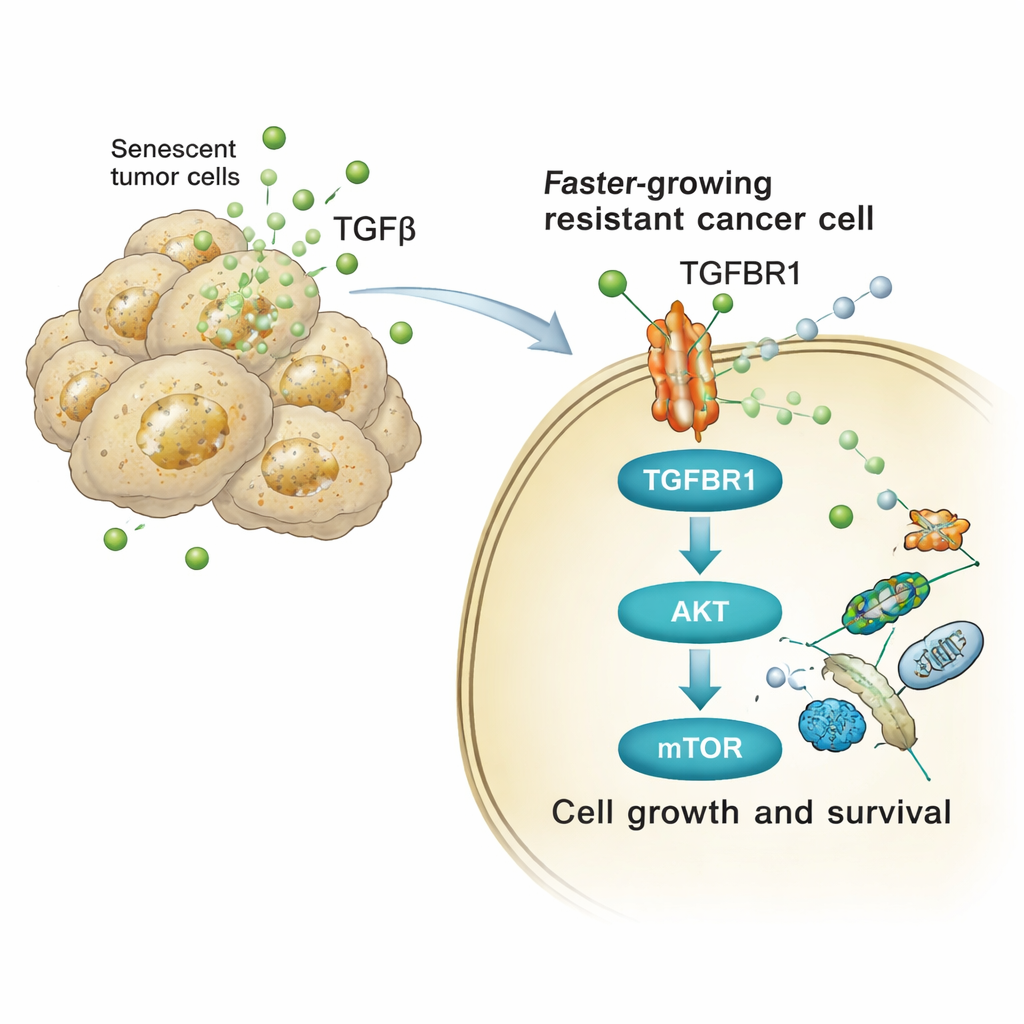
Des souris aux patients : une faiblesse partagée
Ces mécanismes ne se limitaient pas aux boîtes de culture. Chez des souris porteuses de tumeurs pulmonaires, le mélange de cellules cancéreuses sénescentes et non sénescentes conduisait à des tumeurs à croissance plus rapide et à une survie réduite, tandis que l’élimination des cellules sénescentes ou le blocage de TGFBR1 atténuait cet effet. Lorsque le traitement standard au cisplatine a été administré à des souris porteuses de cancers pulmonaires génétiquement modifiés, les tumeurs accumulaient des marqueurs de sénescence accompagnés d’une activité AKT/mTOR élevée dans les cellules voisines encore en division. L’association du cisplatine avec une inhibition de TGFBR1 ou des médicaments sénolytiques (qui éliminent sélectivement les cellules sénescentes) a réduit la charge tumorale et prolongé la survie par rapport à la chimiothérapie seule. De manière cruciale, les analyses d’échantillons humains de cancers du poumon et de cancers séreux de haut grade de l’ovaire prélevés après un traitement à base de platine ont révélé des schémas similaires : augmentation des marqueurs de sénescence et activation renforcée de la voie AKT/mTOR dans le microenvironnement tumoral, en particulier dans les zones riches en cellules sénescentes.
Transformer une faiblesse en atout
Pour le grand public, le message essentiel est que la chimiothérapie au platine peut laisser derrière elle une population de cellules « zombies » endommagées mais dangereuses. Ces cellules tumorales sénescentes ne se divisent plus, mais elles sécrètent des signaux riches en TGFβ qui réveillent les cellules cancéreuses voisines, favorisant la repousse tumorale et la résistance aux traitements ultérieurs. La bonne nouvelle est que cette vulnérabilité est cibleable. Dans des modèles précliniques de cancers du poumon et de l’ovaire, l’ajout de médicaments bloquant le récepteur TGFBR1 ou l’élimination sélective des cellules sénescentes a rendu la chimiothérapie au platine plus efficace et amélioré la survie sans toxicité évidente supplémentaire. Ces travaux ouvrent la voie à des essais cliniques futurs combinant le traitement standard au platine avec des stratégies sénolytiques ou anti‑TGFβ, dans le but de préserver les bénéfices de la chimiothérapie tout en neutralisant ses effets secondaires cachés liés à la sénescence.
Citation: González-Gualda, E., Reinius, M.A.V., Macias, D. et al. Treatment resistance to platinum-based chemotherapy in lung and ovarian cancer is driven by a targetable TGFβ senescent secretome. Nat Aging 6, 368–392 (2026). https://doi.org/10.1038/s43587-025-01054-2
Mots-clés: résistance à la chimiothérapie, sénescence cellulaire, signalisation TGFβ, cancer du poumon, cancer de l’ovaire