Clear Sky Science · fr
Les dommages à l’ADN dans les macrophages provoquent une autoreactivité immune via la présentation d’antigènes nucléaires
Quand l’usure cellulaire fait dérailler le système immunitaire
Le vieillissement s’accompagne d’un risque accru de maladies auto-immunes, où le système immunitaire se met à attaquer le corps qu’il est censé protéger. Cette étude met en lumière un coupable surprenant : les dommages quotidiens à l’ADN au sein des cellules immunitaires appelées macrophages. En retraçant comment ces lésions modifient ce que les macrophages exposent aux autres cellules immunitaires, les chercheurs dévoilent un lien possible entre le vieillissement et l’apparition de maladies comme le lupus.
Les sentinelles du corps qui dévient de leur rôle
Les macrophages sont des défenseurs de première ligne qui engloutissent microbes et débris puis affichent des fragments protéiques aux cellules T, aidant le système immunitaire à décider quoi attaquer. L’équipe a conçu des souris dont les macrophages étaient déficients pour une protéine clé de réparation de l’ADN, ERCC1-XPF, de sorte que ces cellules accumulaient des dommages persistants à l’ADN. En vieillissant, ces souris ont développé des caractéristiques d’auto-immunité : foyers inflammatoires dans les reins, dépôts d’ complexes immuns et de protéines du complément, rate hypertrophiée et taux élevés d’anticorps antinucléaires semblables à ceux observés chez des animaux âgés naturellement. Un profilage immunitaire détaillé a montré une expansion des plasmocytes, des cellules T activées et des cellules tueuses naturelles, signes d’un système immunitaire en stimulation chronique.
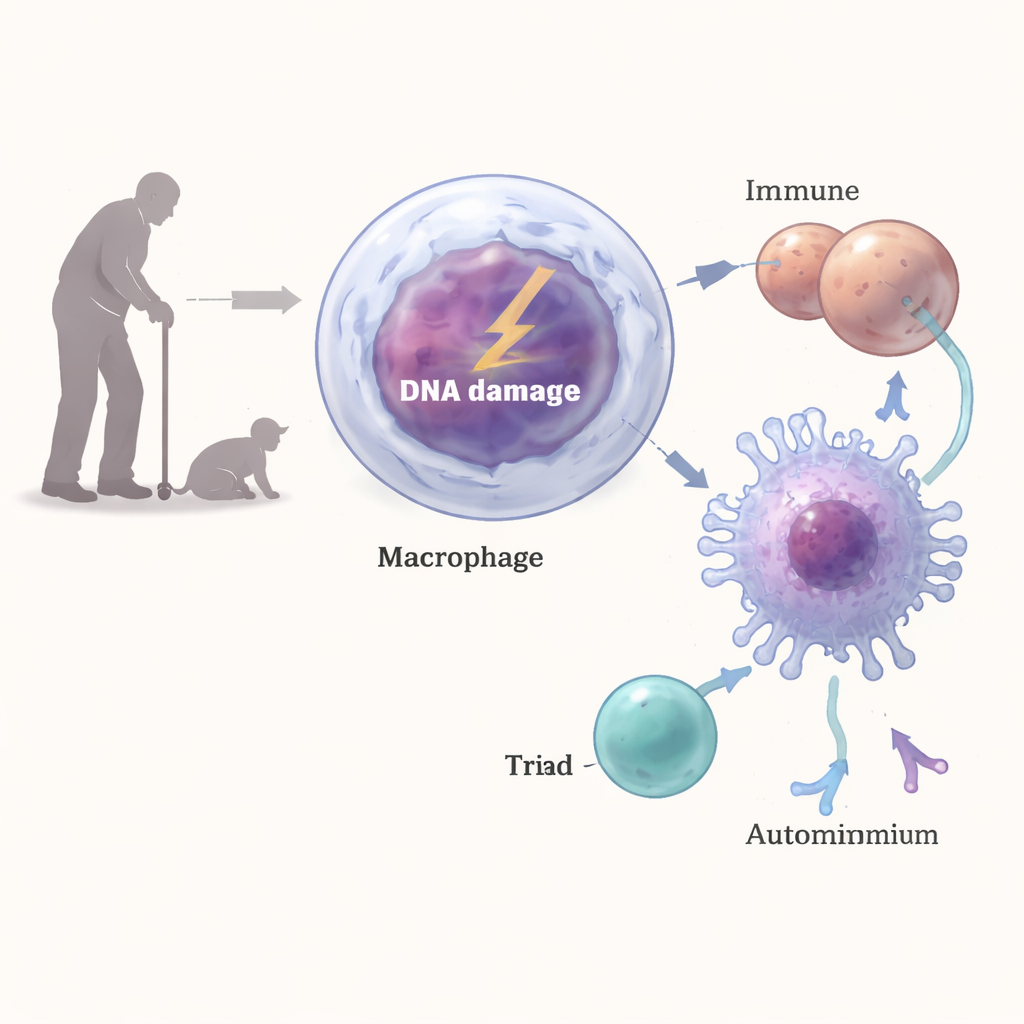
De l’ADN brisé aux cellules T qui ciblent le soi
Comment des dommages à l’ADN dans les macrophages peuvent-ils déclencher une réponse auto-immune aussi marquée ? Les chercheurs ont constaté que les cassures d’ADN activaient une voie classique de réponse aux dommages dans ces cellules, impliquant des enzymes telles qu’ATM, ATR et DNA‑PK. Cette signalisation augmentait les niveaux de MHC de classe II à la surface, les « vitrines » moléculaires utilisées pour présenter des fragments protéiques aux cellules T CD4. Lorsque des macrophages endommagés étaient mis en contact avec des cellules T, ils induisaient une activation T plus forte et une production accrue d’interféron‑gamma par rapport aux macrophages normaux. Le blocage du MHC‑II ou l’altération de la réponse aux dommages à l’ADN inversait une grande partie de cet effet, et in vivo, des anticorps bloquant le MHC‑II ou l’élimination des cellules T CD4 réduisaient l’inflammation rénale et les niveaux d’auto‑anticorps.
Des protéines nucléaires exposées en vitrine
Pour savoir exactement ce que les macrophages endommagés présentaient aux cellules T, l’équipe a isolé les peptides liés au MHC‑II et les a analysés par spectrométrie de masse. Par rapport à des cellules normales ou stimulées par lipopolysaccharide, les macrophages avec dommages à l’ADN présentaient un répertoire de peptides radicalement différent. Plutôt que des protéines membranaires et extracellulaires majoritaires, leurs molécules de MHC‑II étaient enrichies en fragments dérivés de protéines nucléaires et ribosomales, incluant des histones et d’autres composants étroitement associés à l’ADN. Lorsque certains de ces peptides nucléaires furent synthétisés et utilisés pour restimuler des cellules immunitaires issues des souris modifiées, ils déclenchaient de fortes réponses T, suggérant que ces fragments d’origine endogène étaient réellement immunogènes.
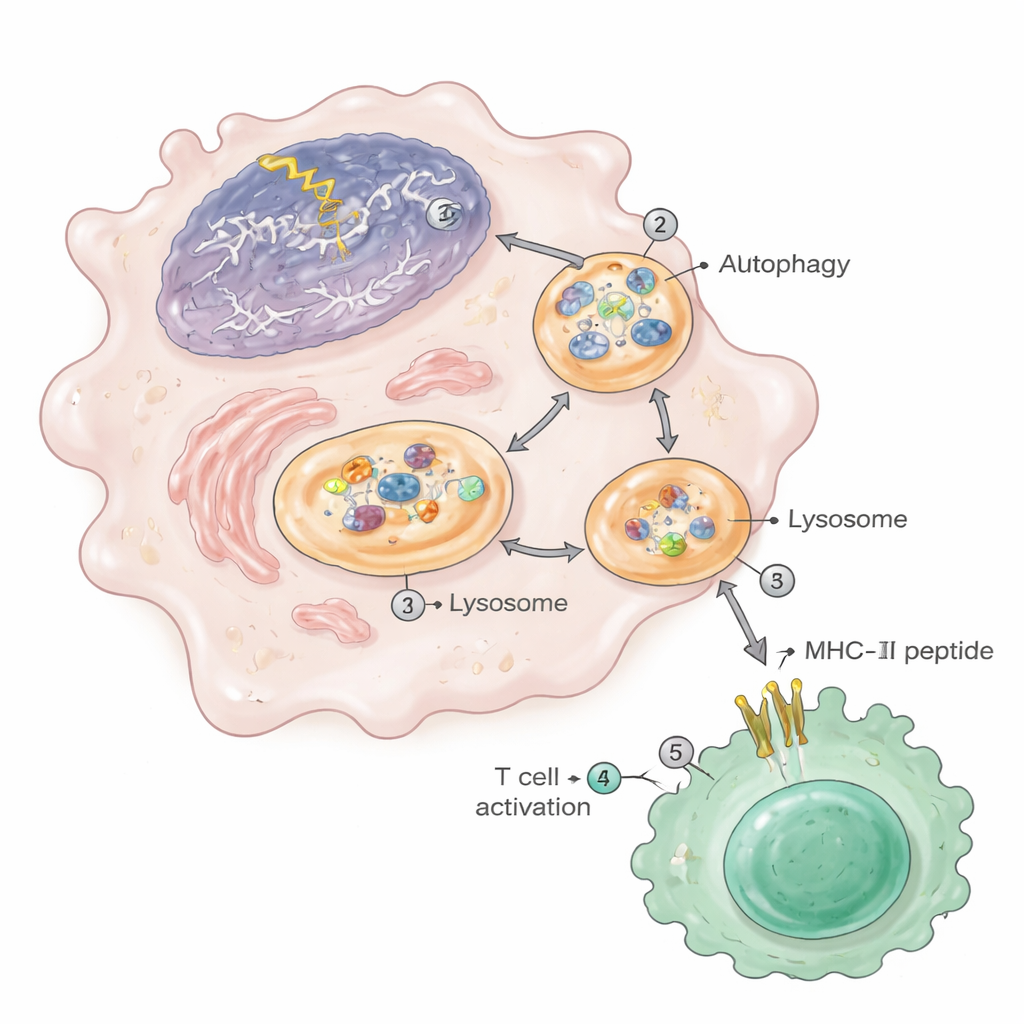
Autophagie : la voie de nettoyage qui alimente l’auto-immunité
Le trajet du matériel nucléaire jusqu’à la vitrine MHC‑II dépendait fortement de l’autophagie, le système de recyclage intracellulaire. En présence de lésions de l’ADN, l’autophagie était stimulée et achemine des fragments de chromatine — issus du noyau de la cellule — vers des autophagosomes qui fusionnent ensuite avec des lysosomes, où les protéines sont découpées en peptides. Ces lysosomes dans les macrophages endommagés contenaient des niveaux élevés de protéines nucléaires et ribosomales. Lorsque les chercheurs bloquaient l’autophagie par des médicaments ou supprimaient génétiquement un gène essentiel de l’autophagie (Atg5) dans les mêmes cellules myéloïdes, les animaux montraient moins de lésions rénales, moins de cellules T et de plasmocytes activés, et une réduction spectaculaire des peptides nucléaires apparaissant sur le MHC‑II. Des fragments de chromatine similaires et une présentation d’antigènes accrue ont été observés dans des macrophages de souris prédisposées au lupus, dans des lignées de monocytes humaines exposées à des médicaments endommageant l’ADN, et chez des macrophages de souris très âgées.
Pourquoi cela compte pour le vieillissement et les maladies auto-immunes
Pris ensemble, ces résultats suggèrent une idée simple mais puissante : en vieillissant, les dommages à l’ADN s’accumulent dans les macrophages, qui, pour dégager les débris nucléaires, sollicitent l’autophagie. Ce faisant, ils fragmentent involontairement le matériel nucléaire en peptides qui sont chargés sur le MHC‑II et présentés aux cellules T comme s’il s’agissait d’un élément étranger. Au fil du temps, cette exposition chronique à des auto‑antigènes nucléaires peut entraîner l’apprentissage d’une réaction immunitaire contre le soi, favorisant l’auto‑immunité. En identifiant précisément cette voie — des dommages à l’ADN à l’autophagie jusqu’à la présentation d’antigènes nucléaires — l’étude met en lumière de nouvelles stratégies pour atténuer l’auto-immunité liée à l’âge, comme renforcer la réparation de l’ADN, ajuster l’autophagie ou bloquer sélectivement la présentation de peptides nucléaires endogènes sans compromettre les défenses vitales du système immunitaire.
Citation: Niotis, G., Arvanitaki, E.S., Theodorakis, E. et al. DNA damage in macrophages drives immune autoreactivity via nuclear antigen presentation. Nat Aging 6, 393–413 (2026). https://doi.org/10.1038/s43587-025-01053-3
Mots-clés: vieillissement et auto-immunité, dommages à l’ADN, macrophages, autophagie, anticorps antinucléaires