Clear Sky Science · fr
Analyses exploratoires des résultats cliniques de l’étude de phase 1b du BIIB080 dans la maladie d’Alzheimer légère
Pourquoi cette recherche compte pour les familles
La maladie d’Alzheimer érode lentement la mémoire, l’autonomie et l’identité ; les médicaments actuels n’apportent qu’un soulagement limité. La plupart des nouvelles thérapies se sont concentrées sur l’élimination d’un coupable, la protéine amyloïde, avec un impact limité sur l’autre marqueur clé de la maladie : des agrégats emmêlés d’une protéine appelée tau à l’intérieur des neurones. Cette étude a exploré si un médicament expérimental, le BIIB080, qui vise à réduire la production de tau à sa source génétique, pourrait ralentir en toute sécurité la perte de mémoire et le déclin fonctionnel au quotidien chez des personnes atteintes d’une forme précoce d’Alzheimer.
Une nouvelle façon de diminuer une protéine problématique
Plutôt que de cibler la tau après la formation des enchevêtrements, le BIIB080 intervient un cran en amont. Il s’agit d’un oligonucléotide antisens, un court brin d’acide nucléique synthétique conçu pour se lier au message utilisé par les cellules pour produire la tau. En se fixant sur ce message, le BIIB080 incite les cellules à le détruire, réduisant ainsi la quantité globale de tau produite par le cerveau, y compris les formes jugées particulièrement toxiques. L’espoir est qu’en produisant moins de nouvelle tau, les enchevêtrements existants pourraient diminuer et se propager plus lentement, atténuant les lésions des circuits cérébraux à l’origine des troubles de la mémoire et des fonctions cognitives dans la maladie d’Alzheimer.
Comment l’essai précoce a été conçu
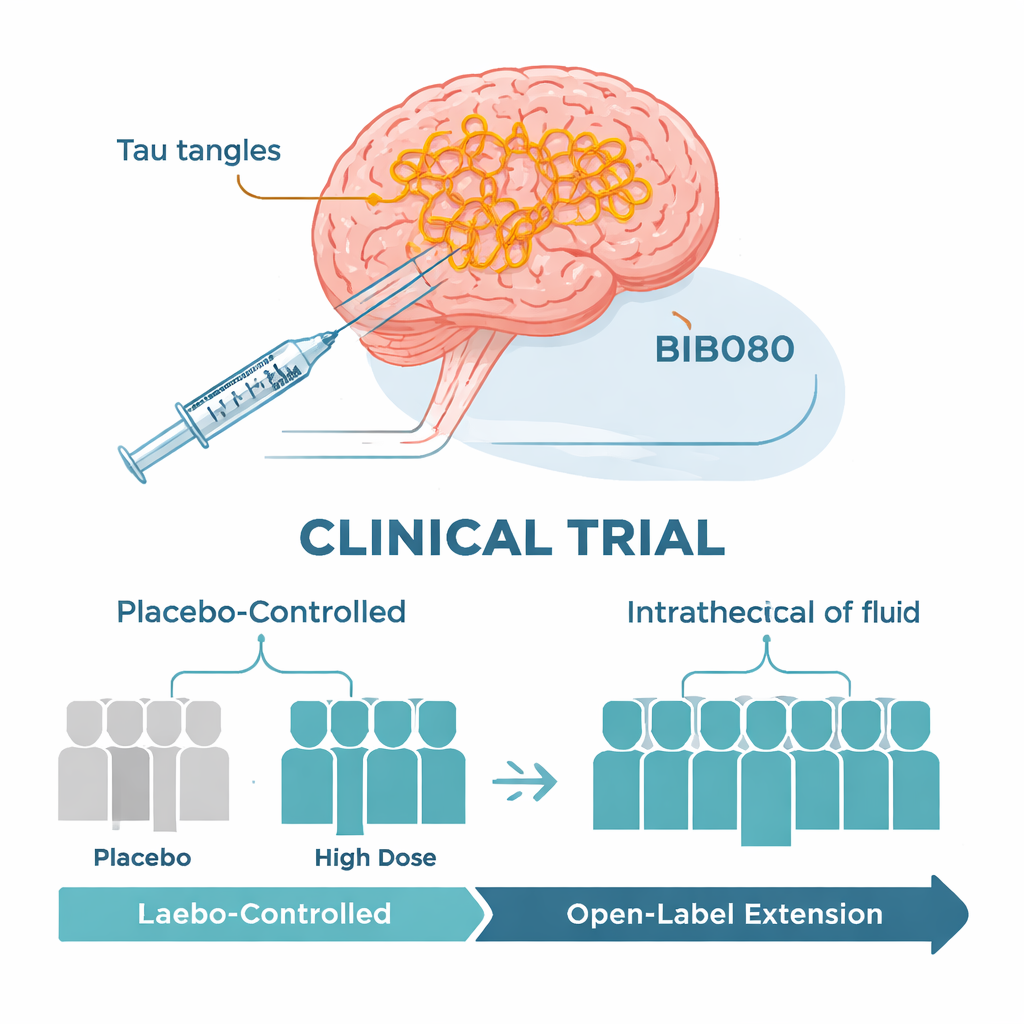
Les chercheurs ont mené un essai clinique international de phase 1b principalement destiné à évaluer la sécurité. Un peu plus de 100 personnes âgées de 50 à 74 ans atteintes d’une forme légère d’Alzheimer, confirmée par des analyses du liquide céphalorachidien, ont été incluses. Dans la première partie de l’étude, les participants ont été répartis au hasard pour recevoir le BIIB080 ou un placebo par injections périodiques dans le liquide entourant la moelle épinière sur trois mois, puis suivis pendant plusieurs mois supplémentaires. Différents groupes ont reçu des doses progressivement plus élevées. Une extension à long terme a ensuite suivi, dans laquelle tout le monde a reçu ce que l’équipe considérait comme une dose élevée de BIIB080 pendant près d’un an. Comme il n’y avait pas de groupe placebo dans cette seconde phase, les scientifiques ont comparé les patients traités avec des patients bien appariés issus d’autres grandes études sur l’Alzheimer.
Signaux d’un ralentissement du déclin cognitif et fonctionnel
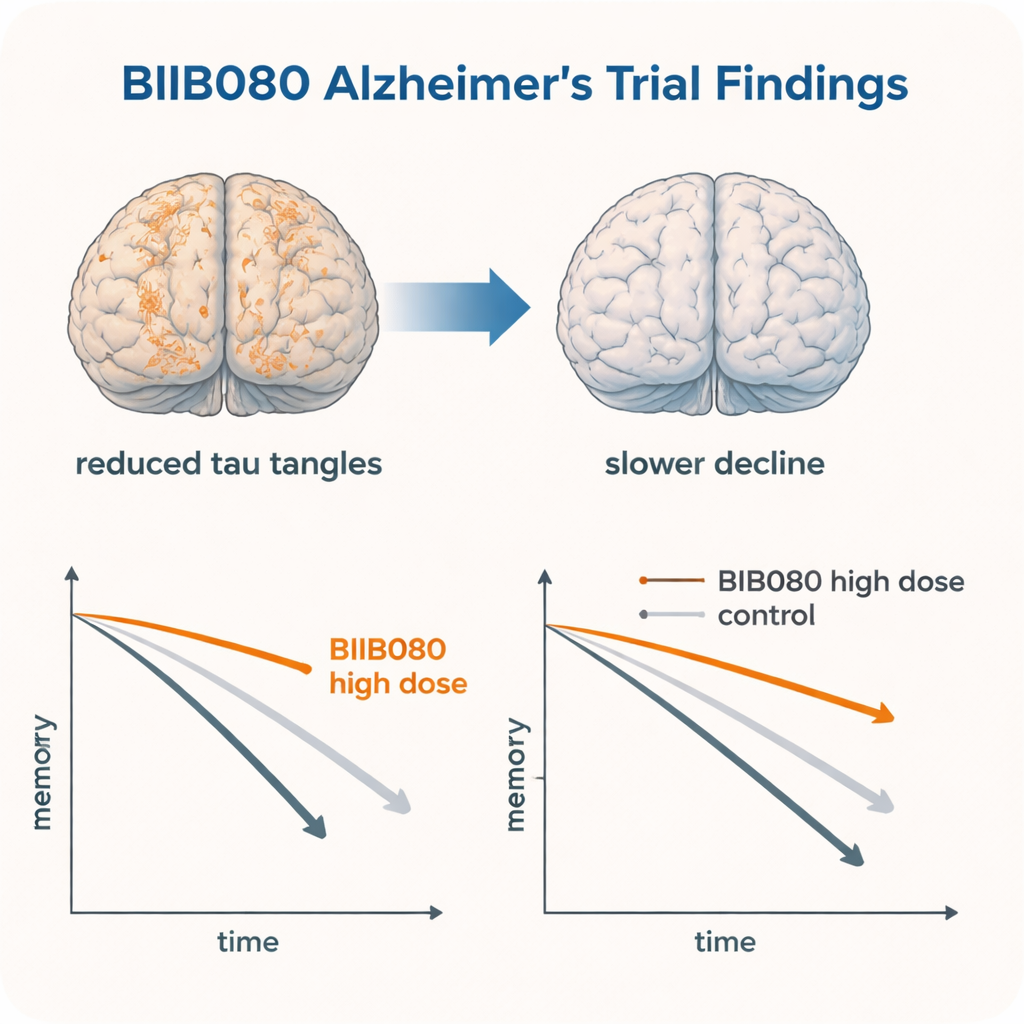
Bien que l’étude soit de petite taille et ne vise pas à démontrer l’efficacité, plusieurs tendances se sont dégagées. Les personnes ayant reçu des doses plus élevées de BIIB080 ont montré, en moyenne, une moins grande détérioration aux tests standard de la cognition (comme le Mini-Mental State Examination), de la mémoire et de la capacité à accomplir les tâches quotidiennes que celles sous placebo au cours des premiers mois. Dans l’extension à long terme, 16 participants restant sous fortes doses ont été comparés à des « témoins externes » soigneusement appariés provenant d’un autre essai axé sur la tau et d’une grande base de données de recherche sur l’Alzheimer. Sur plusieurs mesures — évaluation globale de la démence, scores cognitifs et questionnaires fonctionnels — le groupe traité par BIIB080 a tendance à décliner plus lentement que ces groupes de comparaison sur environ deux ans à partir du début du traitement.
Modifications cérébrales concordantes avec les tendances cliniques
Des rapports antérieurs issus du même essai avaient déjà montré que le BIIB080 réduisait fortement les niveaux de tau dans le liquide céphalorachidien et, de façon frappante, diminuait la quantité d’enchevêtrements de tau observés sur des scanners cérébraux spécialisés dans de nombreuses régions. Les résultats cliniques exploratoires de cette étude s’alignent sur ces changements biologiques : là où les enchevêtrements de tau ont diminué, les fonctions cognitives et la vie quotidienne semblaient se détériorer plus lentement. Dans des modèles animaux surexprimant la tau, des médicaments antisens similaires avaient non seulement réduit les dépôts de tau mais aussi atténué les crises, la perte de neurones et les troubles du comportement. Ensemble, ces éléments suggèrent que diminuer la production de tau à sa source pourrait véritablement modifier le cours de l’Alzheimer, et pas seulement masquer les symptômes.
Sécurité, limites et étapes suivantes
La plupart des effets secondaires du BIIB080 dans cet essai étaient légers à modérés et liés aux injections spinales elles‑mêmes, tels que maux de tête, douleurs dorsales ou vertiges temporaires. Quelques participants ont développé des problèmes plus graves, y compris une aggravation des symptômes de démence, et ont arrêté le traitement, si bien qu’une surveillance attentive reste essentielle. Surtout, l’étude était de petite taille, utilisait plusieurs groupes de doses avec des caractéristiques initiales inégales et s’est appuyée sur des données externes une fois que tous recevaient le médicament actif. Les auteurs insistent donc sur le fait que les tendances encourageantes pourraient encore tenir du hasard ou de biais subtils.
Ce que cela pourrait signifier pour les traitements futurs
Pour les personnes confrontées à la maladie d’Alzheimer, ces résultats n’offrent pas encore de nouvelle thérapie approuvée, mais ils pointent vers une voie prometteuse. Le BIIB080 semble réduire en toute sécurité les enchevêtrements de tau dans le cerveau humain et est associé à un ralentissement du déclin clinique dans cette étude précoce, en particulier à des doses plus élevées. Étant donné le caractère exploratoire de l’essai, des études plus vastes et plus rigoureuses sont nécessaires pour confirmer si le médicament ralentit réellement la perte de mémoire et préserve l’autonomie. Un essai de phase 2 nommé CELIA, qui suivra davantage de patients sur une période plus longue, est actuellement en cours. Si les résultats futurs se confirment, les thérapies visant à réduire la production de tau pourraient s’ajouter aux médicaments ciblant l’amyloïde ou les compléter, offrant une approche plus globale pour modifier l’évolution de l’Alzheimer.
Citation: Shulman, M., Wu, S., Ziogas, N. et al. Exploratory analyses of clinical outcomes from the BIIB080 phase 1b study in mild Alzheimer’s disease. Nat Aging 6, 445–453 (2026). https://doi.org/10.1038/s43587-025-01031-9
Mots-clés: Maladie d’Alzheimer, protéine tau, thérapie antisens, essai clinique, neurodégénérescence