Clear Sky Science · fr
Les sénotoxines ciblent la sénescence via la spécificité de liaison aux lipides, le déséquilibre ionique et la reconfiguration du lipidome
Pourquoi éliminer les cellules « zombies » pourrait améliorer le traitement du cancer
En vieillissant — ou après des traitements éprouvants comme la chimiothérapie — certaines cellules cessent de se diviser mais refusent de mourir. Ces cellules « zombies », appelées cellules sénescentes, sécrètent des molécules inflammatoires qui endommagent les tissus et peuvent favoriser la réapparition des tumeurs. Cette étude explore une voie surprenante pour éliminer sélectivement ces cellules problématiques en utilisant une protéine dérivée d’un venin, ce qui pourrait rendre les traitements anticancéreux à la fois plus efficaces et plus sûrs.
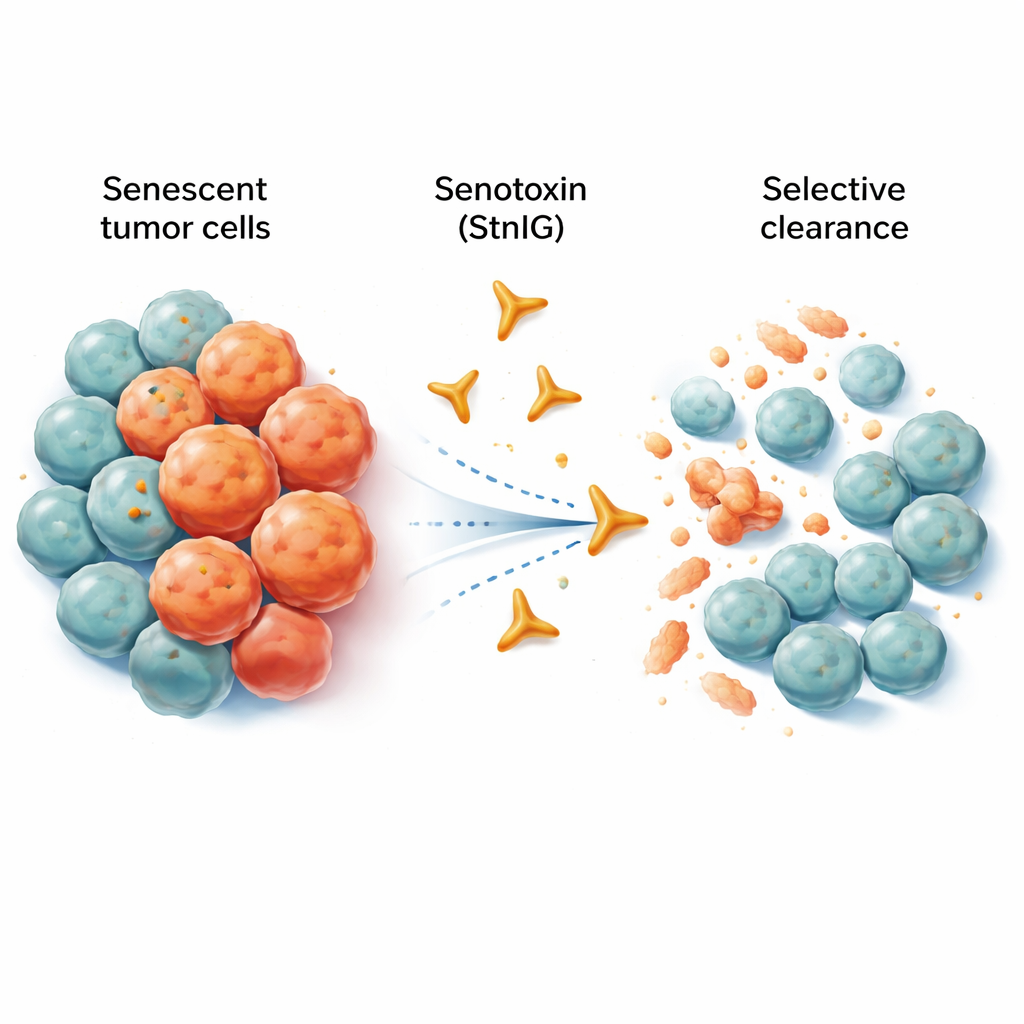
Des cellules vieillies qui refusent de partir
Les cellules sénescentes ressemblent à des travailleurs retraités qui occupent encore leur poste et perturbent le bureau. Elles ne se multiplient plus, mais elles libèrent un cocktail de signaux inflammatoires qui affaiblissent les tissus voisins, accélèrent le vieillissement et peuvent même soutenir la croissance et la dissémination des tumeurs. La chimiothérapie, tout en tuant de nombreuses cellules cancéreuses, laisse souvent derrière elle une population de cellules sénescentes dans et autour de la tumeur. Ces cellules persistantes alimentent l’inflammation chronique, les effets secondaires et, à terme, les rechutes. Les médicaments expérimentaux appelés senolytiques visent à éliminer les cellules sénescentes, mais beaucoup d’entre eux touchent aussi des cellules saines, n’agissent qu’à des doses très précises ou sont difficiles à absorber pour l’organisme.
Transformer le venin d’anémone de mer en un outil de précision
Les chercheurs se sont tournés vers les spécialistes naturels de l’élimination cellulaire : les venins d’animaux. Ils ont étudié une protéine formant des pores, la sticholysine I (StnI), présente chez une anémone de mer des Caraïbes. Cette protéine peut percer de minuscules trous dans les membranes cellulaires. L’équipe a découvert que StnI, et une version affinée qu’ils ont conçue, StnIG, tuent de façon bien plus efficace les cellules cancéreuses sénescentes que leurs voisines non sénescentes. Dans plusieurs types de cellules cancéreuses humaines (mélanome, foie, poumon et tumeurs d’origine nerveuse) induites en sénescence par des chimiothérapies, StnI et surtout StnIG ont éliminé les cellules âgées à des doses bien plus faibles que celles nécessaires pour affecter les cellules en prolifération. StnIG s’est montré plus sélectif qu’un senolytique expérimental de référence, le navitoclax, suggérant que des toxines finement réglées peuvent surpasser les approches actuelles.
Comment les membranes cellulaires modifiées deviennent un talon d’Achille
Les cellules sénescentes ne changent pas seulement à l’intérieur ; leur membrane externe — la couche lipidique qui entoure chaque cellule — se remodèle aussi. Dans les cellules saines, certains lipides se situent principalement sur la face interne de la membrane, cachés depuis l’extérieur. Dans les cellules sénescentes, cet équilibre se rompt et ces lipides deviennent exposés. À l’aide d’analyses chimiques détaillées et de simulations informatiques, l’équipe a montré que StnIG reconnaît et s’accroche à ce paysage lipidique modifié. Sa structure lui permet en particulier de se lier à des lipides spécifiques exposés à la surface des cellules sénescentes. Une fois attaché, StnIG forme des pores qui laissent passer les atomes chargés, ou ions, de façon fortement déséquilibrée.
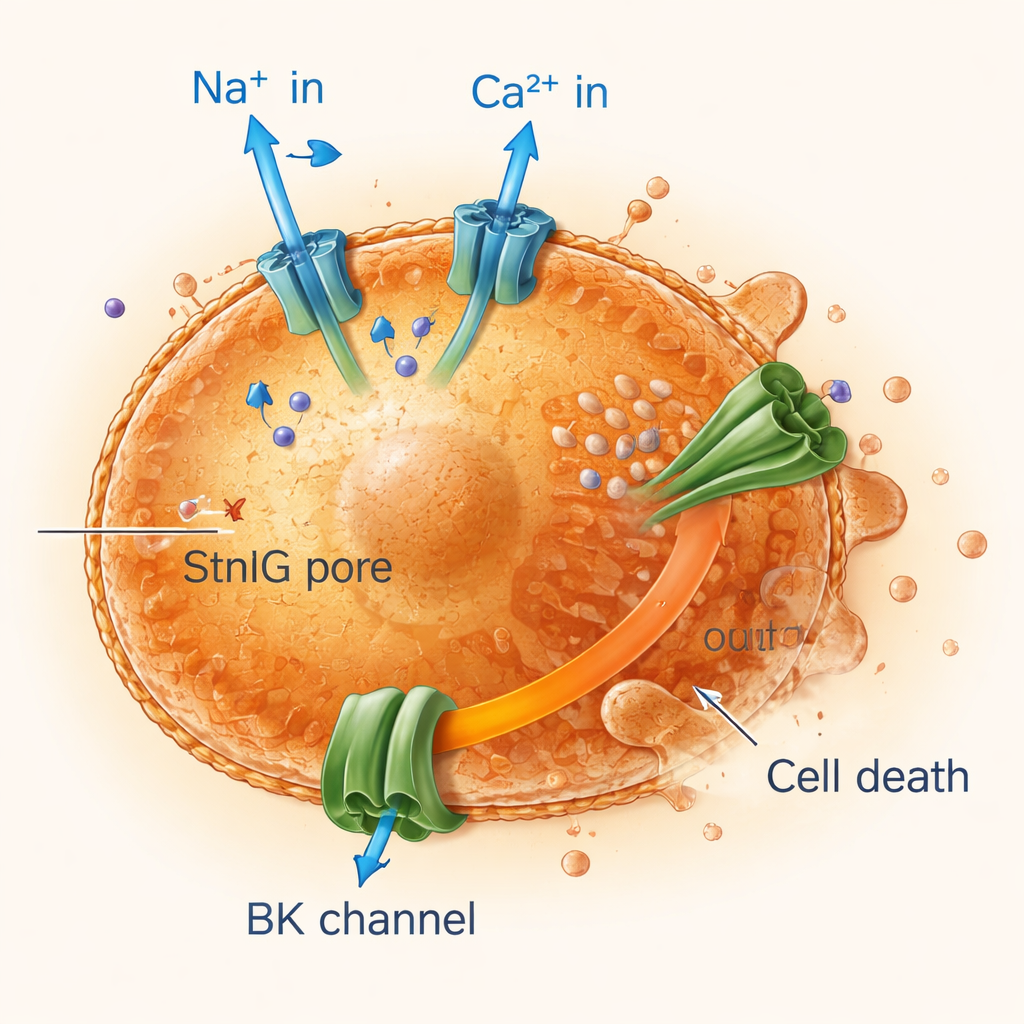
Faire court-circuiter les cellules âgées par le déséquilibre ionique
En suivant les flux électriques et ioniques à travers les membranes, les chercheurs ont constaté que les pores formés par StnIG laissent entrer massivement les ions sodium et calcium dans les cellules sénescentes tandis que le potassium s’en échappe en continu. L’afflux de calcium active de grands canaux potassiques, amplifiant la perte de potassium, essentielle au maintien du volume et de la survie cellulaire. Les cellules sénescentes, déjà moins flexibles et plus fragiles que les cellules saines, ne supportent pas cette perturbation ionique prolongée. Leurs mitochondries — centrales énergétiques de la cellule — perdent leur charge électrique, la production d’énergie chute, et les cellules déclenchent des formes programmées de mort, incluant l’apoptose et une mort inflammatoire marquée appelée pyroptose. Le blocage de l’entrée du calcium ou des canaux potassiques a protégé les cellules sénescentes, confirmant que ce dérèglement ionique est central dans l’action de la toxine.
Des puits de culture aux organismes vivants
L’équipe a ensuite testé si cette stratégie fonctionne chez l’animal. Chez des embryons de poisson-zèbre porteurs de cellules humaines sénescentes de mélanome, de faibles doses de StnIG ont réduit le nombre de ces cellules aussi efficacement que le navitoclax, sans toxicité apparente. Dans des modèles murins de mélanome et de cancer du foie, une chimiothérapie par un inhibiteur du cycle cellulaire (palbociclib) ralentissait la croissance tumorale en amenant de nombreuses cellules cancéreuses en sénescence. Lorsque les chercheurs ont ajouté StnIG de façon intermittente, les tumeurs ont rétréci ou sont entrées en rémission plus efficacement qu’avec la chimiothérapie seule, et de manière comparable à la combinaison chimiothérapie–navitoclax. Fait important, les souris traitées par StnIG ont présenté peu d’effets indésirables et aucun dommage net dans les principaux organes, bien que le potassium sanguin ait augmenté chez les animaux porteurs de tumeurs sénescentes — reflétant probablement la libération massive de potassium lors de la destruction des cellules tumorales.
Ce que cela signifie pour les soins anticancéreux futurs
Ce travail introduit les « sénotoxines » : des protéines inspirées du venin et conçues pour exploiter les particularités membranaires et ioniques des cellules sénescentes. En ciblant les lipides altérés et en provoquant des déséquilibres ioniques fatals, StnIG peut éliminer sélectivement les cellules sénescentes nuisibles tout en épargnant la plupart des tissus sains. Utilisées en complément de la chimiothérapie, ces sénotoxines pourraient un jour aider à éliminer les cellules zombies qui favorisent la rechute et l’inflammation chronique, rendant les traitements contre le cancer plus durables et réduisant potentiellement certains effets secondaires à long terme.
Citation: Moral-Sanz, J., Fernández-Carrasco, I., Ramponi, V. et al. Senotoxins target senescence via lipid binding specificity, ion imbalance and lipidome remodeling. Nat Aging 6, 349–367 (2026). https://doi.org/10.1038/s43587-025-01030-w
Mots-clés: sénescence cellulaire, senolytiques, thérapie anticancéreuse, médicaments dérivés de venin, canaux ioniques