Clear Sky Science · fr
Axicabtagène ciloléucel en association avec le rituximab pour le lymphome diffus à grandes cellules B réfractaire : essai de phase 2 monocentrique ZUMA-14
Pourquoi ce nouveau traitement du lymphome est important
Pour les personnes atteintes d’un cancer du sang agressif appelé lymphome diffus à grandes cellules B, la chimiothérapie standard ne fonctionne pas toujours, et même des traitements cellulaires puissants peuvent perdre de leur efficacité avec le temps. Cette étude a testé une nouvelle stratégie : combiner une thérapie cellulaire immunitaire personnalisée avec un anticorps utilisé depuis longtemps afin de vérifier si attaquer le cancer sur deux fronts pouvait empêcher sa récidive sans ajouter d’effets indésirables dangereux.
Deux médicaments qui s’associent contre un même cancer
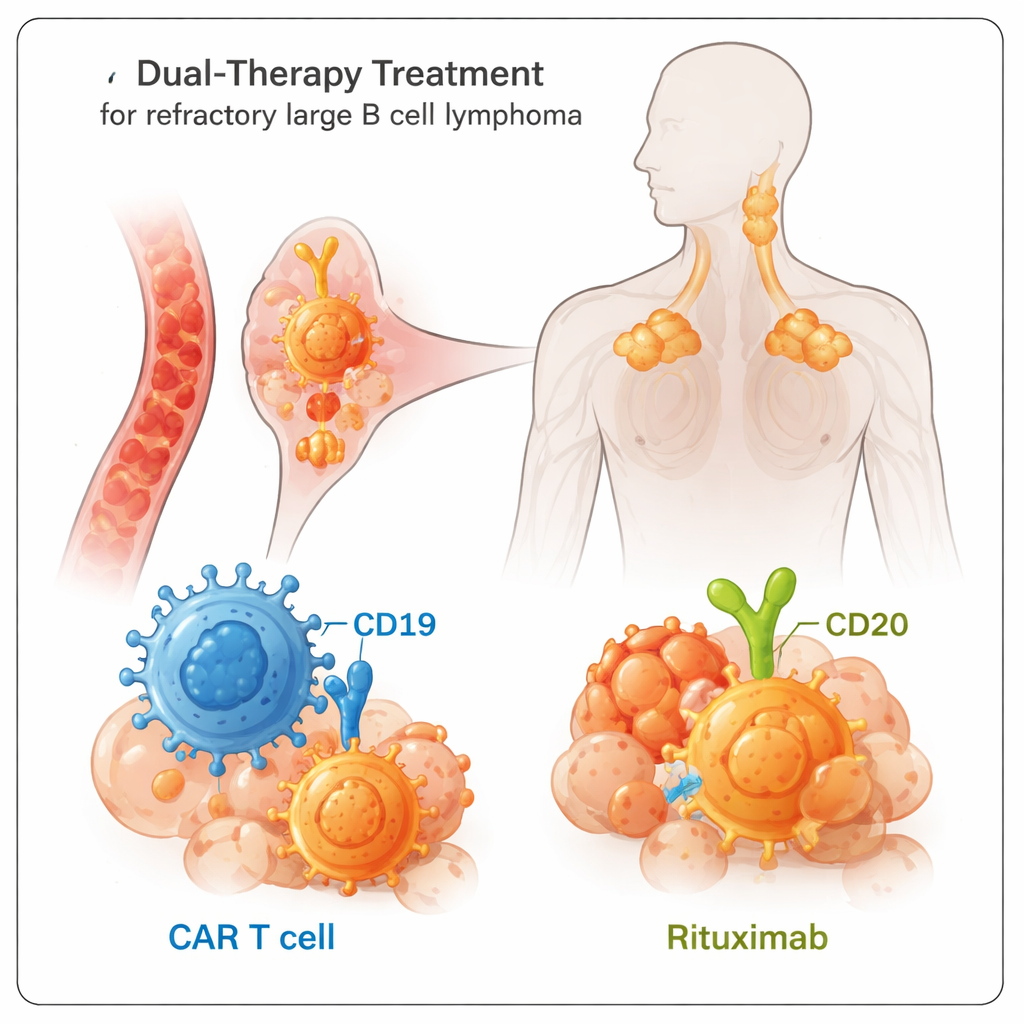
L’essai portait sur des adultes dont le lymphome n’avait pas répondu aux traitements antérieurs, un groupe qui a généralement de mauvais pronostics. Tous les participants ont reçu de l’axicabtagène ciloléucel, ou axi‑cel, un type de thérapie CAR T fabriqué à partir de leurs propres lymphocytes T modifiés pour cibler les cellules exprimant un marqueur appelé CD19. En complément, ils ont reçu du rituximab, un anticorps qui se lie à un marqueur différent sur les mêmes cellules cancéreuses, appelé CD20. L’idée était simple mais puissante : en frappant deux cibles sur les cellules lymphomateuses simultanément, le cancer serait moins à même de « s’échapper » en perdant l’un de ces marqueurs.
Réponses plus fortes et plus durables
Parmi les 26 personnes ayant reçu les deux traitements, près de 9 sur 10 ont vu leurs tumeurs diminuer et presque les trois quarts n’avaient plus de signes détectables de cancer à l’imagerie, soit une réponse complète. Bon nombre de ces réponses profondes n’étaient pas de simples succès éphémères. À un peu plus de deux ans de suivi, presque la moitié des participants présentaient encore des réponses en cours. La durée médiane de la réponse était d’environ 26 mois, et le délai médian sans progression de la maladie approchait les deux ans. La survie globale n’était pas atteinte au moment de l’analyse, ce qui signifie que plus de la moitié des patients étaient encore en vie.
Les effets secondaires restent graves mais gérables
Parce que les thérapies CAR T stimulent fortement le système immunitaire, elles peuvent provoquer des effets indésirables intenses, notamment un syndrome de libération de cytokines et des symptômes neurologiques transitoires. Dans cette étude, presque tous ont présenté un certain degré de réaction immunitaire, mais il est important de noter qu’aucun patient n’a développé les grades les plus sévères du syndrome de libération de cytokines, et des manifestations neurologiques graves sont survenues chez environ 15 % des patients ; tous ces épisodes se sont finalement résolus. Des cytopénies et des infections étaient fréquentes, comme prévu, mais l’ajout du rituximab ne semblait pas aggraver nettement ces complications comparé aux études antérieures d’axi‑cel seul. Deux patients ont développé un second cancer hématologique, un risque rare mais connu à long terme avec les thérapies immunitaires puissantes.
Indices sur qui profite le plus
Les chercheurs ont également exploré la biologie sous-jacente au succès ou à l’échec de la combinaison. Les personnes dont le sang montrait des niveaux plus élevés de cellules CAR T et une exposition au rituximab plus importante avaient tendance à afficher les réponses les plus fortes et les plus durables. Très peu de patients avaient des lymphocytes B normaux — le type de cellule qui devient cancéreux dans cette maladie — pendant une année complète après le traitement, montrant que la thérapie restait active. Les échantillons tumoraux prétraitement suggéraient que les cancers déjà riches en certains types de cellules immunitaires, comme les cellules NK et les lymphocytes T à mémoire, étaient plus susceptibles de rester en rémission à long terme. Les tests sanguins pour détecter des fragments d’ADN tumoral laissaient également entendre que la détection précoce de quantités infimes de maladie résiduelle pouvait prédire une rechute ultérieure.
Ce que cela signifie pour l’avenir
Pour les patients dont le lymphome a résisté à plusieurs lignes de traitement, la combinaison axi‑cel et rituximab a offert des taux de réponse élevés et de nombreuses rémissions durables sans introduire de problèmes de sécurité inattendus. Bien que l’essai soit de petite taille et dépourvu de bras comparatif direct, ses résultats soutiennent l’idée que cibler les cellules cancéreuses via CD19 et CD20 peut aider à empêcher la tumeur de contourner une thérapie à cible unique. Cette approche à double ciblage inspire désormais des thérapies cellulaires de nouvelle génération conçues pour intégrer ces deux attaques dans un seul produit, dans l’espoir de rendre des traitements puissants et durables plus pratiques et plus largement accessibles.
Citation: Strati, P., Leslie, L., Shiraz, P. et al. Axicabtagene ciloleucel in combination with rituximab for refractory large B cell lymphoma: the phase 2, single-arm ZUMA-14 trial. Nat Cancer 7, 304–315 (2026). https://doi.org/10.1038/s43018-025-01102-1
Mots-clés: Thérapie CAR T, lymphome diffus à grandes cellules B, rituximab, ciblage double antigène, résistance à l’immunothérapie